5. Happo-emäs -titraus
Happo-emäs -titraus
Hapon ja emäksen neutraloitumisreaktiossa oksoniumionit reagoivat hydroksidi-ionien kanssa, jolloin muodostuu vettä:
[[$H_3O^+\left(aq\right)+OH^-\left(aq\right)\ \rightarrow\ H_2O\left(l\right)$]]
Kun hapon ja emäksen neutraloitumisreaktio kirjoitetaan täydellisesti niin
happo + emäs → suola + vesi
esim jos bentsoehappoa titrataan natriumhydroksidilla niin neutraloitumisreaktio on
[[$C_6H_5COOH\left(aq\right)+NaOH\left(aq\right)\rightarrow C_6H_5COONa\left(aq\right)+H_2O\ \left(l\right)$]]
Nyt muodostuva suola, natriumbentsoaatti on vesiliuoksessa ioneina
[[$C_6H_5COONa\ \left(aq\right)\ \rightarrow\ Na^+\left(aq\right)+C_6H_5COO^-\left(aq\right)$]]
Tällöin reaktioyhtälössä näkyy mistä haposta ja emäksestä neutraloitumisreaktiossa on kyse ja mitä suolaa muodostuu.
Happo-emästitrauksessa toisen konsentraatio tunnetaan tarkasti ja toisen konsentraatio voidaan määrittää.
Jos esim emäsliuoksen konsentraatio tunnetaan ja hapon konsentraatio halutaan määrittää niin emäsliuos laitetaan pyrettiin. Emästä lisätään pyretistä hapon joukkoon.
Titrauksen ekvivalenttipiste on titrauksen päätepiste
Titrauksen kulkua voidaan seurata myös mittaamalla pH-arvoa titrauksen eri vaiheissa. Kun pystyakselilla on pH-arvo ja vaaka-akselilla titrausliukosen tilavuus, saadaan laadittua titrauskäyrä. Titrauskäyrää tulkitsemalla voidaan
Erilaisia titrauskäyriä
Vahvojen protolyyttien titrauksissa ekvivalenttikohdassa pH on tasan lähellä 7.
Kun heikkoja protolyytteja titrataan vahvoilla hapoilla tai emäksillä, ei pH ole lähellä 7
pe 13.3. tunnilla käsiteltiin tehtävät 107, 108 sekä 168 ja 170
Kotitehtävät: 109 ja 172
[[$H_3O^+\left(aq\right)+OH^-\left(aq\right)\ \rightarrow\ H_2O\left(l\right)$]]
Kun hapon ja emäksen neutraloitumisreaktio kirjoitetaan täydellisesti niin
happo + emäs → suola + vesi
esim jos bentsoehappoa titrataan natriumhydroksidilla niin neutraloitumisreaktio on
[[$C_6H_5COOH\left(aq\right)+NaOH\left(aq\right)\rightarrow C_6H_5COONa\left(aq\right)+H_2O\ \left(l\right)$]]
Nyt muodostuva suola, natriumbentsoaatti on vesiliuoksessa ioneina
[[$C_6H_5COONa\ \left(aq\right)\ \rightarrow\ Na^+\left(aq\right)+C_6H_5COO^-\left(aq\right)$]]
Tällöin reaktioyhtälössä näkyy mistä haposta ja emäksestä neutraloitumisreaktiossa on kyse ja mitä suolaa muodostuu.
- reaktioyhtälö tapahtuu täysin reaktioyhtälön kertoimien ilmoittamassa ainemääräsuhteissa
Happo-emästitrauksessa toisen konsentraatio tunnetaan tarkasti ja toisen konsentraatio voidaan määrittää.
Jos esim emäsliuoksen konsentraatio tunnetaan ja hapon konsentraatio halutaan määrittää niin emäsliuos laitetaan pyrettiin. Emästä lisätään pyretistä hapon joukkoon.
Titrauksen ekvivalenttipiste on titrauksen päätepiste
- neutraloituminen on tapahtunut täydellisesti
- happoa ja emästä on reaktioyhtälön kertoimien mukaisessa ainemääräsuhteessa
- voidaan havaita pH indikaattorin avulla, jossa tapahtuu värinmuutos liuoksen pH-arvon muuttuessa
Titrauksen kulkua voidaan seurata myös mittaamalla pH-arvoa titrauksen eri vaiheissa. Kun pystyakselilla on pH-arvo ja vaaka-akselilla titrausliukosen tilavuus, saadaan laadittua titrauskäyrä. Titrauskäyrää tulkitsemalla voidaan
- päätellä titrauksen ekvivalenttipiste ja määrittää sen avulla tutkitun liuoksen konsentraatio
- valita titraukseen sopiva indikaattori
- laskea heikon hapon happovakio tai heikon emäksen emäsvakio
Erilaisia titrauskäyriä
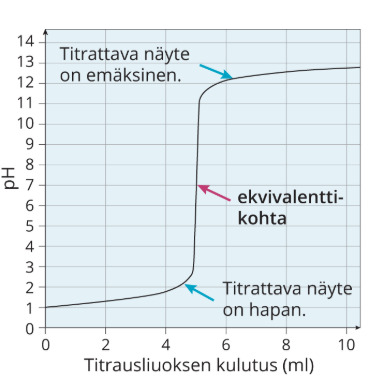
1. Vahvan hapon titraus vahvalla emäksellä

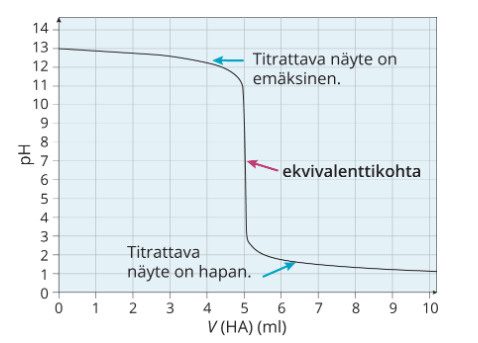
2. Vahvan emäksen titraus vahvalla hapolla

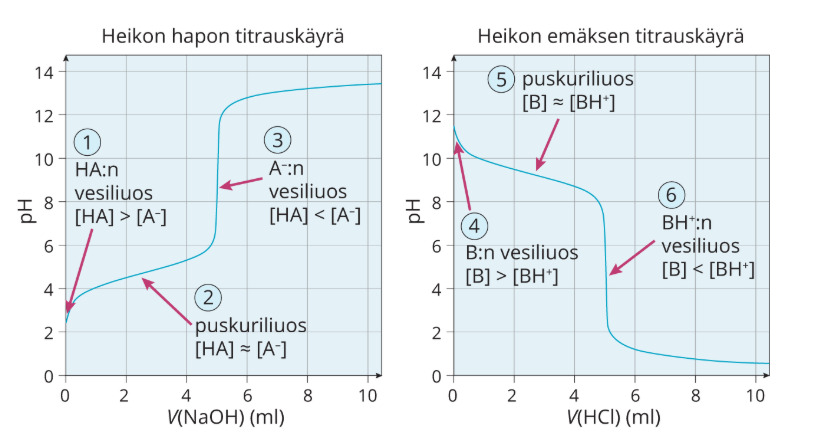
3. Heikon hapon tai emäksen titraus vahvalla emäksellä tai hapolla

Vahvojen protolyyttien titrauksissa ekvivalenttikohdassa pH on tasan lähellä 7.
Kun heikkoja protolyytteja titrataan vahvoilla hapoilla tai emäksillä, ei pH ole lähellä 7
- Heikko happo titrataan vahvalla emäksellä, pH on yli 7
- Tämä johtuu siitä, että syntyvä suolan ioni (heikko emäs) voi protolysoitua vedessä
- Heikko emäs titrataan vahvalla hapolla, pH on alle 7
pe 13.3. tunnilla käsiteltiin tehtävät 107, 108 sekä 168 ja 170
Kotitehtävät: 109 ja 172
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.