2. Kemiallinen tasapaino
Kemiallinen tasapaino ja tasapainovakio
Kemialliset reaktiot voivat edetä lähtöaineista reaktiotuotteisiin (etenevä reaktio) mutta ns. tasapainoreaktiot voivat myös palautua tuotteista takaisin lähtöaineiksi (palautuva reaktio).
esimerkiksi seuraava reaktioyhtälö on tasapainoreaktio
[[$2\ SO_2\left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\left(g\right)$]]
Tasapainotila saavutetaan, kun lähtöaineiden ja reaktiotuotteiden konsentraatiot pysyvät vakioina ts etenevä ja palautuva reaktio tapahtuvat samalla nopeudella. Tasapainotilassa lähtöaineet muuttuvat reaktiotuotteiksi yhtä nopeasti kuin tuotteet hajoavat takaisin lähtöaineiksi.
[[$A+B\ \xrightleftharpoons[v_p]{v_e}\ C+D$]]
Tässä A ja B ovat lähtöaineita sekä C ja D reaktiotuotteita
[[$v_e\ on\ etenevän\ reaktion\ nopeus\ ja\ v_p\ palautuvat\ reaktion\ nopeus$]]
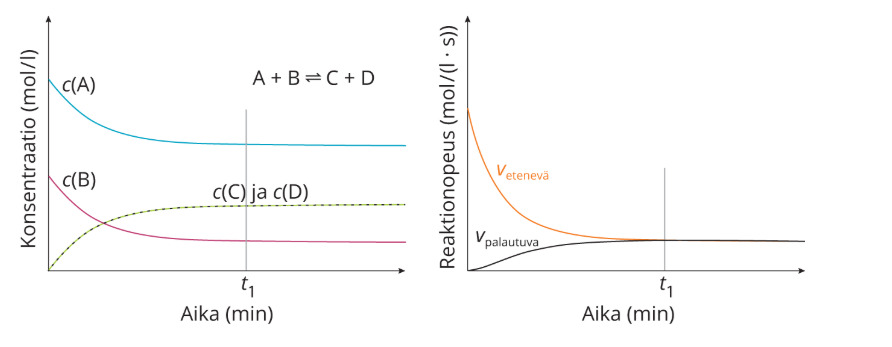
Tasapainotilassa
[[$v_e=v_p\ \ \ \Leftrightarrow\ \ k_e\ \left[A\right]\cdot\left[B\right]=k_p\left[C\right]\cdot\left[D\right]{,}\ jossa\ k_e\ ja\ k_p\ ovat\ olosuhteista\ riippuvia\ \ker toimia{,}\ verrannollisuus\ker toimia$]]
[A] tarkoittaa lähtöaineen A konsentraatiota, c(A) eli aineen konsentraatiota merkitään hakasulkeilla
[[$\Leftrightarrow\ \frac{k_e}{k_p}=\frac{\left[C\right]\cdot\left[D\right]}{\left[A\right]\cdot\left[B\right]}=K{,}\ tässä\ K\ on\ reaktion\ tasapainovakio$]]
Tasapainovakion lausekkeessa aineiden konsentraatiot ovat tasapainotilassa olevia konsentraatioita eli tasapainokonsentraatioita.
Tasapainovakion lauseke kaikille kaasuissa ja liuoksissa tapahtuville homogeenisille tasapainoreaktiolle (massavaikutuksen laki)
[[$rA+sB\ \xrightleftharpoons[]{}\ tC+qD$]]
[[$K=\frac{\left[C\right]^t\left[D\right]^q}{\left[A\right]^r\left[B\right]^s}$]]
Tasapainovakion arvo riippuu olosuhteista mm lämpötilasta.
esimerkiksi tasapainoreaktion tasapainovakion arvo
[[$2\ SO_2\left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\left(g\right)$]]
[[$K=\frac{\left[SO_3\right]^2}{\left[SO_2\right]^2\cdot\left[O_2\right]}{,}\ jonka\ yksikkö\ on\ \frac{1}{\frac{mol}{dm^3}}=\frac{dm^3}{mol}=\frac{l}{mol}$]]
Kotitehtävät: 45 ja 40
Kotitehtävät (11.2.) : 53 loppuun ja 49
esimerkiksi seuraava reaktioyhtälö on tasapainoreaktio
[[$2\ SO_2\left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\left(g\right)$]]
Tasapainotila saavutetaan, kun lähtöaineiden ja reaktiotuotteiden konsentraatiot pysyvät vakioina ts etenevä ja palautuva reaktio tapahtuvat samalla nopeudella. Tasapainotilassa lähtöaineet muuttuvat reaktiotuotteiksi yhtä nopeasti kuin tuotteet hajoavat takaisin lähtöaineiksi.
[[$A+B\ \xrightleftharpoons[v_p]{v_e}\ C+D$]]
Tässä A ja B ovat lähtöaineita sekä C ja D reaktiotuotteita
[[$v_e\ on\ etenevän\ reaktion\ nopeus\ ja\ v_p\ palautuvat\ reaktion\ nopeus$]]

Tasapainotilassa
[[$v_e=v_p\ \ \ \Leftrightarrow\ \ k_e\ \left[A\right]\cdot\left[B\right]=k_p\left[C\right]\cdot\left[D\right]{,}\ jossa\ k_e\ ja\ k_p\ ovat\ olosuhteista\ riippuvia\ \ker toimia{,}\ verrannollisuus\ker toimia$]]
[A] tarkoittaa lähtöaineen A konsentraatiota, c(A) eli aineen konsentraatiota merkitään hakasulkeilla
[[$\Leftrightarrow\ \frac{k_e}{k_p}=\frac{\left[C\right]\cdot\left[D\right]}{\left[A\right]\cdot\left[B\right]}=K{,}\ tässä\ K\ on\ reaktion\ tasapainovakio$]]
Tasapainovakion lausekkeessa aineiden konsentraatiot ovat tasapainotilassa olevia konsentraatioita eli tasapainokonsentraatioita.
Tasapainovakion lauseke kaikille kaasuissa ja liuoksissa tapahtuville homogeenisille tasapainoreaktiolle (massavaikutuksen laki)
[[$rA+sB\ \xrightleftharpoons[]{}\ tC+qD$]]
[[$K=\frac{\left[C\right]^t\left[D\right]^q}{\left[A\right]^r\left[B\right]^s}$]]
Tasapainovakion arvo riippuu olosuhteista mm lämpötilasta.
esimerkiksi tasapainoreaktion tasapainovakion arvo
[[$2\ SO_2\left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\left(g\right)$]]
[[$K=\frac{\left[SO_3\right]^2}{\left[SO_2\right]^2\cdot\left[O_2\right]}{,}\ jonka\ yksikkö\ on\ \frac{1}{\frac{mol}{dm^3}}=\frac{dm^3}{mol}=\frac{l}{mol}$]]
Kotitehtävät: 45 ja 40
Kotitehtävät (11.2.) : 53 loppuun ja 49
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tasapainon siirtäminen
Kemiallista tasapainoa voidaan siirtää muuttamalla lämpötilaa, painetta tai konsentraatiota.
Le Chatelierin periaate: Kun tasapainossa olevaan systeemiin kohdistetaan jokin ulkoinen häiriö / pakote, systeemissä tapahtuu reaktio (muutos), joka vähentää häiriön vaikutusta.
Tarkastellaan kemiallista tasapainoa
[[$A+B\ \xrightleftharpoons[]{}\ C+D{,}\ jossa\ K=\frac{\left[C\right]\left[D\right]}{\left[A\right]\left[B\right]}$]]
Jos A:n tai B:n konsentraatiot kasvavat (reaktioseokseen lisätään lähtöaineita A ja/tai B), siirtyy reaktion tasapaino vasemmalta oikealle eli [C] ja [D] lisääntyvät.
Jos vastaavasti systeemiin lisätään tuotteita C ja/tai D niin tasapaino siirtyy lähtöaineiden suuntaan eli [A] ja [B] lisääntyvät.
Paine vaikuttaa reaktion tasapainoon, jos
tarkastellaan esimerkkinä tasapainoa
[[$2\ SO_2\ \left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\ \left(g\right)$]]
Nyt lähtöaineiden puolella on 3 mol kaasuja ja tuotteiden puolella 2 mol kaasuja.
Merkitään lähtöaineiden ainemääriä a ja b sekä tuotteen ainemäärää d
[[$\begin{array}{l|l} &2SO_2\left(g\right)+O_2\left(g\right)\xrightleftharpoons[]{}2SO_3\left(g\right)\\ \hline konsentraatio&\ \ \frac{a}{V}\ \ \ \ \ \ \ \ \ \ \ \ \ \frac{b}{V}\ \ \ \ \ \ \ \ \ \ \ \ \ \frac{d}{V} \end{array}$]]
[[$K=\frac{\left[SO_3\right]^2}{\left[SO_2\right]^2\left[O_2\right]}=\frac{\frac{d^2}{V^{^2}}}{\frac{a^2}{V^2}\cdot\frac{b}{V}}=\frac{d^2V}{a^2b}$]]
Jos tilavuutta pienennetään, paine kasvaa ⇒ d kasvaa sekä a ja b pienenevät eli tasapaino siirtyy oikealle tuotteiden suuntaan.
Tasapainossa olevassa kaasusysteemissä paineen kasvu aiheuttaa reaktio siirtymisen siihen suuntaan, jossa kaasujen kokonaisainemäärä on pienempi.
Reaktion tasapainovakiolla K on tietty vakioarvo eri lämpötiloille, joten muuttamalla lämpötilaa K muuttuu.
Lämpötilan nosto aiheuttaa tasapainossa olevaan systeemiin muutoksen, joka sitoo lämpöenergiaa eli tapahtuu endoterminen reaktio.
Katalyytillä ei ole vaikutusta tasapainovakion arvoon. Se nopeuttaa vain reaktion tasapainovakion saavuttamista.
Le Chatelierin periaate: Kun tasapainossa olevaan systeemiin kohdistetaan jokin ulkoinen häiriö / pakote, systeemissä tapahtuu reaktio (muutos), joka vähentää häiriön vaikutusta.
1. Konsentraation vaikutus
Tarkastellaan kemiallista tasapainoa
[[$A+B\ \xrightleftharpoons[]{}\ C+D{,}\ jossa\ K=\frac{\left[C\right]\left[D\right]}{\left[A\right]\left[B\right]}$]]
Jos A:n tai B:n konsentraatiot kasvavat (reaktioseokseen lisätään lähtöaineita A ja/tai B), siirtyy reaktion tasapaino vasemmalta oikealle eli [C] ja [D] lisääntyvät.
Jos vastaavasti systeemiin lisätään tuotteita C ja/tai D niin tasapaino siirtyy lähtöaineiden suuntaan eli [A] ja [B] lisääntyvät.
2. Paineen vaikutus
Paine vaikuttaa reaktion tasapainoon, jos
- reaktioon ottaa osaa kaasuja ja
- lähtöaineiden ja reaktiotuotteiden puolella on eri ainemäärät kaasumooleja.
tarkastellaan esimerkkinä tasapainoa
[[$2\ SO_2\ \left(g\right)+O_2\left(g\right)\ \ \xrightleftharpoons[]{}\ 2\ SO_3\ \left(g\right)$]]
Nyt lähtöaineiden puolella on 3 mol kaasuja ja tuotteiden puolella 2 mol kaasuja.
Merkitään lähtöaineiden ainemääriä a ja b sekä tuotteen ainemäärää d
[[$\begin{array}{l|l} &2SO_2\left(g\right)+O_2\left(g\right)\xrightleftharpoons[]{}2SO_3\left(g\right)\\ \hline konsentraatio&\ \ \frac{a}{V}\ \ \ \ \ \ \ \ \ \ \ \ \ \frac{b}{V}\ \ \ \ \ \ \ \ \ \ \ \ \ \frac{d}{V} \end{array}$]]
[[$K=\frac{\left[SO_3\right]^2}{\left[SO_2\right]^2\left[O_2\right]}=\frac{\frac{d^2}{V^{^2}}}{\frac{a^2}{V^2}\cdot\frac{b}{V}}=\frac{d^2V}{a^2b}$]]
Jos tilavuutta pienennetään, paine kasvaa ⇒ d kasvaa sekä a ja b pienenevät eli tasapaino siirtyy oikealle tuotteiden suuntaan.
Tasapainossa olevassa kaasusysteemissä paineen kasvu aiheuttaa reaktio siirtymisen siihen suuntaan, jossa kaasujen kokonaisainemäärä on pienempi.
3. Lämpötilan vaikutus
Reaktion tasapainovakiolla K on tietty vakioarvo eri lämpötiloille, joten muuttamalla lämpötilaa K muuttuu.
Lämpötilan nosto aiheuttaa tasapainossa olevaan systeemiin muutoksen, joka sitoo lämpöenergiaa eli tapahtuu endoterminen reaktio.
- Lämpötilan nousu siirtää reaktion tasapainoa endotermisen reaktion suuntaan.
- Lämpotilan lasku taas siirtää tasapainoa eksotermiseen suuntaan
Katalyytillä ei ole vaikutusta tasapainovakion arvoon. Se nopeuttaa vain reaktion tasapainovakion saavuttamista.
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.