Molekyylien väliset heikot sidokset
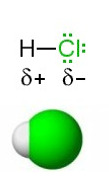
- Kovalenttinen sidos on poolinen, jos se on muodostunut kahden eri epämetalliatomin välille ja atomeilla on eri elektronegatiivisuusarvo.
- Jos molekyyli muodostuu vain kahdesta eri epämetalliatomista niin koko molekyyli on on poolinen. Muodostuu dipolimolekyyli.
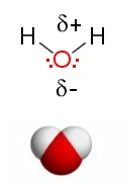
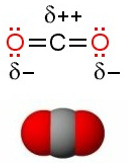
- Jos molekyyli muodostuu useammasta epämetalliatomista niin molekyylin muoto ratkaisee, onko molekyyli poolinen
- Kovalenttinen sidos on pooliton, jos se on muodostunut kahden saman epämetalliatomin (ei elektronegatiivisuuseroa) välille. Tällainen kaksiatominen molekyyli on pooliton, kuten kaikki kaksiatomiset kaasut.
1. Dispersiovoimat
- Esiintyy poolittomien molekyylien välillä esim. happomolekyylien välillä
- ovat hyvin heikkoja sidoksia, jotka aiheutuvat varausten epätasaisesta jakautumisesta molekyylien välillä
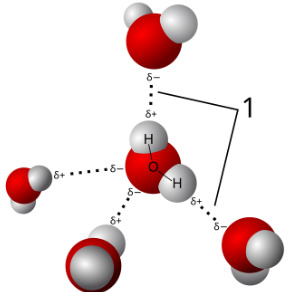
2. Dipoli - dipolisidos
- Syntyy poolisten eli dipolimolekyylien välille, jossa toisen molekyylin negat. osittaisvaraus vetää puoleensa toisen molekyylin posit. osottaisvarausta
- ovat huomattavasti voimakkaampia kuin dispersiovoimat
- dipolimolekyylien kiehumispisteet ovat suurempia kuin poolittomien molekyylien kiehumispisteet
- Vetysidos on dipoli - dipolisidoksen erikoistapaus
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.