3. Sähkökemia
Hapettumis-pelkistymisreaktiot
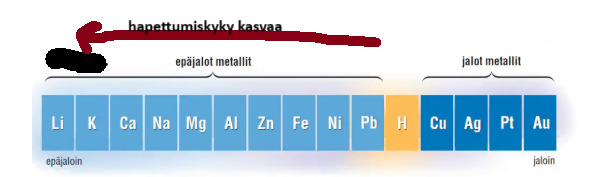
Metallien sähkökemiallinen sarja
Raudan ruostumisessa tapahtuu hapettumista. Tällöin Fe-atomi luovuttaa uloimman kuoren elektroninsa eli muodostuu positiivinen Fe2+- tai joskus Fe3+-ioni. Hapettuminen on elektronien luovuttamista. Samanaikaisesti tapahtuu myös elektronien vastaanottaminen eli pelkistyminen eli jonkin aineet täytyy vastaanottaa metalliatomien luovuttamat 1-3 uloimman kuoren valenssielektronit.
Metallit jaetaan jaloihin ja epäjaloihin metalleihin. Jaloja metalleja on vaikea saada hapettumaan.
- Epäjalot metallit hapettuvat, kun ne laitetaan esim suolahappoliuokseen (sisältää vetyioneja).
- tällöin vetyionit, H+ pelkistyvät vetykaasuksi, H2
- Esim kun magnesiumia laitetaan suolahappoliuokseen Mg-atomit hapettuvat Mg2+-ioneiksi (Mg luovuttaa 2 elektronia) ja 2H+ ionit vastaanottavat kaksi elektronia eli pelkistyvät, jolloin muodostuu vetykaasua H2
- Metallit voidaan asettaa hapettumiskykynsä mukaisesti järjestykseen eli saadaan metallien sähkökemiallinen jännitesarja
Hapetusluvut
- Hapettumisen eri tasoja merkitään hapetusluvuilla, joita merkitään yleensä roomalaisilla numeroilla
- Osa alkuaineista saa tietyn hapetusluvun johtuen sen elektronirakenteesta
- Happi saa yleensä hapetusluvun -II ja vety +I
- 1. ryhmän alkuaineet saavat hapetusluvut +I ja 2. ryhmän +II, halogeenit (17. ryhmä) taas -I
- Sivuryhmien alkuaineet, esim rauta, voivat esiintyä useilla eri hapetusluvuilla
- Hapetuslukuja määritettäessä nuodatetaan seuraavia sääntöjä
- Puhtaan alkuaineen hapetusluku on aina nolla
- Yhdisteessä alkuaineiden hapetuslukujen summa on nolla
- Ionin muodostavien alkuaineiden hapetuslukujen summa on ionin varaus

Kotitehtävät: 75, 78 ja 79
Reaktioyhtälön kertoimien määritys hapetuslukumenetelmällä
Koska hapettumis-pelkistymisreaktioissa luovutettujen ja vastaanotettujen elektronien määrät ovat yhtä suuret, niin reaktiossa tapahtuvien hapetuslukujen muutosten täytyy olla yhtä suuret.
esim. tasapainota reaktioyhtälö
Selvitetään, mikä alkuaine hapettuu ja mikä pelkistyy tässä reaktioyhtälössä
Lähtöaineet
+I -II
Tuotteet:
Kotitehtävät: 83 ja 86a,b
Sähkökemiallinen pari
Kun kaksi eri metallia kytketään saman metallin ioneja sisältävässä liuoksessa johtimella toisiinsa muodostuu sähköpari
Miten sähkökemiallisen parin tuottama jännite saadaan?
Esimerkiksi Daniellin parin antama jännite (teoreettinen) saadaan
[[$anodilla\ hapett.:\ Zn\left(s\right)\ \rightarrow\ Zn^{2+}\left(aq\right)+2e^-\ \ \ {,}\ E_h=0{,}76\ V$]]
[[$katoodilla\ pelk.:\ Cu^{2+}\left(aq\right)+2e^-\ \ \rightarrow\ Cu\left(s\right){,}\ E_p=0{,}34\ V$]]
[[$Parin\ jännite\ E=\left(0{,}76+0{,}34\right)V=1{,}1\ V$]]
Tehtäviä alkaen 92 →
Kotitehtävät: 98 ja 99
- Jotta saadaan suljettu virtapiiri, täytyy astiat yhdistää suolasillalla toisiinsa
- epäjalompi hapettuu ja jalompi pelkistyy
- Hapettuminen ja pelkistyminen saa elektronit liikkumaan johtimessa
- Esimerkkinä Daniellin pari
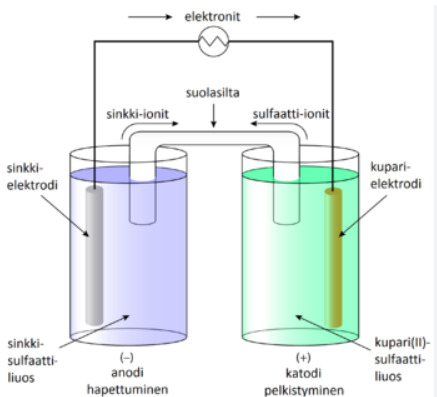
- Sinkkisulfaattiliuoksessa on sinkki- ja sulfaatti-ioneita ja kuparisulfaattiliuoksessa kupari- ja sulfaatti-ioneita
- [[$CuSO_4\left(aq\right)\ \rightarrow\ Cu^{2+}\left(aq\right)+SO_4^{2-}\left(aq\right)\ \ ja\ ZnSO_4\left(aq\right)\rightarrow Zn^{2+}\left(aq\right)+SO_4^{2-}\left(aq\right)$]]
- Anodi on negatiivinen elektrodi (kohtio), jossa tapahtuu hapettuminen.
- [[$Zn\left(s\right)\rightarrow Zn^{2+}\left(aq\right)+2e^-$]]
- Zn-ionit siirtyvät liuokseen
- Elektronit siirtyvät johdita pitkin kuparielektrodille (katodille)
- Katodi on posit. elektrodi, jossa tapahtuu pelkistyminen.
- [[$Cu^{2+}\left(aq\right)+2e^-\ \rightarrow\ Cu\left(s\right)$]]
- liuoksessa olevat kupari-ionint pelkistyvät puhtaaksi kupariksi Cu-elektrodin pintaan
- Suolasillan (jokin suolaliuos) saadaan suljettu virtapiiri. Suolasiltaa pitkin ionit siirtyvät liuoksesta toiseen.
- sähköparin kennokaavio
- [[$-\ Zn\left(s\right)\ \mid\ Zn^{2+}\left(aq\right)\ \parallel\ Cu^{2+}\left(aq\right)\ \mid\ Cu\left(s\right)\ +$]]
Miten sähkökemiallisen parin tuottama jännite saadaan?
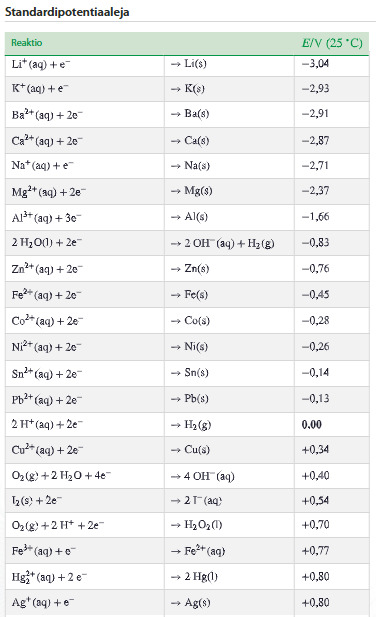
- käytetään apuna normaalipotentiaalitaulukkoa (standardipotentiaali)
- Kun katodilla tapahtuu pelkistyminen niin taulukosta saadaan suoraan pelkistymisreaktion potentiaali Ep
- Anodilla tapahtuvan hapettumispuolireaktion reaktio kirjoitetaan toisin päin eli saadaan hapettumisreaktion potentiaali Eh
- Koko reaktion potentiaali eli jännite E = Eh+Ep
Esimerkiksi Daniellin parin antama jännite (teoreettinen) saadaan
[[$anodilla\ hapett.:\ Zn\left(s\right)\ \rightarrow\ Zn^{2+}\left(aq\right)+2e^-\ \ \ {,}\ E_h=0{,}76\ V$]]
[[$katoodilla\ pelk.:\ Cu^{2+}\left(aq\right)+2e^-\ \ \rightarrow\ Cu\left(s\right){,}\ E_p=0{,}34\ V$]]
[[$Parin\ jännite\ E=\left(0{,}76+0{,}34\right)V=1{,}1\ V$]]
Tehtäviä alkaen 92 →
Kotitehtävät: 98 ja 99
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Elektrolyysi
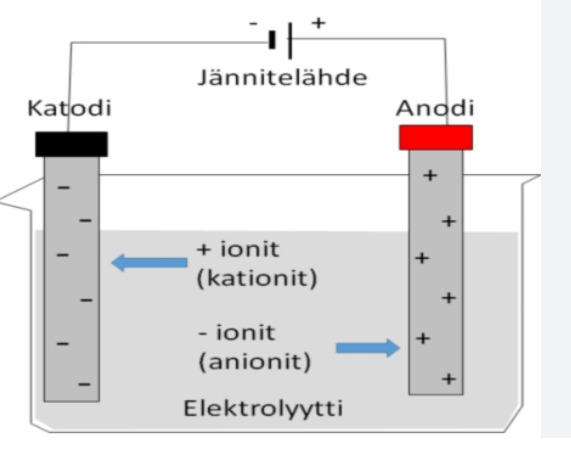
- Elektrolyysissä sähkövirran avulla saadaan aikaan pakotettu hapettumis-pelkistymisreaktio. Negatiivisella elektrodilla, katodilla tapahtuu pelkistyminen ja posit. elektrodilla, anodilla hapettuminen.
- Posit. ionit, kationit kulkevat katodille (saavat elektroneja) ja negat. ionit anionit anodilla (luovuttavat elektroneja).
- Elektrodit ovat metallia tai hiiltä. Passiviset elektrodit (hiili ja platina) eivät ota osaa reaktioon.
- Elektrolyyttiliuoksen tulee olla sähköä johtavaa.
- suolan vesiliuos tai sula suola
- Käyttökohteita
- tärkeä merkitys monien alkuaineiden, kuten natriumin, alumiinin ja kloorin valmistuksessa
- käytetään hyväksi raakakuparia puhdistettaessa
- käytetään metalliesineiden suojaukseen, galvanointiin päällystämällä ne paremmin kestävillä metalleilla
- Elektrolyyttien vesiliuoksessa on elektrolyyteistä syntyneiden ionien ja vesimolekyylien lisäksi aina myös oksonium-ioneita, H3O+ ja hydroksidi-ioneita, OH-. Liuoksessa olevat eri ionit ja vesimolekyylit "kilpailevat" reaktiojärjestyksestä elektrodeilla.
- Norm. potentiaalien arvojen avulla voidaan päätellä, missä järjestyksessä ja mitkä reaktiot elektrolyysissä tapahtuvat
- Esim tarkastellaan laimeaa NaCl:n vesiliuosta
- [[$Liuoksessa\ on\ vesimolekyylejä\ sekä\ Na^+{,}\ Cl^-{,}\ H_3O^+\ ja\ OH^-\ -ioneja$]]
- [[$Anodilla\ Cl^-\ ja\ H_2O\ kilpailevat\ hapettumisesta:$]]
[[$H_2O\left(aq\right)\xrightleftharpoons[]{}\ \frac{1}{2}O_2\left(g\right)+2H^+\left(aq\right)+2e^-\ \ {,}\ E_h=-1{,}23\ V $]]
[[$tai\ 2Cl^-\left(aq\right)\ \xrightleftharpoons[]{}\ Cl_2\left(g\right)+2e^-\ {,}\ E_h=-1{,}36\ V$]]
- Näistä ylempi tapahtuu, koska norm.potentiaali on pienempi (hapettuu helpommin)
- [[$Katodilla\ Na^{+\ }\ ja\ H_2O\ kilpailevat\ pelkistymisestä$]]
- [[$2H_2O\ \left(aq\right)+2e^-\ \xrightleftharpoons[]{}\ H_2\left(g\right)+2OH^-\left(aq\right)\ {,}\ E_p=-0{,}83\ V$]]
[[$tai\ \ Na^+\left(aq\right)+e^-\ \xrightleftharpoons[]{}\ Na\left(s\right)\ {,}\ E_p=-2{,}71\ V$]]
- Näistä ylempi tapahtuu, koska norm. potentiaali on suurempi (pelkistyy helpommin)
- Näistä tapahtuvat:
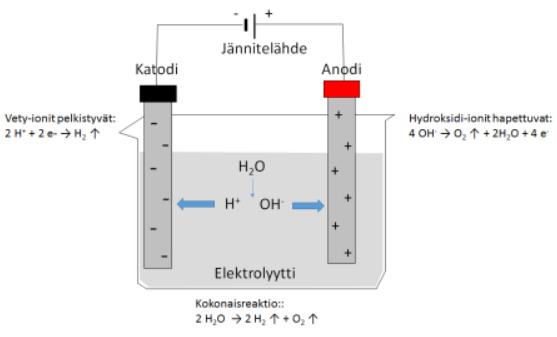
- [[$Katodilla:\ 2\ H_2O\ +2e^-\ \rightarrow\ H_2+2\ OH^-{,}\ E_p=-0{,}83\ V$]]
- [[$Anodilla:\ H_2O\ \rightarrow\ \frac{1}{2}O_2+2\ H^++2e^-\ {,}\ E_h=-1{,}23\ V$]]
- [[$Kok:\ 3\ H_2O\ \ \rightarrow\ H_2+\frac{1}{2}\ O_2+2\ H^++2\ OH^-\ eli$]]
[[$H_2O\ \rightarrow\ H_2+\ \frac{1}{2}\ O_2\ {,}\ E=-0{,}83\ V\ -1{,}23\ V=-2{,}06\ V$]]
- Laimeissa elektrolyyttien vesiliuoksissa vesi hajoaa vedyksi ja hapeksi
- [[$2\ H_2O\ \left(aq\right)\ \rightarrow\ 2\ H_2\ \left(g\right)+O_2\ \left(g\right)$]]
- Jos anodimateriaalina käytetään esim kuparia ja se hapettuu helpommin kuin elektrolyyttiliuoksen ionit tai molekyylit, hapettuu anodimateriaali esim kupari ioneina liuokseen
- [[$Cu\left(s\right)\ \rightarrow\ Cu^{2+}\left(aq\right)+2e^-$]]
- Näin voidaan kuparoida anodimateriaali
Kotitehtävät: 130 ja 131
Elektrolyysissä liikkuva sähkömäärä
Faradayn elektrolyysilaista saadaan johdettua kaava, jossa Q on sähkömäärä
[[$\left(Q=\right)\ \ It=nzF$]], jossa
[[$I=elektrolyysissä\ käytetyn\ virran\ voimakkuus$]]
[[$t=elektrolyysiin\ käytetty\ aika$]]s
[[$n=erottuneen\ aineen\ ainemäärä\ \left(=\frac{m}{M}\right)$]]
[[$z=ionin\ varaus$]]
[[$F=Faradayn\ elektrolyysivakio\ =\ 96485\ \frac{As}{mol}$]]
Kaavaa käytetään, kun lasketaan
- elektrolyysissä purkautuvien aineiden määrää
- purkautumisessa tarvittavaa sähkömäärää (virta ja /tai aika)
Jos sama virta samassa ajassa niin
[[$Q=It\ on\ vakio\ \ \Rightarrow\ \ n_1z_1F=n_2z_2F\ \ \Leftrightarrow\ n_1z_1=n_2z_2\ \ \left(kahdessa\ tilanteessa\right)$]]
Lyijyakku
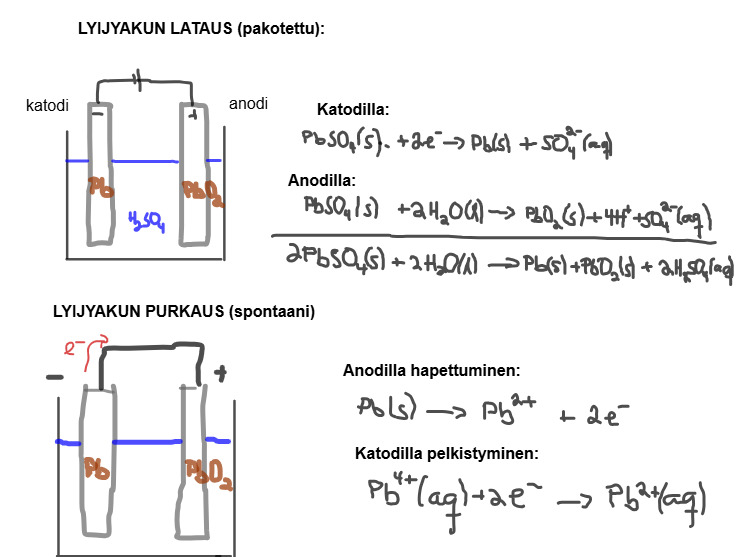
[[$Kokonaisreaktio:\ \ 2\ PbSO_4\left(s\right)+2\ H_2O\ \left(l\right)\ \ \xrightleftharpoons[purkaus]{lataus}\ Pb\left(s\right)+PbO_2\left(s\right)+2\ H_2SO_4\left(aq\right)$]]
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.