4. Metallit ja niiden ominaisuudet
Metallinjalostus ja valmistus
- Metallit eivät esiinny luonnossa vapaina vaan ne ovat maaperässä yhdisteinä, kuten erilaisina metallioksideina ja -sulfideina.
- Malmi on sellainen mineraaliesiintymä, josta on taloudellisesti kannattavaa erottaa metallia tai metalleja. Malmin on toteutettava seuraavat kriteerit:
- riittävän korkea metallipitoisuus ja laatu
- metalli on voitava erottaa mineraalista riittävän taloudellisesti
- rikkikiisusta FeS2 raudan erottaminen on kallista
- riittävän korkea metallin markkinahinta
- riittävän hyvät liikenneyhdeydet ja infra
Metallinjalostuksen vaiheet:
- Louhinta ja murskaus
- tapahtuu kaivoksessa
- Rikastus
- Sivukiven erottaminen mineraalista käyttäen fysikaalisia ja kemiallisia menetelmiä
- painovoima
- magneettierotus
- vaahdotus; mineraalit kohovat nesteen pintaan vaahdon mukana
- bioliuotus; bakteerien avulla hapetetaan sivukiven sulfaatit
- Sivukiven erottaminen mineraalista käyttäen fysikaalisia ja kemiallisia menetelmiä
- Pelkistys
- Puhdistus
- Seostaminen ja valaminen
Raudan (teräksen) valmistus

Tehtävä: Tee lyhyt yhteenveto/tiivistelmä kuparin ja alumiinin valmistusprosessista reaktioyhtälöineen.
Alla on linkki kuparin valmistukseen:
kuparin valmistus
Metallien ominaisuudet ja kierrätettävyys
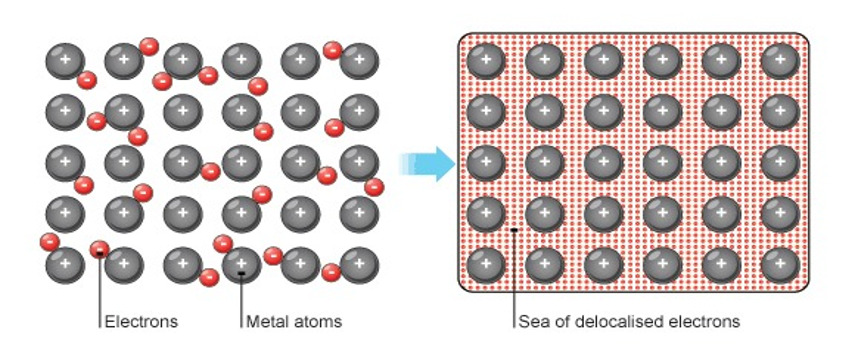
- Metalliatomit luovuttavat uloimman kuoren 1 - 3 elektronia, jolloin syntyy positiivisia metalli-ioneja ja vapaita elektroneja. Näiden välillä olevaa vahvaan sähköistä vetovoimaa kutsutaan metallisidokseksi.
- Metallien ominaisuudet:
- hyvä lämmön- ja sähkönjohtokyky
- muokattavuus
- korkea sulamispiste
- muokattavuus
- lujuus, kovuus, kiilto
- Metalliseos eli lejeerenki saadaan, kun metalleja sekoitetaan keskenään
- pronssi on kuparin ja tinan seos
- ruostumaton teräs on raudan, hiilen ja kromin seos
- Suurin osa jaksollisen järjestelmän metalleista on siirtymämetalleja
- d-orbitaalit ovat osittain täyttyneet
- ylemmän kuoren s-orbitaali täyttyy ennen alemman kuoren d-orbitaalin täyttymistä
- esiintyvät useilla hapetusluvuilla
- voivat luovuttaa s- ja d-orbitaalien elektroneja
Korroosio ja sen ehkäiseminen
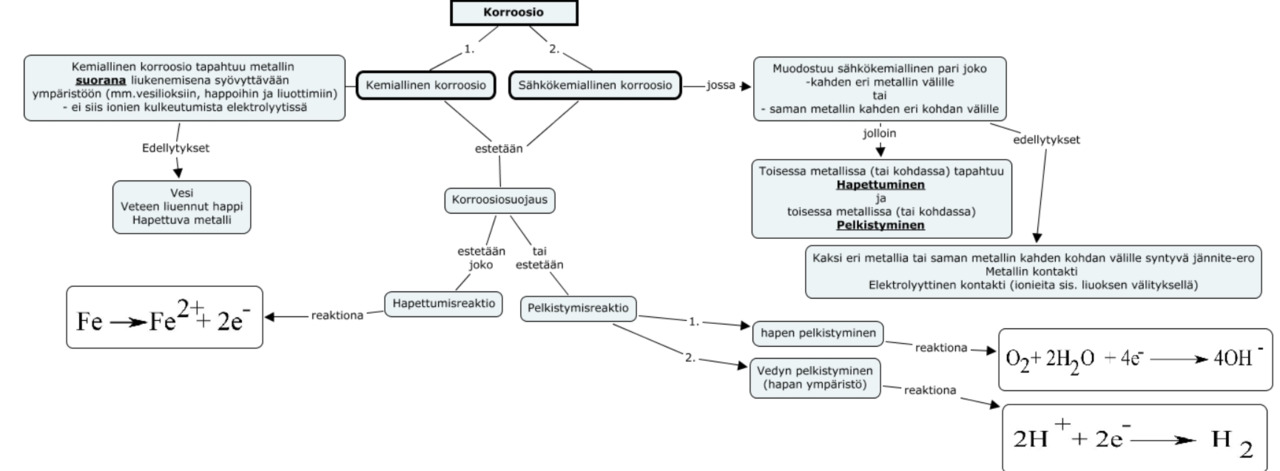
- metallien kemiallinen vahingoittuminen hapettumalla
- kyseessä on hapettumis-pelkistymisreaktio
- tarkoitetaan usein raudan ruostumista
- ruostumisen ehtona ovat ilman happi, vesi (kosteus) ja siihen liuenneet suolat
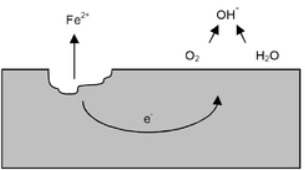
- [[$2\ Fe\rightarrow2\ Fe^{2+}+4e^-\ \ \ E_h=0{,}44\ V$]]
- [[$2\ H_2O\ +O_2+4e^-\rightarrow4OH^-\ \ E_p=0{,}40\ V$]]
- Kokonaisreaktio
- [[$2\ Fe\left(s\right)+2H_2O\left(l\right)+O_2\left(g\right)\rightarrow\ 2Fe^{2+}(aq)+4\ OH^-(aq)\ \ E=0{,}84\ V\ eli\ spontaani\ reaktio$]] ,
- Tästä rauta(II) -ionit hapettuvat edelleen rauta(III) -ioneiksi. Nämä muodostavat seoksen oksideita ja hydroksideja, joka on punertavanruskeaa ruostetta.
- Jos happi pelkistyy happamissa olosuhteissa eli pelkistymisreaktio on
- [[$O_2\left(g\right)+4\ H^+\left(aq\right)+4e^-\ \rightarrow\ 2\ H_2O\ \left(l\right){,}\ E_p=1{,}23\ V\ $]]
- niin reaktio tapahtuu edellistä helpommin. ⇒ Alhainen pH (happamat olosuhteet) lisäävät korroosiota.
- Joidenkin metallien, kuten alumiinin, pintaan muodostuu tiivis oksidikerros, joka suojaa korroosiolta
- Kupari ja hopea hapettuvat pinnaltaan ilman kosteuden ja kaasujen vaikutuksesta
- kuparin pintaan muodostuu vihreä patina, joka on lähinnä kuparikarbonaattia
- hopeaesineiden tummuminen johtuu hopeasulfidin muodostumisesta
Korroosion suojaus
- maalaaminen ja massaaminen
- galvanointi
- esim rauta voidaan päällystää sitä helpommin hapettuvalla metallilla kuten sinkillä, Zn
- Zn hapettuu Fe:n säilyessä
- esim rauta voidaan päällystää sitä helpommin hapettuvalla metallilla kuten sinkillä, Zn
- Uhrimetallin (uhrianodi) käyttö
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.