4. LÄMPÖ JA AINE Soveltavat tehtävät (451–469)
451. Veden jäähtyminen lasi- ja styroksiastiassa
Suljettavan styroksiastian ja avoimen lasiastian eristyskykyä tutkittiin. Molempiin kaadettiin 3,0 dl kuumaa vettä vedenkeittimestä. Tämän jälkeen styroksiastia suljettiin ja molempien lämpötilaa mitattiin 60 s ajan. Lämpötilat olivat oheisten mittaustulostaulukkojen mukaiset.
- Esitä mittaustulokset aika–lämpötila-koordinaatistossa. Kumpi kuvaajista esittää styroksiastiaa?
- Määritä tulosten perusteella tehot, joilla astioista siirtyi lämpöä ympäristöön.
Aineisto
Taulukko: veden_jaahtyminen.ods (LibreCalc)
Taulukko: veden_jaahtyminen.cmbl (Logger Pro)
Taulukko: veden_jaahtyminen.cap (Capstone)
Ratkaisu:
a. Ohessa on lämpötilojen kuvaajat ajan suhteen. Styroksiastia on avointa lasiastiaa paremmin eristetty, joten siitä siirtyy vähemmän lämpöä pois mittauksen aikana. Kuvaaja 2 (sininen) esittää siis styroksiastiaa, koska sen esittämä lämpötila muuttuu hitaammin.

b. Vesi luovuttaa jäähteyssään lämmön lämmön [[$ Q=cm\Delta T $]].
Veden ominaislämpökapasiteetti on [[$ c=4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja massa [[$ m=0,30 \text{ kg} $]].
Lämpö siirtyy ympäristöön teholla P, joten
[[$ P=\dfrac{Q}{t}\\ P=\dfrac{cm\Delta T}{t}=cm\dfrac{\Delta T}{t} $]]
Lauseke [[$ \frac{\Delta T}{t} $]] on a-kohdassa esitettyjen kuvaajien fysikaalinen kulmakerroin. Kulmakertoimien suuruuksiksi (itseisarvo) määritettiin mittausohjelmistolla
[[$ k_{1}= 0,07407 \frac {^\circ \text{C}}{\text{s}} $]] ja
[[$ k_{2}= 0,01767 \frac {^\circ \text{C}}{\text{s}} $]].
Lasketaan tehot.
Lasiastia: [[$ P_1=cm\dfrac{\Delta T}{t}=cm k_1=4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,30 \text{ kg}\cdot 0,07407 \frac {^\circ \text{C}}{\text{s}} =93,105\dots\text{ W}\approx 93\text{ W} $]]
Styroksiastia: [[$ P_2=cm\dfrac{\Delta T}{t}=cm k_2=4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,30 \text{ kg}\cdot 0,01767 \frac {^\circ \text{C}}{\text{s}} =22,211\dots\text{ W}\approx 22\text{ W} $]]
452. Kananmunien jäähdytys kylmässä vedessä
Ratkaisu:
Merkitään loppulämpötilaa tunnuksella T.
Kananmunat luovuttavat jäähtyessään lämmön [[$ Q_m=5C\Delta T_m $]].
Lämpökapasiteetti on [[$ C=180 \frac {\text{J}}{^\circ \text{C}} $]]. Munien lämpötilan muutos [[$ \Delta T_m $]] lasketaan positiivisena lukuna vähentämällä munien alkulämpötilasta niiden loppulämpötila [[$ T_m=100 ^\circ \text{C} $]]: [[$ \Delta T_m = T_m-T $]]
Vesi vastaanottaa lämmön [[$ Q_v=cm\Delta T_v $]].
Ominaislämpökapasiteetti on [[$ c=4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja massa [[$ m=1,5 \text{ kg} $]].Veden lämpötilan muutos [[$ \Delta T_v $]] lasketaan positiivisena lukuna vähentämällä loppulämpötilasta alkulämpötila. [[$ \Delta T_v = T-T_v $]]
Systeemi oletetaan eristetyksi, joten veden vastaanottama lämpö on yhtä suuri kuin munien luovuttama. Kirjoitetaan tämä yhtälönä ja ratkaistaan loppulämpötila.
[[$ \begin{align*}Q_j&=Q_l \\
cm \Delta T_v&=5C\Delta T_m\\
cm(T-T_v)&=5C(T_m-T)\\
cmT-cmT_v&=5CT_m-CT\\
cmT+5CT&=5CT_m+cmT_v\\
(cm+5C)T&= 5CT_m+cmT_v&||:(cm+C)\\
T&=\dfrac{5CT_m+cmT_v}{cm+5C} \\
T&=\dfrac{5\cdot180 \frac {\text{J}}{^\circ \text{C}}\cdot 100 ^\circ \text{C} +4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 1,5 \text{ kg}\cdot 11^\circ \text{C} }{4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 1,5 \text{ kg}+5 \cdot 180 \frac {\text{J}}{^\circ \text{C}}}\\
T&=21,962\dots ^\circ\text{C}\approx 22^\circ \text{C}
\end{align*} $]]
453. Veden ja metallikappaleen lämmitys uppokuumentimella
Ratkaisu:
Vesi vastaanottaa lämmön [[$ Q_v=cm\Delta T_v $]].
Veden ominaislämpökapasiteetti on [[$ c=4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]],massa [[$ m=0,40 \text{ kg} $]] ja lämpötilan muutos [[$ \Delta T_v=50\text{ } ^\circ \text{C}-8,5\text{ } ^\circ \text{C}=41,5\text{ } ^\circ \text{C} $]].
Metallikappaleeseen siirtyy lämpö [[$ Q_m=C\Delta T_m $]].
Kappaleen lämpökapasiteetti on [[$ C=375 \text{ }\frac {\text{J}}{^\circ \text{C}} $]] ja lämpötilan muutos [[$ \Delta T_m=50,0\text{ } ^\circ \text{C}-23,0\text{ } ^\circ \text{C}=27,0\text{ } ^\circ \text{C} $]].
Kokonaisuudessaan systeemiin siirtyvä lämpö on
[[$ Q=Q_v+Q_m =cm\Delta T_v +C\Delta T_m= 4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} \cdot 0,40 \text{ kg} \cdot 41,5\text{ } ^\circ \text{C} +375 \text{ }\frac {\text{J}}{^\circ \text{C}}\cdot 27,0 \text{ } ^\circ \text{C}= 79679\text{ J} $]]
Lämpö siirtyy teholla [[$ P=\dfrac{Q}{t}\\ $]], minkä perusteella voidaan ratkaista aika.
[[$ \begin{align*}P&=\dfrac{Q}{t}\\
Pt&=Q\\
t&=\dfrac{Q}{P}\\
t&=\dfrac{79679 \text{ J}}{180 \text{ s} }\\
t&=442,66 \dots \text{ s}\\
t& \approx 7 \text{ min }20\text{ s}\\
\end{align*}
$]]
454. Heikkotehoinen uppokuumennin ei saa vettä kiehumaan
Ratkaisu:
Jos veden lämpötila ei nouse keittimessä, keitin tuo lämpöä astiaan samalla teholla kuin lämpöä siirtyy ympäristöön. Tällainen tasapainotilanne voi syntyä, sillä lämpöhäviöt voimistuvat systeemin ja ympäristön välisen lämpötilaeron kasvaessa. Lämmön siirtyminen ympäristöön jatkuu samalla teholla sammutettaessa keitin.
Jäähtyessään vesi luovuttaa lämmön [[$ Q=cm\Delta T $]].
Veden ominaislämpökapasiteetti on [[$ c=4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja massa [[$ m=0,67 \text{ kg} $]].
Tehon määritelmän nojalla
[[$ P=\dfrac {Q}{t}=\dfrac {cm\Delta T}{t}=\dfrac{4190 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,67 \text{ kg}\cdot 2,5 \text{ }^\circ \text{C}}{60 \text{ s}}=116,97\dots \text{ W} \approx 120\text{ W} $]]
455. Tuntemattoman nesteen ominaislämpökapasiteetti
Tuntemattoman nesteen ominaisuuksia tutkittiin lämmittämällä sitä 65 W:n teholla hyvin eristetyssä astiassa. Nestettä oli 0,30 kg. Mitattaessa nesteen lämpötilaa ajan suhteen saatiin oheiset tulokset. Määritä tulosten perusteella nesteen ominaislämpökapasiteetti graafista esitystä hyväksikäyttäen.
|
Aika (min) |
0,0 |
1,0 |
2,0 |
3,0 |
4,0 |
5,0 |
6,0 |
7,0 |
8,0 |
|---|---|---|---|---|---|---|---|---|---|
|
Lämpötila (°C) |
21,7 |
25,6 |
30,0 |
34,0 |
37,9 |
41,8 |
45,5 |
49,7 |
53,4 |
Ratkaisu:
Nesteen vastaanottama lämpö on
[[$ Q=cm \Delta T $]]
Tehon määritelmän mukaan
[[$ P= \dfrac {Q}{\Delta t} $]], missä [[$ \Delta t $]] on lämmitykseen kuluva aika.
Siis
[[$ P= \dfrac {cm\Delta T}{\Delta t}\\
\dfrac {P}{cm}= \dfrac {\Delta T}{\Delta t}\\
$]],
joka voidaan määrittää aika–lämpötila-kuvaajan kulmakertoimena.
Esitetään tulokset aika–lämpötila-koordinaatistossa ilmaisten ajat sekunteina.

Kuvaajan fysikaaliseksi kulmakertoimeksi saadaan [[$ k=0,06608 \frac {^\circ \text{C}}{s} $]].
Määritetään nesteen ominaislämpökapasiteetti aiemmin johdetun yhtälön perusteella.
[[$ \dfrac {P}{cm}= k\\
P=kcm\\
c= \dfrac {P}{km}= \dfrac {65 \text { W}}{ 0,06608 \frac {^\circ \text{C}}{\text{s}} \cdot 0,30 \text{ kg}} = 3278,8 \dots \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} \approx 3300 \frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]]
456. Muuttuva ominaislämpökapasiteetti
Aineen ominaislämpökapasiteetti riippuu aineen lämpötilasta, mutta yleensä tämä jätetään huomioimatta. Tutki MAOL-taulukkokirjasta löytyvää kuvaajaa veden ominaislämpökapasiteetin lämpötilariippuvuudesta.
- Miten veden ominaislämpökapasiteetti muuttuu, kun veden lämpötila kasvaa 20 celsiusasteesta 80 celsiusasteeseen?
- Jos otetaan huomioon veden muuttuva ominaislämpökapasiteetti, vakiopaineessa veden lämmittämiseen 20 celsiusasteesta 80 celsiusasteeseen tarvitaan energiaa 251,1 kJ yhtä kilogrammaa vettä kohden. Kuinka suuri absoluuttinen virhe tehdään, jos tarvittavan energian määrä lasketaan käyttämällä veden ominaislämpökapasiteetille arvoa 4,1819 kJ/(kg K)?
- Miten ominaislämpökapasiteetin muuttuminen voidaan havaita tilanteessa, jossa lämmitetään vettä vakioteholla?
a. Veden ominaislämpökapasiteettin riippuvuu lämpötilasta. Taulukkokirjasta huomataan, että veden ominaislämpökapasiteetti lämpötilassa [[$ 20^\circ\text{C} $]] on noin [[$ 4{,}183 \dfrac{\text{kJ}}{\text{kg K}}. $]] Vastaavasti veden ominaislämpökapasiteetti lämpötilassa [[$ 80^\circ\text{C} $]] on noin [[$ 4{,}197\dfrac{\text{kJ}}{\text{kg K}}. $]]
Veden ominaislämpökapasiteetti muuttuu noin [[$ 4{,}197\dfrac{\text{kJ}}{\text{kg K}}-4{,}183 \dfrac{\text{kJ}}{\text{kg K}}=0{,}014 \dfrac{\text{kJ}}{\text{kg K}} \approx 10 \dfrac{\text{J}}{\text{kg K}} $]]
Vastaus: noin [[$ 10 \dfrac{\text{J}}{\text{kg K}} $]].
b. Lasketaan kuinka paljon energiaa tarvitaan yhden kilogramman vettä lämmittämiseen 20 celsiusasteesta 80 celsiusasteeseen, kun veden ominaislämpökapasiteetti on 4,1819 kJ/(kg K).
[[$ \begin{align} Q&=cm\Delta T \\ &=4{,}1819 \dfrac{\text{kJ}}{\text{kg K}}\cdot 1,0 \text{ kg} \cdot 60 \text{ K} \\ &=250,914 \text{ kJ} \end{align} $]]
Lasketaan absoluuttisen virheen suuruus.
[[$ \Delta Q=251{,}1 \text{ kJ}-250{,}914\text{ kJ}=0{,}186 \text{ kJ} $]]
Vastaus: Absoluuttisen virheen suuruus on noin 0,186 kJ.
c. Veden ominaislämpökapasiteetin arvo kasvaa lämpötilan muuttuessa 20 celsiusasteesta 80 celsiusasteeseen. Tämä tarkoittaa sitä, että veden lämmittämiseen tarvitaan enemmän energiaa jokaista celsiusastetta ja jokaista kilogrammaa kohden. Käytännössä tämä havaitaan siten, että vakioteholla vettä lämmittäessä veden lämmittäminen kestää kauemmin.
457. Kodin lämpimän käyttöveden lämmitysenergia
- Arvioi, kuinka paljon energiaa kuluu kodissasi käytettävän veden lämmitykseen vuodessa.
- Arvioi, mikä on kyseisen lämmityksen hinta sähköllä lämmitettäessä.
Ratkaisu:
a. Ei malliratkaisua, yksilöllinen tehtävä.
b. Ei malliratkaisua, yksilöllinen tehtävä.
.
458. Nesteiden haihtuminen ihon pinnalta
Ratkaisu:
Molemmat huoneenlämpöiset nesteet tuntuvat viileältä ihon pinnalla. Iho tuntuu huomattavasti viileämmältä etanolipisaran alla kuin vesipisaran alla.
Samalla määrällä vettä ja etanolia vesi tarvitsee enemmän energiaa höyrystymiseen, koska sen ominaishöyrystymislämpö on suurempi. Tämä ei kuitenkaan selitä miksi etanolin alla iho tuntuu viileämmältä.
Etanoli vaikuttaa haihtuvan nopeammin ihon pinnalta kuin vesi. Etanolin kiehumislämpötila on noin 80 celciusastetta, kun veden kiehumislämpötila on noin 100 celsiusastetta. Koska etanolin kiehumislämpötila on matalampi, niin se haihtuu nopeammin ja sitoo siten nopeammin energiaa haihtumiseen ihon pinnalta. Tämän takia etanoli tuntuu viileämmältä.
459. Kuuman ja kylmän löylyveden ero
Ratkaisu:
Kiukaan kivet luovuttavat vedelle lämpöä, jolloin se ensin lämpenee kiehumispisteeseen ja höyrystyy sitten.
Lämmetessä veteen siirtyy lämpö [[$ Q=cm\Delta T $]].
Veden ominaislämpökapasiteetti on [[$ c_j=4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja massa m.
Lämpötilan muutos on joko [[$ \Delta T_1=100 \text{ } ^\circ \text{C} - 8,0 \text{ } ^\circ \text{C}=92 \text{ } ^\circ \text{C} $]] tai [[$ \Delta T_2=100 \text{ } ^\circ \text{C} - 55 \text{ } ^\circ \text{C}=45 \text{ } ^\circ \text{C} $]].
Veden höyrystyessä siirtyy siihen lämpö [[$ Q_r=rm $]], jossa veden ominaishöyrystymislämpö on [[$ r=2 \, 260 \, 000 \text{ }\frac {\text{J}}{\text{kg}} $]]. Höyrystymisen vaatima lämpö on riippumaton veden alkulämpötilasta.
Lasketaan kokonaisenergioiden suhde eri alkulämpötiloilla:
[[$ \dfrac{cm\Delta T_1+rm}{cm\Delta T_2+rm}= \dfrac{c\Delta T_2+r}{c\Delta T_1+r}= \dfrac{4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 45 \text{ } ^\circ \text{C}+2 \, 260 \, 000 \text{ }\frac {\text{J}}{\text{kg}}}{4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 92 \text{ } ^\circ \text{C}+2 \, 260 \, 000 \text{ }\frac {\text{J}}{\text{kg}}} \approx 1,080 ^\circ \text{C}$]]
Kylmän veden käyttö löylynheitossa vaatii 8 % enemmän energiaa kuin lämpimän.
460. Riittävän kylmän mehujään syöminen ei lihota
Mehujään lämmetessä ja sulaessa siihen siirtyy lämpöä. Jään lämpeneminen sulamispisteeseen vaatii lämmön
[[$ Q_j=c_jm\Delta T_j $]].
Jään ominaislämpökapasiteetti on [[$ c_j=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]].
Massa on [[$ m=0,10 \text{ kg} $]].
Lämpötilan muutos on tuntematon.
Jään sulaessa siirtyy siihen lämpö [[$ Q_s=sm $]], jossa veden ominaissulamislämpö [[$ s=333 000 \text{ }\frac {\text{J}}{\text{kg}} $]].
Sulanut mehujää oletetaan vedeksi, joka lämpenee, jolloin siihen siirtyy lämpö
[[$ Q_v=c_v m\Delta T_v $]].
Veden ominaislämpökapasiteetti on [[$ c_v=4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]].
Massa on [[$ m=0,10 \text{ kg} $]].
Lämpötilan muutos on [[$ \Delta T_v=37\text{ } ^\circ \text{C} $]].
Kokonaisuudessaan kuluva energia
[[$ Q=80000\text{ J} $]] on näiden kolmen summa. Kirjoitetaan yhtälö, josta ratkaistaan jään lämpötilan muutos.
[[$ \begin{align*} Q_j+Q_s+Q_v&=Q\\ c_jm\Delta T_j+sm+c_vm\Delta T_v&=Q\\ c_jm\Delta T_j&=Q-sm-c_vm\Delta T_v\\ \Delta T_j&=\dfrac{Q-sm-c_vm\Delta T_v} {c_jm}\\ \Delta T_j&=\dfrac{80000 \text{ J}-333 000 \text{ }\frac {\text{J}}{\text{kg}}\cdot 0,10 \text{ kg}-4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,10 \text{ kg} \cdot 37 \text{ } ^\circ \text{C}}{2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,10 \text{ kg} }\\ \Delta T_j&= 149,26 \dots^\circ \text{C} \approx 150^\circ \text{C} \end{align*} $]]
Jään lämpötilan muutos on [[$ 150 \text{ }^\circ \text{C} $]], joten mehujää tulisi syödä sen lämpötilan ollessa [[$ -150 \text{ }^\circ \text{C} $]].
461. Katulämmityksen teho lumisateella
Lumi lämpenee sulamispisteeseen ja sulaa. Lämmetessään lumi vastaanottaa lämmön
[[$ Q_l=cm\Delta T $]].
Lumen ominaislämpökapasiteetti on [[$ c=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]]. Tunnissa satavan lumen massa on [[$ m=0,45 \frac {\text{kg}}{\text{m}^2}\cdot 1500 \text{m}^2=675 \text{ kg} $]].
Lämpötilan muutos on [[$ \Delta T=5,0\text{ } ^\circ \text{C} $]].
Lumen sulaessa siirtyy siihen lämpö [[$ Q_s=sm $]], jossa veden ominaissulamislämpö on [[$ s=333 000 \text{ }\frac {\text{J}}{\text{kg}} $]].
Tunnin aikana vaadittava energia on näiden lämpöjen summa. Tehon määritelmän nojalla
[[$ P=\dfrac{Q_l+Q_s}{t}\\ P=\dfrac{cm\Delta T+sm}{t}=\dfrac{}{}= \dfrac{2090 \text{ }\frac {\text{J}}{\text{kg}\cdot \text{ }^\circ \text{C}}\cdot 675 \text{ kg}\cdot 5,0 \text{ } ^\circ \text{C}+333 000 \text{ }\frac {\text{J}}{\text{kg}}\cdot 675 \text{ kg}}{60 \cdot 60 \text{ s}} =64396,875 \text{ W}\approx 64\text{ kW} $]]
462. Jään ja kuuman veden sekoitus
Vesi jäähtyy nolla-asteiseksi ja luovuttaa lämmön [[$ Q_v=c_vm_v\Delta T_v $]]. Veden ominaislämpökapasiteetti on
[[$ c_v=4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja lämpötilan muutos [[$ \Delta T_v= 58\text{ }^\circ \text{C}$]].
Veden massa [[$ m_v $]] on tuntematon.
Jää lämpenee nolla-asteiseksi ja vastaanottaa lämmön [[$ Q_j=c_jm_j\Delta T_j $]]. Jään ominaislämpökapasiteetti on
[[$ c_j=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja lämpötilan muutos [[$ \Delta T_j= 19\text{ }^\circ \text{C}$]].
Jään massa on [[$ m_j=1,0 \text{ kg}$]].
Jään sulaessa siirtyy siihen lämpö [[$ Q_s=sm_j $]], jossa s on jään (veden) ominaissulamislämpö.
Systeemi on eristetty , joten veden luovuttama lämpö on yhtä suuri kuin jään vastaanottama kokonaislämpö.
[[$ \begin{align*} Q_v&=Q_j+Q_s\\ c_vm_v\Delta T_v&=c_jm_j\Delta T_j+sm_j\\ m_v&=\dfrac{c_jm_j\Delta T_j+sm_j}{c_v\Delta T_v}\\ m_v&=\dfrac{2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 1,0 \text{ kg}\cdot 19\text{ }^\circ \text{C} +333000 \frac {\text{J}}{\text{kg}}\cdot 1,0 \text{ kg}}{4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 58\text{ }^\circ \text{C} }\\ m_v&= 1,5336\dots \text{ kg}\approx 1,5\text{ kg} \end{align*} $]]
463. Jääpaloja lämpimään virvoitusjuomaan
Ratkaisu:
Lasketaan lämpö, joka vaaditaan kaiken jään sulattamiseen. Jää lämpenee sulamispisteeseen ja vastaanottaa lämmön
[[$ Q_j=c_jm_j\Delta T_j $]]. Jään ominaislämpökapasiteetti on [[$ c_j=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]] ja
lämpötilan muutos [[$ \Delta T_j= 18\text{ }^\circ \text{C}$]]. Jään massa on [[$ m_j=0,090 \text{ kg}$]]. Tämän lisäksi jään sulaminen
vaatii lämmön [[$ Q_s=sm_j $]], jossa s on jään (veden) ominaissulamislämpö.
[[$ \begin{align*} Q_j+Q_s&=c_jm_j\Delta T_j+sm_j\\ &=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,090 \text{ kg}\cdot 18\text{ }^\circ \text{C} +333000 \frac {\text{J}}{\text{kg}}\cdot 0,090 \text{ kg}\\ &=33355,8 \text{ J} \end{align*} $]]
Varmistetaan sulaako kaikki jää laskemalla juoman luovuttama lämpö sen jäähtyessä nolla-asteiseksi.
[[$ Q=c_vm_v\Delta T =4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,50 \text{ kg}\cdot 18\text{ }^\circ \text{C} =37710 \text{ J}$]]
Laskettu lämpö on suurempi kuin sulamisen vaatima, joten kaikki jää sulaa.
Määritetään systeemin loppulämpötila T. Vesi jäähtyy tähän lämpötilasta [[$ T_a=18\text{ }^\circ \text{C} $]], jolloin se luovuttaa lämmön [[$ Q_1=c_vm_v\Delta T =c_vm_v (T_a-T)$]]. Jää vastaanottaa aiemmin lasketun lämmön [[$ Q_j+Q_s $]]. Sulanut jää lämpenee (nyt vetenä) ja vastaanottaa edelleen lämmön [[$ Q_2=c_vm_j\Delta T_j =c_vm_v T$]].
Systeemi on eristetty, joten veden luovuttama lämpö on yhtä suuri kuin jään vastaanottama kokonaislämpö.
[[$ \begin{align*} Q_1&=Q_j+Q_s+Q_2\\ c_vm_v(T_a-T)&=Q_j+Q_s +c_vm_j T\\ c_v m_v T_a -c_v m_v T&=Q_j+Q_s +c_vm_j T\\ -c_v m_v T-c_vm_j T&=Q_j+Q_s -c_v m_v T_a\\ ( -c_v m_v-c_vm_j )T&=Q_j+Q_s -c_v m_v T_a\\ T&=\dfrac{Q_j+Q_s -c_v m_v T_a}{-c_v m_v-c_vm_j}\\ T&=\dfrac{33355,8 \text{ J}-4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,50 \text{ kg}\cdot 18\text{ }^\circ \text{C}}{-4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,50 \text{ kg} -4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0,090 \text{ kg}}\\ T&=1,7613 \dots \text{ }^\circ \text{C} \approx 1,8 \text{ }^\circ \text{C} \end{align*} $]]
464. Jääpaloja jäähtyneeseen termospulloon
Ratkaisu:
Termospullossa oleva vesi jäähtyy ja luovuttaa lämmön [[$ Q_v=c_v m_v\Delta T_v $]].
Veden ominaislämpökapasiteetti on [[$ c_v=4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]], massa [[$ m=0{,}50 \text{ kg} $]] ja lämpötilan muutos [[$ \Delta T_v=11\text{ } ^\circ \text{C} $]].
Termospullo jäähtyy myös ja luovuttaa lämmön [[$ Q_t=C\Delta T_v $]].
Termospullon lämpökapasiteetti on [[$ C=150 \text{ }\frac {\text{J}}{^\circ \text{C}} $]] ja lämpötilan muutos sama kuin veden [[$ \Delta T_v=11\text{ } ^\circ \text{C} $]].
Kaikki jää lämpenee sulamispisteeseen ja vastaanottaa lämmön [[$ Q_j=c_jm_j\Delta T_j $]].
Jään ominaislämpökapasiteetti on [[$ c_j=2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}} $]],
massa [[$ m=0{,}11 \text{ kg} $]] ja lämpötilan muutos [[$ \Delta T_j=15\text{ } ^\circ \text{C} $]].
Oletetaan, että jäätä sulaa massa [[$ m_s $]] ja systeemin loppulämpötila on [[$ 0\text{ } ^\circ \text{C} $]]. Jään sulaessa siirtyy siihen lämpö [[$ Q_s=sm_s $]], jossa veden ominaissulamislämpö [[$ s=333 000 \text{ }\frac {\text{J}}{\text{kg}} $]].
Systeemi oletetaan eristetyksi, joten sen osien vastaanottama kokonaislämpö on yhtä suuri kuin sen osien luovuttama lämpö. Kirjoitetaan yhtälö ja ratkaistaan sulavan jään massa.
[[$ \begin{align*} Q_j+Q_s&=Q_v+Q_t\\ c_jm_j\Delta T_j+sm_s&=c_v m_v\Delta T_v+C\Delta T_v \\ sm_s&=c_v m_v\Delta T_v+C\Delta T_v-c_jm_j\Delta T_j \\ m_s&=\dfrac{c_v m_v\Delta T_v+C\Delta T_v-c_jm_j\Delta T_j}{s}\\ m_s&=\dfrac{4190 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0{,}50 \text{ kg}\cdot 11\text{ } ^\circ \text{C} +150 \text{ }\frac {\text{J}}{^\circ \text{C}} \cdot 11\text{ } ^\circ \text{C}- 2090 \text{ }\frac {\text{J}}{\text{kg}\cdot^\circ \text{C}}\cdot 0{,}11 \text{ kg}\cdot 15\text{ } ^\circ \text{C} }{333 000 \text{ }\frac {\text{J}}{\text{kg}} }\\ m_s&= 0{,}063803\dots \text{ kg}\\ m_s&\approx 64\text{ g}\\ \end{align*} $]]
Koska kaikki jää ei sula, niin systeemin loppulämpötila on 0 °C.
465. Kastepiste
Alla olevassa kuvaajassa on esitetty suhteellisen ilmankosteuden riippuvuutta lämpötilasta. Vastaa kuvaajan perusteella seuraaviin kysymyksiin.
- Paljonko on suurin mahdollinen absoluuttinen ilmankosteus, kun lämpötila on 40 °C?
- Mikä on kastepiste, kun absoluuttinen ilmankosteus on 100 g/m3?
- Saunan lämpötila on 70 °C ja suhteellinen kosteus 60 %. Missä lämpötilassa höyryä alkaa tiivistyä nesteeksi, jos lämpötila laskee?
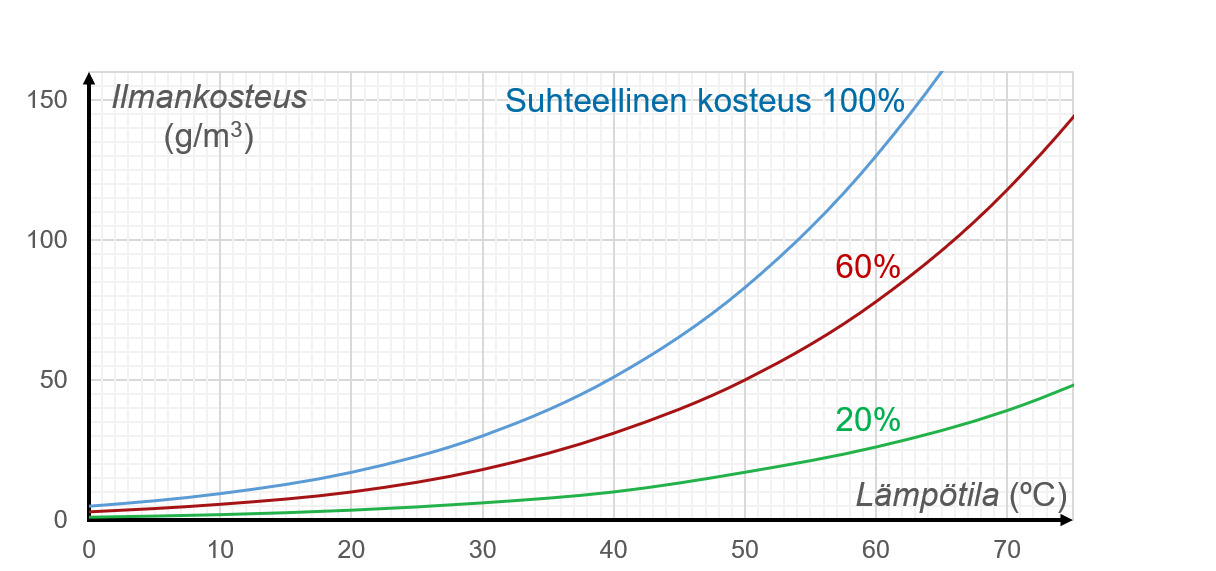
Ratkaisu:
b. Absoluuttinen ilmankosteuden ollessa 100 g/m3 voidaan käyrältä suhteellinen kosteus 100 %, että kastepiste on 54 °C.
c. Höyry alkaa tiivistyä nesteeksi noin lämpötilassa 58°C.
466. Saunomiseen liittyviä lämpöopin ilmiöitä
- Saunailman lämpötila on 75 astetta. Kiukaalle heitetään vettä, joka höyrystyy. Miksi vettä tiivistyy saunojan iholle? Miksi saunoja kokee kuumuutta löylyä heitettäessä?
- Vaikka lämpimästä suihkusta tulee lämpimiin sisätiloihin, tulee melko nopeasti kylmä, jos ei kuivaa ihoa. Mistä tämä johtuu?
- Masa tulee suihkusta, mutta pyyhe on hukassa. Missä olosuhteissa iho kuivuu nopeasti ja millaisessa tilanteessa hitaasti? Miksi?
Ratkaisu:
a. Saunojan ihon lämpötila on alhaisempi kuin vesihöyryn. Vesihöyry luovuttaa iholle lämpöä ja tiivistyy samalla. Ihon vastaanottama lämpö nostaa ihon lämpötilaa ja aiheuttaa lämmön aistimuksen.
b. Kostealta iholta höyrystyy vettä koko ajan ellei huoneilma ole kylläistä höyryä. Höyrystyminen vaatii lämpöä, joka siirtyy veteen ympäristöstä, erityisesti ihosta. Lämmön johtuminen pois ihosta aistitaan kylmyytenä.
c. Ihon kuivuu kun sen pinnalla oleva vesi höyrystyy. Höyrystymistä edesauttaa ympäristön korkea lämpötila, alhainen suhteellinen kosteus sekä ilmavirtaukset, joiden mukana höyryä kulkeutuu pois ihon läheisyydestä.
467. Virvoitusjuomatölkin rutistaminen lämpöopin keinoin
Virvoitusjuomatölkin suuaukko on avoin, ja sen pohjalla on hieman vettä. Miten selität videolla havaittavan tölkin rutistumisen kokoon?
Lämmitettäessä tölkkiä se täyttyy vesihöyrystä. Kun tölkki siirretään kylmään veteen, luovuttaa höyry vedelle energiaa ja tiivistyy. Nesteeksi tiivistyessä höyryn tilavuus pienenee huomattavasti, joten tölkkiin syntyy alipaine suhteessa ympäristöön. Paine-erosta aiheutuva voima puristaa tölkin kasaan. Tölkki on käännetty ylösalaisin, joten korvaavaa ilmaa ei pääse ympäristöstä tölkkiin.
Myös tölkin sisältämän ilman ja vesihöyryn lämpötilan aleneminen pienentää tölkin sisällä vaikuttavaa painetta, sillä vakiotilavuudessa tapahtuvassa tilanmuutoksessa kaasun paine ja lämpötila ovat suoraan verrannolliset.
468. Lämpöilmiöitä
Ilmiö 1. Suljetussa lääkeruiskussa on vettä. Lääkeruiskun mäntää vedetään poispäin, jolloin suljetun lääkeruiskun tilavuus kasvaa. Tilavuuden kasvaessa lääkeruiskun sisällä oleva paine pienenee. Paineen pienentyessä veden kiehumislämpötila alenee ja vesi lääkeruiskun sisällä alkaa kiehua.
Ilmiö 2. Vesi haihtuu lämpömittarista. Haihtuminen sitoo energiaa lämpömittarista, joka näkyy lämpömittarin viilenemisenä. Kaiken veden haihduttua lämpömittari alkaa lämmetä huoneenlämpöiseksi.
469. Höyrystymislämpö eri lämpötiloissa
Kun lämpötila ja paine ylittävät kriittisen pisteen, nesteen ja kaasun välillä ei ole selkeää rajaa. Tämä tarkoittaa, että tällä faasikaavion alueella tapahtuvassa olomuodon muutoksessa ei vapaudu eikä sitoudu energiaa.
Onko höyrystymislämpö sama eri lämpötiloissa ja paineissa? Jos ei, miten se muuttuu? Päättele tai ota selvää.
Ratkaisu:
Höyrystyminen tapahtuu lämpötilassa, joka riippuu paineesta. Esimerkiksi veden höyrystymislämpötila kasvaa paineen kasvaessa. Paineen kasvaessa myös ominaishöyrystymislämpö muuttuu. Se pienenee kunnes kriittisen pisteen paineessa saavuttaa nollan. Kriittistä pistettä korkeammassa paineessa ja lämpötilassa kaasun ja nesteen faasiraja häviää.