Elektrolyysi
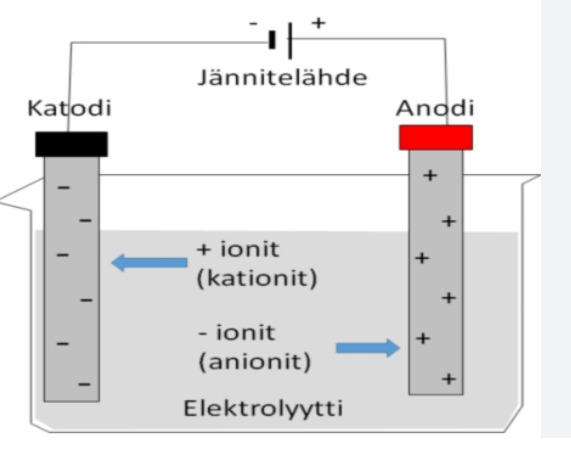
- Elektrolyysissä sähkövirran avulla saadaan aikaan pakotettu hapettumis-pelkistymisreaktio. Negatiivisella elektrodilla, katodilla tapahtuu pelkistyminen ja posit. elektrodilla, anodilla hapettuminen.
- Posit. ionit, kationit kulkevat katodille (saavat elektroneja) ja negat. ionit anionit anodilla (luovuttavat elektroneja).
- Elektrodit ovat metallia tai hiiltä. Passiviset elektrodit (hiili ja platina) eivät ota osaa reaktioon.
- Elektrolyyttiliuoksen tulee olla sähköä johtavaa.
- suolan vesiliuos tai sula suola
- Käyttökohteita
- tärkeä merkitys monien alkuaineiden, kuten natriumin, alumiinin ja kloorin valmistuksessa
- käytetään hyväksi raakakuparia puhdistettaessa
- käytetään metalliesineiden suojaukseen, galvanointiin päällystämällä ne paremmin kestävillä metalleilla
- Elektrolyyttien vesiliuoksessa on elektrolyyteistä syntyneiden ionien ja vesimolekyylien lisäksi aina myös oksonium-ioneita, H3O+ ja hydroksidi-ioneita, OH-. Liuoksessa olevat eri ionit ja vesimolekyylit "kilpailevat" reaktiojärjestyksestä elektrodeilla.
- Norm. potentiaalien arvojen avulla voidaan päätellä, missä järjestyksessä ja mitkä reaktiot elektrolyysissä tapahtuvat
- Esim tarkastellaan laimeaa NaCl:n vesiliuosta
- [[$Liuoksessa\ on\ vesimolekyylejä\ sekä\ Na^+{,}\ Cl^-{,}\ H_3O^+\ ja\ OH^-\ -ioneja$]]
- [[$Anodilla\ Cl^-\ ja\ H_2O\ kilpailevat\ hapettumisesta:$]]
[[$H_2O\left(aq\right)\xrightleftharpoons[]{}\ \frac{1}{2}O_2\left(g\right)+2H^+\left(aq\right)+2e^-\ \ {,}\ E_h=-1{,}23\ V $]]
[[$tai\ 2Cl^-\left(aq\right)\ \xrightleftharpoons[]{}\ Cl_2\left(g\right)+2e^-\ {,}\ E_h=-1{,}36\ V$]]
- Näistä ylempi tapahtuu, koska norm.potentiaali on pienempi (hapettuu helpommin)
- [[$Katodilla\ Na^{+\ }\ ja\ H_2O\ kilpailevat\ pelkistymisestä$]]
- [[$2H_2O\ \left(aq\right)+2e^-\ \xrightleftharpoons[]{}\ H_2\left(g\right)+2OH^-\left(aq\right)\ {,}\ E_p=-0{,}83\ V$]]
[[$tai\ \ Na^+\left(aq\right)+e^-\ \xrightleftharpoons[]{}\ Na\left(s\right)\ {,}\ E_p=-2{,}71\ V$]]
- Näistä ylempi tapahtuu, koska norm. potentiaali on suurempi (pelkistyy helpommin)
- Näistä tapahtuvat:
- [[$Katodilla:\ 2\ H_2O\ +2e^-\ \rightarrow\ H_2+2\ OH^-{,}\ E_p=-0{,}83\ V$]]
- [[$Anodilla:\ H_2O\ \rightarrow\ \frac{1}{2}O_2+2\ H^++2e^-\ {,}\ E_h=-1{,}23\ V$]]
- [[$Kok:\ 3\ H_2O\ \ \rightarrow\ H_2+\frac{1}{2}\ O_2+2\ H^++2\ OH^-\ eli$]]
[[$H_2O\ \rightarrow\ H_2+\ \frac{1}{2}\ O_2\ {,}\ E=-0{,}83\ V\ -1{,}23\ V=-2{,}06\ V$]]
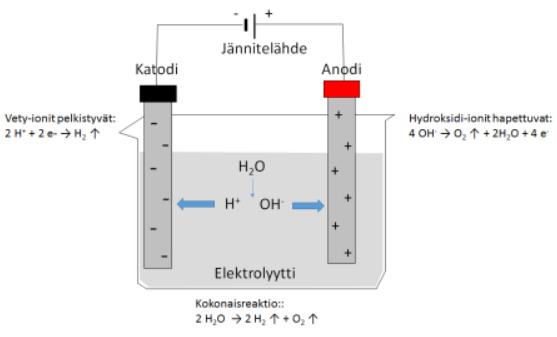
- Laimeissa elektrolyyttien vesiliuoksissa vesi hajoaa vedyksi ja hapeksi
- [[$2\ H_2O\ \left(aq\right)\ \rightarrow\ 2\ H_2\ \left(g\right)+O_2\ \left(g\right)$]]
- Jos anodimateriaalina käytetään esim kuparia ja se hapettuu helpommin kuin elektrolyyttiliuoksen ionit tai molekyylit, hapettuu anodimateriaali esim kupari ioneina liuokseen
- [[$Cu\left(s\right)\ \rightarrow\ Cu^{2+}\left(aq\right)+2e^-$]]
- Näin voidaan kuparoida anodimateriaali
Kotitehtävät: 130 ja 131
Elektrolyysissä liikkuva sähkömäärä
Faradayn elektrolyysilaista saadaan johdettua kaava, jossa Q on sähkömäärä
[[$\left(Q=\right)\ \ It=nzF$]], jossa
[[$I=elektrolyysissä\ käytetyn\ virran\ voimakkuus$]]
[[$t=elektrolyysiin\ käytetty\ aika$]]s
[[$n=erottuneen\ aineen\ ainemäärä\ \left(=\frac{m}{M}\right)$]]
[[$z=ionin\ varaus$]]
[[$F=Faradayn\ elektrolyysivakio\ =\ 96485\ \frac{As}{mol}$]]
Kaavaa käytetään, kun lasketaan
- elektrolyysissä purkautuvien aineiden määrää
- purkautumisessa tarvittavaa sähkömäärää (virta ja /tai aika)
Jos sama virta samassa ajassa niin
[[$Q=It\ on\ vakio\ \ \Rightarrow\ \ n_1z_1F=n_2z_2F\ \ \Leftrightarrow\ n_1z_1=n_2z_2\ \ \left(kahdessa\ tilanteessa\right)$]]
Lyijyakku
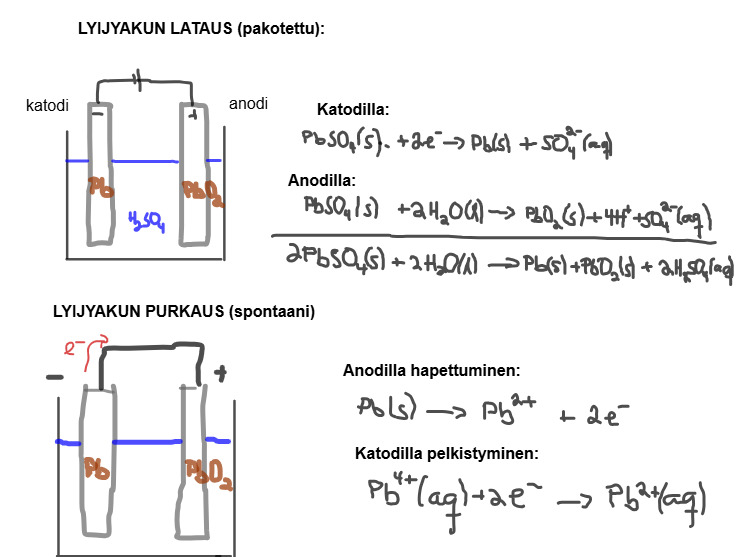
[[$Kokonaisreaktio:\ \ 2\ PbSO_4\left(s\right)+2\ H_2O\ \left(l\right)\ \ \xrightleftharpoons[purkaus]{lataus}\ Pb\left(s\right)+PbO_2\left(s\right)+2\ H_2SO_4\left(aq\right)$]]
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.