Stereoisomeria
Stereoisomerian lajit
Stereoisomeriassa eli geometrisessä isomeriassa yhdisteiden avaruudellinen rakenne on erilainen. Stereoisomeria jaetaan cis-trans-isomeriaan, optiseen isomeriaan ja konformaatioisomeriaan. Avaruusisomeereillä voi olla niin samanlaiset kemialliset ominaisuudet, että niiden erottaminen toisistaan perinteisin kemiallisin menetelmin voi olla vaikeaa. Isomeerien maku, haju tai teho lääkkeenä voi olla hyvin erilainen.
| Cis-trans-isomeria | 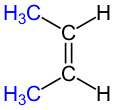 |
 |
|
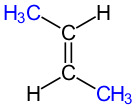
| Cis-2-buteeni | Trans-2-buteeni | ||
| Optinen isomeria eli peilikuvaisomeria | 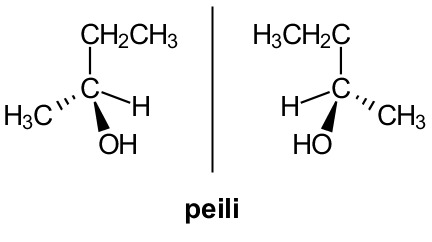 |
||
| Konformaatioisomeria | 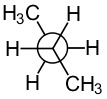 |
 |
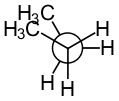 |
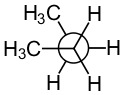
| anti | gauche | eclipsed | |
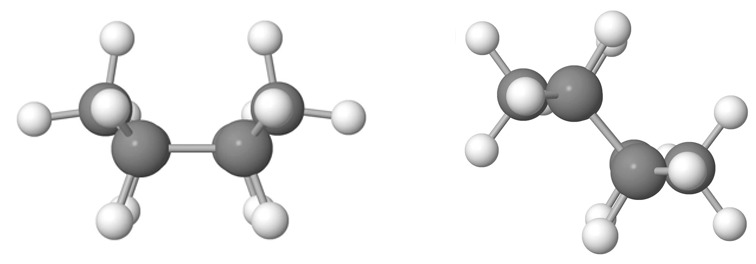
Cis-trans-isomeria edellyttää kaksoissidoksen tai renkaan
Cis-trans-isomerian edellytys on hiiliketjussa oleva kaksoissidos tai rengasrakenne. Kaksoissidoksellisen yhdisteen molekyylirakenne on tasomainen. Kaksoissidoksessa hiiliatomit ovat sp2-hybridisoituneet. Atomit liittyvät yhteen sigma- ja piisidoksilla. Piisidos jäykistää rakenteen, eivätkä hiiliatomeihin liittyneet ryhmät voi kiertyä sidosakselin ympäri samalla tavoin kuin ne yksikertaisessa sidoksessa voivat. Hiiliatomeihin liittyvien atomien ja ryhmien paikka tulee olennaiseksi tarkasteltavaksi tekijäksi. Tätä ilmiötä kutsutaan cis-trans-isomeriaksi.
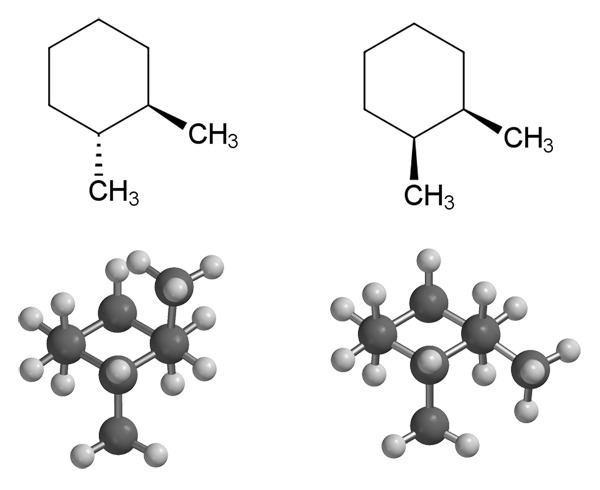
Avoketjuisen yhdisteen tapauksessa cis-muodoksi sanotaan isomeeriä, jossa tietyt kaksi ryhmää ovat samalla puolella kaksoissidoksen tasoa, kun taas trans-muodossa ne ovat eri puolilla. Rengasrakenteisten yhdisteiden cis- ja trans-isomeereissä tietyt kaksi ryhmää ovat renkaan muodostavan tason samalla (cis) tai eri puolella (trans).

Vasemmalla cis-2-buteeni | oikealla trans-2-buteeni.
Cis-trans-isomerian edellytyksenä on, että kaksoissidoksen hiiliatomeihin kiinnittyneet atomit tai atomiryhmät ovat keskenään erilaisia.
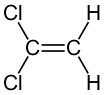 |
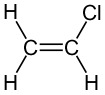 |
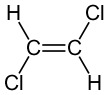 |
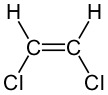 |
| Yhdiste ei ole cis-trans isomeeri |
Yhdiste ei ole cis-trans-isomeeri |
Yhdiste on cis-trans-isomeeri |
Yhdiste on cis-trans-isomeeri |
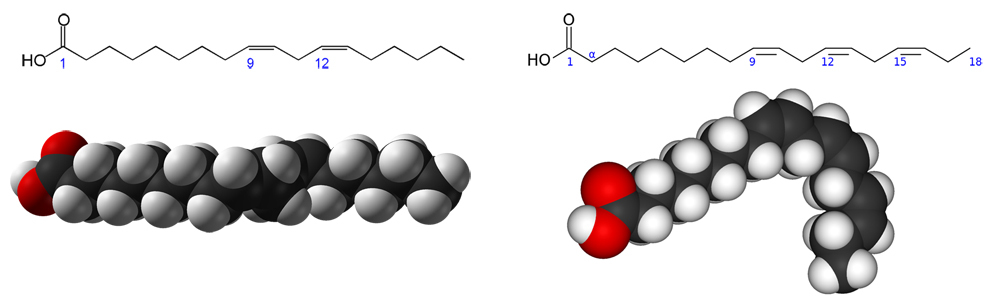
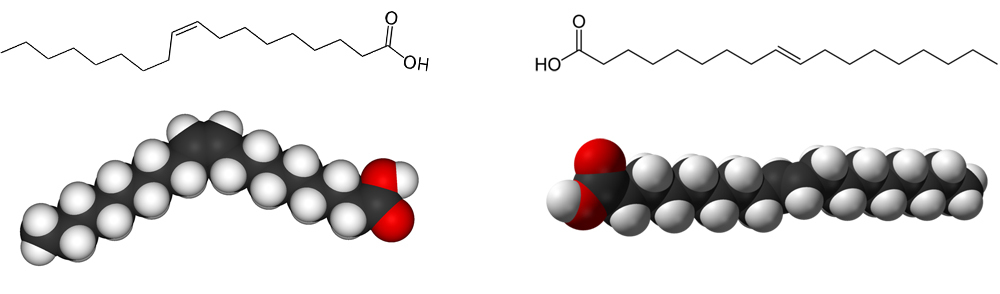
Cis-trans-isomeria vaikuttaa aineen fysiologisiin reaktioihin. Monityydyttymättömien rasvahappojen hydrauksessa syntyvät trans-rasvahapot ovat ihmiselimistölle haitallisempia kuin cis-rasvahapot. Nykyisin suositellaan kertatyydyttymättömien rasvahappojen käyttöä, koska niiden hydrauksessa syntyy tyydyttyneitä rasvahappoja. Esimerkiksi öljyhapon (cis) ja elaidiinihapon (trans) erottaa toisistaan 9-hiilen ja 10-hiilen välisen kaksoissidoksen isomeria. Elaidiinihapon ominaisuudet vastaavat tyydyttyneiden rasvahappojen ominaisuuksia.
Silmän sauvasolut ovat erikoistuneet toimimaan heikossa valossa. Niiden näköpurppurassa on rodopsiinia, joka koostuu proteiiniosasta ja siihen sitoutuneesta retinaalista. Retinaali on A-vitamiinin johdannainen. Siksi A-vitamiinin puute ilmenee ensimmäiseksi hämäräsokeutena. Kaikki näkyvän valon aallonpituudet aiheuttavat retinaalin muuttumisen trans-muodosta aktiiviseen cis-muotoon. Tästä seuraa, että rodopsiinin muoto muuttuu, jolloin reseptori aktivoituu ja syntyy näköaistimus.
Retinaalin isomeria
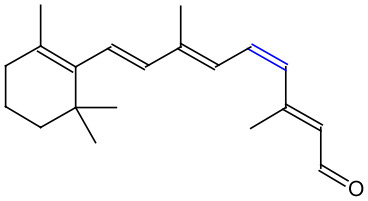
Cis-11-retinaali.
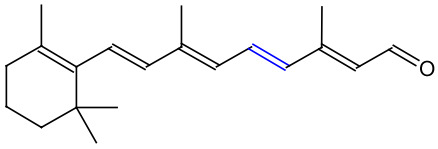
Trans-11-retinaali.
Optinen isomeria edellyttää kiraalisen hiiliatomin
Optisen isomerian nimitys perustuu siihen, että optisilla isomeereillä on kyky kääntää tasopolaroidun valon värähtelysuuntaa. Tasopolaroitunut valo värähtelee kulkusuuntaansa nähden vain yhdessä tasossa. Toinen isomeereistä kääntää polaroidun valon värähtelysuuntaa myötäpäivään ja toinen vastapäivään. Optista isomeriaa nimitetään myös peilikuvaisomariaksi.
Isomerian edellytyksenä on, että asymmetrinen hiiliatomiin eli hiiliatomiin on liittynyt neljä erilaista atomia, hiiliketjua tai toiminnallista ryhmää. Tällaista hiiltä nimitetään molekyylin kiraliakeskukseksi. Sen paikka merkitään rakennekaavaan tähdellä. Saman yhdisteen eri kiraaliset molekyylimuodotovat toistensa optisia isomeerejä. Yhteisnimitys niille on enantiomeerit. Yhdisteessä voi olla useita kiraliakeskuksia, jolloin optisia isomeerejäkin on useita.
Enantiomeerit erotetaan toisistaan sen perusteella, miten ne kiertävät tasopolaroidun valon värähtelysuuntaa. Jos kierto on myötäpäivään, enantiomeeri merkitään plus (+) muodoksi. Jos kierto on vastapäivään, enantiomeeri merkitään miinus (−) muodoksi. Plusmerkinnälle vaihtoehtoiset merkintätavat ovat d (dextrorotatory lat. myötäpäivään) ja R (rectus lat. oikea), miinusmerkinnälle l (levorotatory lat. vastapäivään) ja S (sinister lat. vasen).
Kun optisesti aktiivisia yhdisteitä valmistetaan laboratoriossa, tuloksena on seos, jossa kumpaakin isomeeriä on yhtä paljon. Tällainen seos on optisesti inaktiivinen eli tehoton, ja siitä käytetään nimitystä raseeminen seos. Nykytekniikalla seoksen optiset isomeerit pystytään erottamaan toisistaan.
Esimerkkejä enantiomeerien ominaisuuksista
Enantiomeerien fysikaaliset ominaisuudet, kuten kiehumispiste, sulamispiste ja liukoisuus, ovat samat, mutta niiden kemialliset ominaisuudet voivat poiketa toisistaan merkittävästi. Tällä on merkitystä esimerkiksi lääketeollisuudessa, sillä solujen reaktioihin osallistuvat optisesti aktiiviset aineet ovat pääsääntöisesti vain toista optista isomeeriä.
Talidomidi
Talidomidi oli 1950–60 luvuilla yleisesti käytetty raskausajan pahoinvointilääke. Talidonimolekyylin +-muoto oli tehokas unilääke, joka ei aiheuttanut riippuvuutta, auttoi raskauspahoinvointiin ja oli tehokas syöpälääke. Molekyylin muoto sen sijaan häiritsi sikiön käsien ja jalkojen pitkien luiden kasvua, aiheutti elinvaurioita ja vakavaa kehitysvammaisuutta. Lääkkeen käyttö johti lukuisiin vastasyntyneiden raajaepämuodostumiin ennen kuin sen vaikutusmekanismi tunnistettiin. Katastrofin syy oli se, että lääkettä valmistettiin raseemisena seoksena ja vain toinen avaruusmuodoista toimi elimistölle vaarattomana rauhoittavana aineena.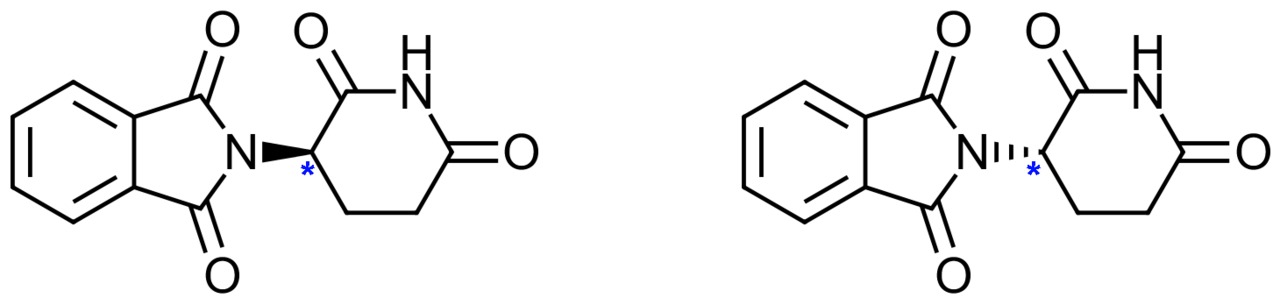
Vasemmalla (−)-talidomidi ja oikealla (+)-talidomidi.
Ibuprofeeni
Tulehduskipulääkkeenä käytetty ibuprofeeni valmistetaan raseemisena seoksena. Molempia muotoja on yhtä paljon, ja vain molekyylin +-muoto on kipua lievittävä aine. Osa vaikuttamattomasta aineesta muuttuu elimistössä vaikuttavaksi muodoksi, mutta muuttumaton osa varastoituu rasvakudoksiin.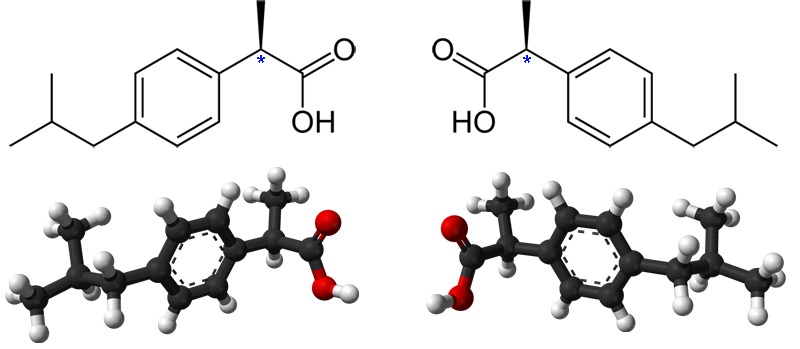
Vasemmalla (−)-ibuprofeeni, ei biologista aktiivisuutta | Oikealla (+)-ibuprofeeni, tulehduskipulääke.
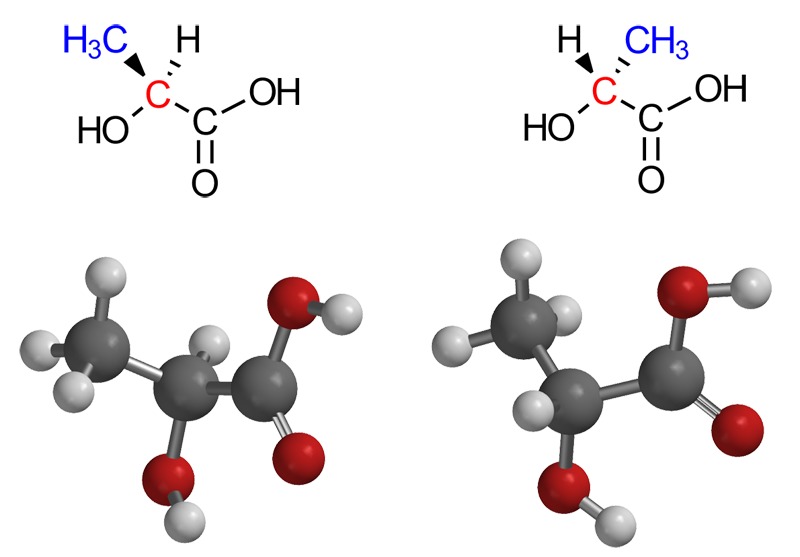
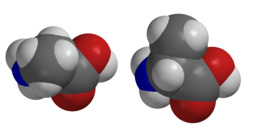
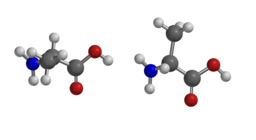
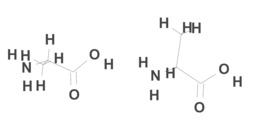
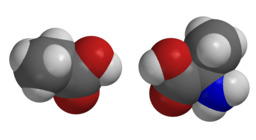
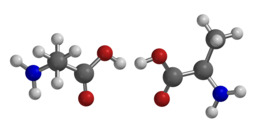
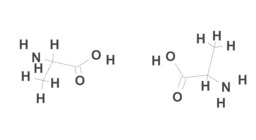
Maitohappo
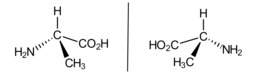
Maitohappo voi esiintyä kahtena peilikuvaisomeerinä. Luonnossa niitä voi tavata lihaksistossa (vasen molekyyli) ja hapatetuissa maitotuotteissa (oikea molekyyli).Alaniinin peilikuvaisomeria
Konformaatioisomeria
Tyydyttyneiden molekyylien muoto muuttuu, kun hiiliketjuun liittyneet ryhmät kiertyvät yksinkertaisen sidoksen akselin ympäri. Tästä isomerian lajista käytetään nimitystä konformaatioisomeria. Konformaatioisomeerejä on lukemattomia, ja ne muuttuvat jatkuvasti toisikseen. Konformaatioisomeereistä käytetään joissain yhteyksissä nimitystä konformeerit tai rotameerit. Konformaatioisomeria ei näy yhdisteen nimessä, eikä sitä yleensä huomioida isomeriatehtävissä.

Molekyylin konformaation muuttamiseen tarvitaan energiaa. Jotkut konformaatioisomeerit voivat olla muita pysyvämpiä muotoja. Esimerkiksi sykloheksaanin pysyvimmät konformaatiot ovat niin sanotut vene- ja tuolimuoto.