3.4 Hajoamislaki
Radioaktiivisuuden taustaa
Alkuaineiden isotoopeista alle 10 % on vakaita. Epävakaat isotoopit hajoavat jollain aiemmin esitellyistä radioaktiivisen hajoamisen tavoista. Yleensä jokainen isotooppi hajoaa vain tietyllä tavalla, mutta esimerkiksi hyvin raskaat isotoopit voivat hajota sekä alfahajoamisen että spontaanin fission kautta. Alla olevaan kaavioon on sijoitettu kaikki tunnetut isotoopit. Vaaka-akselilla on isotoopin järjestysluku Z, eli protonien lukumäärä ja pystyakselilla isotoopin neutronien lukumäärä. Eri värit kuvaavat isotooppien pysyvyyttä.
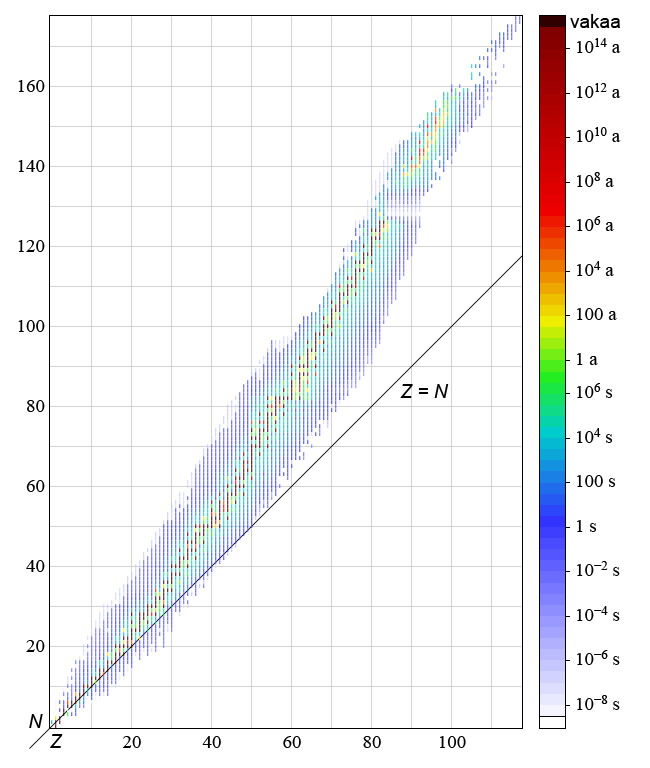
Kaaviossa pysyvät isotoopit on merkitty mustalla. Kevyimmissä isotoopeissa protoneja ja neutroneja on likimäärin yhtä paljon, eli suhde [[$\mathrm{\frac{N}{Z}}\approx 1$]]. Raskaammissa vakaissa atomiytimissä suhde [[$\mathrm{\frac{N}{Z}}$]] on suurempi kuin yksi. Vahvan vuorovaikutuksen on helpompi liittää yhteen neutroneja kuin protoneja, koska neutronien välillä ei esiinny sähköistä poistovoimaa. Radioaktiivinen hajoaminen tapahtuukin niin, että tytärytimen [[$\mathrm{\frac{N}{Z}}$]]-suhde on lähempänä optimaalista protonien ja neutronien suhdetta kuin emoytimessä.
Satunnaisuus on luonteenomaista radioaktiiviselle hajoamiselle. Tämä perustuu nukleonien aalto-hiukkasdualistisiin ominaisuuksiin. Edellisessä luvussa tutustuttiin kvanttimekaniikan periaatteisiin, joiden mukaan hiukkasilla ei ole tarkkaa paikkaa. Sen sijaan hiukkasten sijainnilla on todennäköisyysjakauma. Ytimen nukleonit ovat vahvan vuorovaikutuksen vaikutuksen alaisena, eikä niiden liike-energia riitä ytimestä karkaamiseen. Nukleonien sijainnin todennäköisyysjakauma voi ulottua kuitenkin ytimen ulkopuolelle, mikä mahdollistaa tunneloitumisen. Tunneloitumisen myötä hiukkanen pääsee ytimen ulkopuolelle, vaikka klassisen fysiikan mukaan se ei voisi sinne liikkua. Hyvin raskaiden ydinten tapauksessa hiukkaset erkanevat ytimistä heliumytimien muodostamina kokonaisuuksina, eli alfahiukkasina. Paettuaan vahvan vuorovaikutuksen voimakkaimman vaikutuksen alueelta alfahiukkasen ja ytimen välinen sähköinen hylkimisvoima sinkoaa ne suurella vauhdilla poispäin toisistaan. Alla oleva kuvaaja esittää alfahiukkasen energiaa ytimen välittömässä läheisyydessä. Osana ydintä se on potentiaalienergiakuopassa, ja sen energia on pienempi kuin poispäin siirtymisen edellyttämä liike-energia. Tunneloituminen mahdollistaa kuitenkin potentiaalienergiavallin ylittämisen, jolloin alfahiukkanen karkaa ytimestä.

Aktiivisuus
Kvanttifysiikan mukaan radioaktiivisuus on aidosti satunnainen ilmiö. Vastaavaan satunnaisuuteen on tutustuttu käsiteltäessä elektronin sijaintia tai atomin viritystilan purkautumista. Yksittäisen radioaktiivisen ytimen hajoamishetkeä ei voida edes teoriassa ennustaa. Sen sijaan ytimen hajoamisen todennäköisyys voidaan ennustaa. Hajoamisen todennäköisyyttä kuvaa hajoamisvakion suure [[$ \lambda $]].
Hajoamisvakio ilmaisee kuinka suuri osa radioaktiivisen näytteen ytimistä hajoaa aikayksikössä. Mitä suurempi se on, sitä epävakaampi isotooppi on kyseessä. Hajoamisvakion suuruus on tyypillisesti luku väliltä 0...1 ja yksikkö 1/s. Esimerkiksi fluori-20:n hajoamisvakio on 0,063 1/s. Mikäli näytteessä on 1 000 aktiivista fluoriydintä, hajoaa niitä sekunnin aikana noin 63 kappaletta (0,063[[$ \cdot $]]1 000). Hajoamisten määrä aikayksikköä kohden voidaan yleisesti laskea hajoamisvakion [[$ \lambda $]] ja hiukkasten lukumäärän [[$N$]] tulona: [[$ \lambda N $]]. Tämä tulo on aktiivisuus ([[$A$]]).
[[$ \qquad A= \lambda N $]]
Aktiivisuus ilmaisee näytteessä tapahtuvien hajoamisten lukumäärän aikayksikössä. Sen yksikkö on becquerel (Bq), jolle pätee 1 Bq = 1/s. Yksikkö on nimetty ranskalaisen fyysikon Henri Becquerelin (1852–1908) mukaan.
Ytimen hajotessa syntyy säteilyä, joka voidaan havaita säteilyilmaisimella. Mikään säteilymittari ei kuitenkaan havaitse kaikkia näytteessä tapahtuvia hajoamisia, sillä säteily leviää joka suuntaan ja absorboituu ympäröiviin aineisiin. Säteilymittari mittaakin suhteellista aktiivisuutta, joka on tietty prosentuaalinen osuus näytteen koko aktiivisuudesta.
Aktiivisuus
Aktiivisuus [[$A$]] ilmaisee aineessa tapahtuvien hajoamisten lukumäärän aikayksikköä kohden.
[[$ \qquad A =\lambda N $]]
[[$N$]] on ydinten lukumäärä ja [[$ \lambda $]] isotoopin hajoamisvakio.
Radioaktiivisen näytteen ydinten lukumäärää on käytännössä mahdotonta laskea. Makroskooppisella tasolla voidaan sen sijaan mitata näytteen massa. Massa [[$m$]] on suoraan verrannollinen ydinten lukumäärään [[$N$]].
[[$ \quad N=\dfrac{m}{m_{\text{atomi}}} $]]
Eri isotooppien atomimassat esitetään taulukoissa. Ne ilmoitetaan atomimassayksiköissä (u). Atomimassayksikkö on kilogrammoina 1,66053886 · 10-27 kg. Näiden tietojen avulla on laskettavissa tietyn massaisen tunnettua isotooppia olevan näytteen ydinten lukumäärä. Alla on laskettu, paljonko ytimiä on 10 mg:n näytteessä radioaktiivista jodi-131-isotooppia.
[[$ \quad N=\dfrac{m}{m_{\text{atomi}}}=\dfrac{10\cdot 10^{-6}\text{ kg}} {130{,}906124\cdot 1{,}66053886\cdot 10^{-27} {\text{ kg}}}\approx 4{,}0 \cdot 10^{19} $]]
Hajoamislaki
Radioaktiivinen ydin muuttuu hajotessaan toiseksi ytimeksi. Aktiivisten ydinten määrä siis vähenee ajan kuluessa. Radioaktiivisen näytteen aktiivisuus on määritelmänsä [[$ A=\lambda N $]] mukaan suoraan verrannollinen aktiivisten ydinten lukumäärään. Siksi myös aktiivisuus vähenee ydinten hajotessa. Alla olevalla videolla esitetään säteilymittaus näytteelle, jonka aktiivisuus pienenee minuuttien aikana merkittävästi alkuperäiseen aktiivisuuteen nähden. Säteilymittari havaitsee tietyn suhteellisen osuuden lähteen synnyttämästä säteilystä, eli mitattava suure on suhteellinen aktiivisuus (Bq) ajan suhteen.
Videolla säteilyn määrä vähenee lähelle nollaa kymmenessä minuutissa. Säteilyarvoissa on satunnaista vaihtelua, mutta valistuneena arvauksena aikariippuvuudelle voidaan esittää eksponentiaalinen malli. Tämä on myös teoriassa oikea malli, mikä voidaan osoittaa seuraavasti. Yhden becquerelin aktiivisuus tarkoittaa, että aktiivisten ydinten määrä vähenee yhdellä yhtä sekuntia kohden. Aktiivisuus ilmaisee yleisemmin ydinten määrän muutosnopeuden. Määrän väheneminen tarkoittaa negatiivista muutosta.
[[$ \qquad -A=\dfrac{\Delta N}{\Delta t} $]]
Ydinten määrä ajan funktiona merkitään [[$ N(t) $]]. Aktiivisuus on tällöin [[$ \lambda N(t) $]], ja muutosnopeus on ydinten lukumäärän derivaatta. Edellinen yhtälö voidaan siis muotoilla uudelleen.
[[$ \qquad N'(t)=-\lambda N(t)$]]
Yhtälö, jossa esiintyy funktio ja sen derivaatta, on niin sanottu differentiaaliyhtälö. Differentiaaliyhtälöitä ei käsitellä lukiomatematiikassa, mutta tämän yhtälön ratkaisu voidaan päätellä. Yhtälön toteuttavat funktiot, jotka ovat muotoa [[$ N(t) = ke^{-\lambda t} $]], jossa [[$k$]] on vakio. Tämä voidaan todeta yhdistetyn funktion ja eksponenttifunktion derivointisääntöjen perusteella.
[[$ \qquad D N(t) =D ke^{-\lambda t}=-k\lambda e^{-\lambda t}=-\lambda N(t) $]]
Funktion vakiotermin [[$k$]] merkitys voidaan päätellä laskemalla funktion arvo ajanhetkellä 0 s.
[[$ \qquad N(0 \text{ s})=ke^{-\lambda \cdot 0 \text{ s}}=k \cdot 1 =k $]]
Vakiotermi ilmaisee ydinten lukumäärän tarkastelun alkuhetkellä, jota merkitään [[$ N_0 $]]. Näin on perusteltu radioaktiivisten ydinten lukumäärää ajanhetkellä [[$t$]] ilmaiseva hajoamislaki.
[[$ \qquad N(t) =N_0 e^{-\lambda t} $]]
Myös näytteen aktiivisuus vähenee eksponentiaalisesti ajan suhteen. Tämä on selvää, sillä jokaisella ajanhetkellä aktiivisuus on hajoamisvakion ja ydinten lukumäärän tulo.
[[$ \qquad A(t) =A_0 e^{-\lambda t} $]]
Hajoamislaki
Radioaktiivisten ydinten lukumäärä [[$N$]] vähenee eksponentiaalisesti ajan [[$t$]] suhteen.
[[$ \qquad N(t) =N_0 e^{-\lambda t} $]]
[[$N_0$]] on ydinten lukumäärä alussa ja [[$ \lambda $]] isotoopin hajoamisvakio.
Myös näytteen aktiivisuus [[$A$]] vähenee eksponentiaalisesti.
[[$ \qquad A(t) =A_0 e^{-\lambda t} $]]
Puoliintumisaika
Radioaktiivisten isotooppien pysyvyyttä havainnollistaa puoliintumisajan suure [[$T_{1/2}$]]. Se on aika, jonka kuluessa 50 % isotoopin radioaktiivisista ytimistä on hajonnut. Jos ytimiä on paljon, kuten missä tahansa tavanomaisessa näytteessä, niiden määrä likimäärin puolittuu puoliintumisajan kuluessa. Samalla näytteen aktiivisuus laskee puoleen. Tämä on eksponentiaalisen mallin yleinen ominaisuus: tietyn ajan kuluessa prosentuaalinen muutos on aina yhtä suuri. Alla oleva kuvaaja esittää ydinten määrää ajan funktiona sekä puoliintumisajan ja ydinten lukumäärän välisen yhteyden.
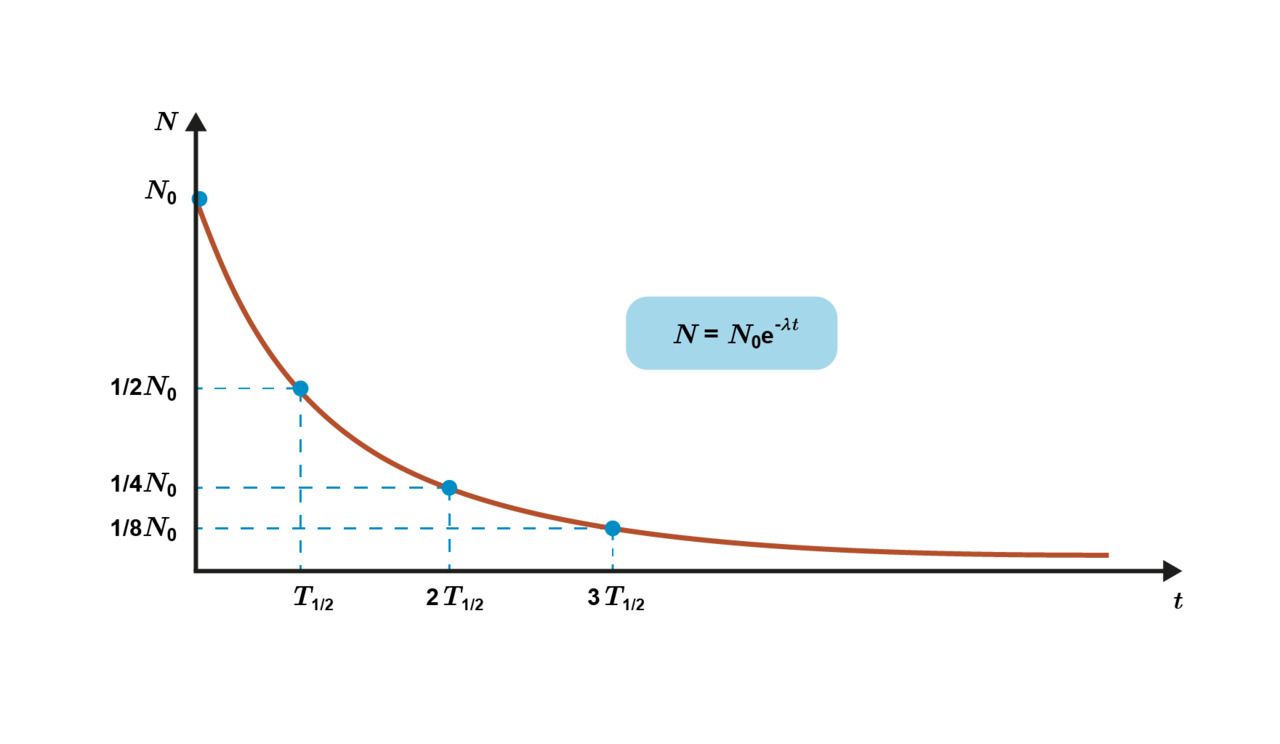
Puoliintumisajan yhteys isotoopin hajoamisvakioon voidaan ratkaista hajoamislain perusteella. Ratkaistaan hajoamislaista aika, jolloin ydinten määrä on puolet alkuperäisestä.
[[$ \qquad \begin {align*} A_0 e^{-\lambda T_{1/2}}&=\frac {1}{2} A_0 &\|& :A_0 \\ \, \\ e^{-\lambda T_{1/2}}&=\frac {1}{2} &|& \text{ otetaan logaritmi puolittain} \\ \, \\ -\lambda T_{1/2} &= \ln \frac {1}{2} &|& \text{ sovelletaan logaritmin laskusääntöjä} \\ \, \\ -\lambda T_{1/2} &= -\ln 2 \\ \, \\ T_{1/2} &= \frac {\ln 2}{\lambda} \\ \end {align*} $]]
Puoliintumisaika
Puoliintumisaika [[$T_{1/2}$]] on aika, jossa puolet radioaktiivisen aineen ytimistä hajoaa. Puoliintumisaika ja hajoamisvakio [[$ \lambda $]] riippuvat toisistaan.
[[$ \qquad T_{1/2} = \dfrac {\ln 2}{\lambda} $]]
Alla olevassa simulaatiossa voi havainnoida ydinten lukumäärän muutosta ajan suhteen.
Pysähdy pohtimaan
Esimerkkejä
Esimerkki 1
Kuinka suuri on aktiivisuus 1,0 milligrammassa radium-223-isotooppia? Kuinka suuri kokonaisenergia on vapautunut yhden radiumin puoliintumisajan kuluttua?
Esimerkki 2
Lääketieteellisen merkkiaineen aktiivisuus sen valmistuksen jälkeen on 45 MBq. Aktiivisuus on 34 MBq, kun aine tuodaan sairaalaan 16 tunnin kuluttua.- Määritä aineen puoliintumisaika.
- Aine on käyttökelpoista, kunnes sen kokonaisaktiivisuus laskee alle 5,0 MBq. Kuinka kauan tähän kuluu aikaa?