Lisätietoa
Elektroninsiirtäjät
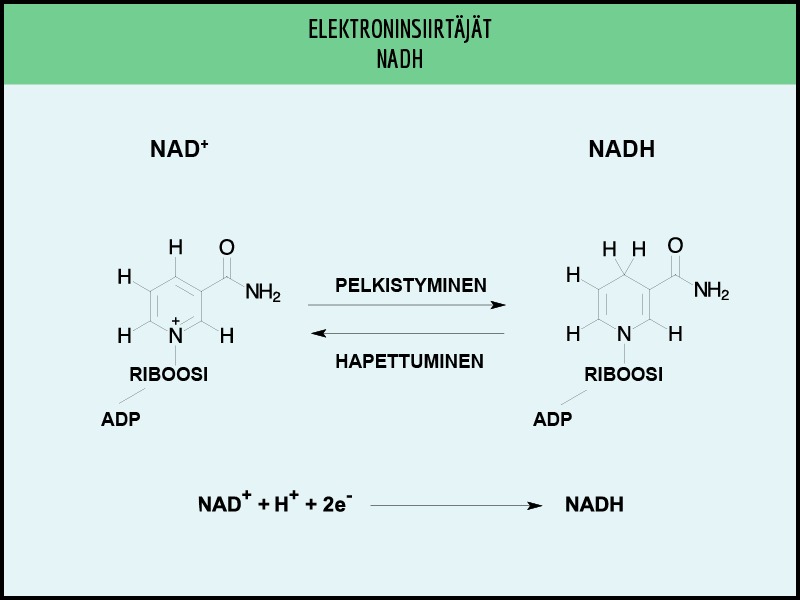
Solussa yleisenä elektronien vastaanottajana eli hapettimena toimii NAD+ (nikotiiniamidiadeniinidinukleotidi). Se ottaa vastaan hapetus-pelkistysreaktioissa vapautuvat elektronit sekä yhden vetyatomin ja siitä syntyy NADH:ta.
NADH voi luovuttaa elektroninsa eli toimia pelkistimenä useissa solun reaktioissa. Useimmiten se luovuttaa kuitenkin elektroninsa ja niiden mukana energiaa hengitysketjun elektroninsiirtäjille. Nämä elektroninsiirtäjät saavat aikaan ATP:n muodostumisen mitokondrion sisäkalvolla (luku 7).
Toisinaan NADH:n on liittynyt fosfaatti, jolloin sitä kutsutaan NADPH:ksi (nikotiiniamididinukleotidifosfaatti). NADPH toimii useissa solun reaktioissa pelkistimenä: se esimerkiksi kantaa fotosynteesissä vedeltä saatuja elektroneja ja toimii rasvahappojen muodostamisessa. Pääsääntönä voidaan pitää, että NADH luovuttaa elektroninsa hengitysketjun elektroninsiirtoketjulle, kun taas NADPH luovuttaa elektroninsa kemiallisten reaktioiden substraateille.
Lisätietoa entsyymeistä
Aktiivisessa kohdassa entsyymin kemialliset ryhmät muodostavat sopivia sidoksia substraattiin, mikä saa substraatin sitoutumaan aktiiviseen kohtaan. Kun substraatti sitoutuu aktiivisen kohtaan, entsyymin muoto muuttuu. Tämä saa aikaan muutoksen myös substraatissa, mikä helpottaa kemiallista reaktiota.
Osa entsyymeistä osallistuu kemialliseen reaktioon muodostamalla kovalenttisia sidoksia substraatin kanssa. Esimerkiksi mahalaukussa muita proteiineja hajottava pepsiini sitoutuu lyhytaikaisesti substraattiinsa eli toisiin proteiineihin. Näin se katkaisee proteiinista kahden aminohapon välisen peptidisidoksen. Kun entsyymi on suorittanut tehtävänsä, se irtoaa substraatista. Tämän jälkeen se on valmis katalysoimaan uutta reaktiota.
Entsyymi-inhibitiota on kahdentyyppisiä: palautuvaa ja ei-palautuvaa. Ei-palautuvassa inhibitiossa inhibiittori sitoutuu entsyymiin kovalenttisesti ja estää sen toiminnan. Entsyymi ei siis palaudu enää toimintakykyiseksi vaan se täytyy hajottaa. Monet lääkeaineet, kuten penisilliini ovat tällaisia inhibiittoreita.
Palautuvassa inhibitiossa inhibiittori sitoutuu entsyymiin heikoin sidoksin. Inhibiittori voi matkia substraattia ja sitoutua entsyymin aktiiviseen kohtaan. Tällaista inhibitiota kutsutaan kilpailevaksi eli kompetitiiviseksi inhibitioksi.
Inhibiittori voi sitoutua myös muuhun kohtaan entsyymiä: tällöin entsyymin muoto voi muuttua ja se ei enää kykene sitomaan substraattia aktiiviseen kohtaan. Tällaista estoa kutsutaan ei-kilpalevaksi estoksi. Jotkin inhibiittorit voivat olla sekä kilpailevia että ei-kilpailevia samanaikaisesti.
Lisätietoa ATP:sta
:rightUseimmiten ATP:n sisältämä energia ei vapaudu suoraan ympäristöön. Energia voi siirtyä esimerkiksi entsyymimolekyylille, joka käyttää sitä entsyymireaktion nopeuttamiseen. ATP voi siirtää fosfaattiryhmän fosfodiesterisidoksella myös jollekin toiselle molekyylille. Esimerkiksi fosfaattiryhmän siirtäminen entsyymille voi aktivoida sen toiminnan.
Toisinaan ATP:sta lohkeaa pois kaksi fosfaattiryhmää, jolloin siitä irtoaa AMP (adenosiinimonofosfaatti) ja kaksi fosfaattiryhmää sisältävä pyrofosfaatti. Pyrofosfaatti hajoaa solussa kahdeksi fosfaattiryhmäksi.
ATP:ta voidaan tuottaa soluhengityksen lisäksi myös joissain kemiallisissa reaktioissa, joissa vapautuu runsaasti energiaa. Esimerkiksi glykolyysissä eli glukoosin hajoamisessa anaerobisesti pyruvaatiksi entsyymit muodostavat ATP:ta ADP:stä ja fosfaatista. Näissä reaktioissa entsyymit käyttävät glukoosin kemiallisten sidosten hajoamisesta vapautuvaa energiaa. Tätä kutsutaan substraattitason fosforylaatioksi, sillä ATP:hen sitoutuva energia on peräisin entsyymireaktioiden substraateilta. Soluhengityksessä tapahtuvaa ATP:n muodostumista kutsutaan oksidatiiviseksi fosforylaatioksi, sillä reaktiosarjassa tarvitaan happea (eng. oxygen).