4.2 Radioaktiiviset hajoamisreaktiot
Radioaktiivisuuden havaitseminen
Kun aine absorboi sähkömagneettista säteilyä infrapunasäteilyn aallonpituusalueella, absorboitunut energia havaitaan kappaleen lämpötilan kasvuna. Rakenneosasten lämpöliike kasvaa, ja elektronit voivat virittyä korkeammille energiatiloille. Kun sähkömagneettisen sätelyn aallonpituutta lyhennetään, säteilyn energia kasvaa. Riittävän suurienerginen säteily kykenee irrottamaan elektroneja ytimistä, jolloin aineen atomeja alkaa muuttua ioneiksi. Näin suurienergistä säteilyä kutsutaan ionisoivaksi säteilyksi. Korkeaenergisen sähkömagneettisen säteilyn lisäksi myös hiukkassäteily voi olla ionisoivaa, jos hiukkasten liike-energia on riittävän suuri.
 Ionisoivan säteilyn havaitsemisessa yksinkertaisin laite on geigermittari (kaaviokuva oikealla). Geigermittarin putken sisällä on voimakas sähkökenttä, ja putki on täytetty matalapaineisella kaasulla. Mittari havaitsee säteilyn, jonka energia kykenee ionisoimaan putkessa olevia kaasumolekyylejä. Ionisaatiossa irronnut elektroni kulkee sähkökentän ohjaamana anodille ja aiheuttaa lyhyen virtapiikin. Se voidaan mitata, ja putkeen kytketystä kaiuttimesta kuullaan signaali. Geigermittarin toimintaperiaatteen keksi 1908 saksalainen Hans Geiger (1882-1945).
Ionisoivan säteilyn havaitsemisessa yksinkertaisin laite on geigermittari (kaaviokuva oikealla). Geigermittarin putken sisällä on voimakas sähkökenttä, ja putki on täytetty matalapaineisella kaasulla. Mittari havaitsee säteilyn, jonka energia kykenee ionisoimaan putkessa olevia kaasumolekyylejä. Ionisaatiossa irronnut elektroni kulkee sähkökentän ohjaamana anodille ja aiheuttaa lyhyen virtapiikin. Se voidaan mitata, ja putkeen kytketystä kaiuttimesta kuullaan signaali. Geigermittarin toimintaperiaatteen keksi 1908 saksalainen Hans Geiger (1882-1945).
Kaikista 3000 löydetystä isotoopista vain n. 250 on vakaita. Loput ovat epävakaita ja hajoavat itsestään ilman ulkoista vaikutusta. Tällöin vapautuu energiaa, ja jäljelle jää kevyempiä atomiytimiä. Tätä prosessia kutsutaan radioaktiiviseksi hajoamiseksi eli usein kansankielellä radioaktiivisuudeksi. Vapautuva energia havaitaan ionisoivana säteilynä, joka on hajoamistyypistä riippuen joko sähkömagneettista säteilyä, hiukkassäteilyä tai molempia.
Yllä olevalla videolla tarkkailtiin kolmen eri radioaktiivisen isotoopin lähettämää ionisoivaa säteilyä. Videolla pystytään erottelemaan kolme säteilylajia sen mukaan, miten ne läpäisivät ainetta ja vuorovaikuttivat magneettikentän kanssa. Nämä kolme keskeistä säteilylajia nimettiin 1900-luvun alussa alfa-, beeta- ja gammasäteilyksi. Myöhemmin säteilylajit tunnistettiin. Gammasäteily koostuu suurienergisistä fotoneista ja on sähkömagneettista säteilyä, jonka energia on suurempi kuin röntgensäteilyllä. Gammasäteily pysähtyy vasta hyvin paksuun kerrokseen tiheää ainetta. Beetasäteily on hiukkassäteilyä, joka koostuu elektroneista tai positroneista, eli elektronin antihiukkasista. Se pysähtyy helpommin ja sähkövarauksensa takia sen rata kääntyy magneettikentässä. Alfasäteily on hiukkasssäteilyä, jonka hiukkaset koostuvat kahdesta protonista ja kahdesta neutronista, eli ne ovat heliumatomin ytimiä. Niitä kutsutaan alfahiukkasiksi. Hiukkaset ovat niin raskaita, että ne pysähtyvät paksuun ilmakerrokseen tai paperiin.
Eri säteilylajit on nykyään helppo erottaa toisistaan sen mukaan, miten ne käyttäytyvät sähkö- ja magneettikentässä. Voit tutkia asiaa oheisessa simulaatiossa ja pohtia, miten kurssin 6 tietoja voisi soveltaa.
Yksi varhainen hiukkasilmaisin on sumukammio. Se on suljettu astia, jossa on täysin kylläistä vesihöyryä. Varauksellisen hiukkasen kulkeminen höyryn läpi aiheuttaa vesihöyryn tiivistymisen vesipisaraksi. Tiivistyminen voidaan havaita paljaalla silmällä. Oheisessa videossa kammioon päästetään radioaktiivista radonkaasua. Kaasu leviää kammioon, ja joka puolella nähdään radonydinten hajotessa vapautuvien alfahiukkasten jättämiä jälkiä. Alfahiukkaset ovat isoja ja pystyvät siksi kulkemaan sumukammiossa vain lyhyen matkan ennen pysähtymistään.
![]() Video: Radon-kaasua sumukammiossa (herberd)
Video: Radon-kaasua sumukammiossa (herberd)
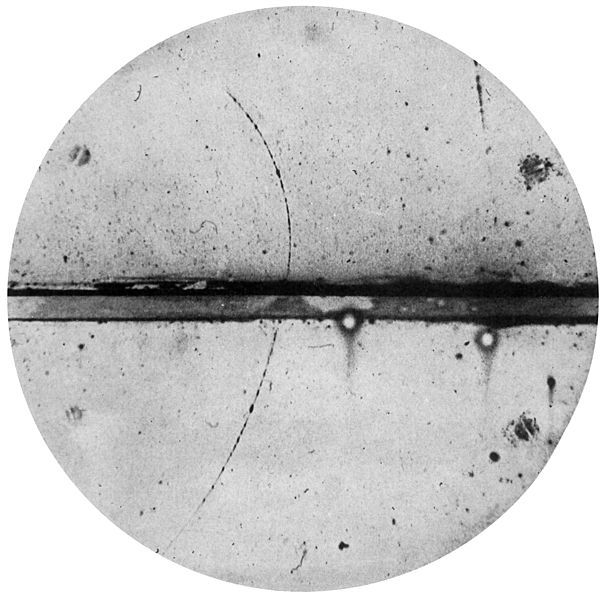
Betasäteily jättää kammioon pidempiä jälkiä, jotka kaartuvat voimakkaasti, mikäli kammio on magneettikentässä. Oheisessa kuvassa on ensimmäinen havainto positronista v. 1932. Rata kaartuu magneettikentässä yhtä paljon kuin elektronilla, mutta päinvastaiseen suuntaan. Kyseessä täytyi olla elektronin massainen, varaukseltaan vastakkainen hiukkanen.
Beetahajoaminen
Beetasäteilyllä tarkoitetaan elektroneja tai positroneja. Osa radioaktiivisista ytimistä lähettää beetasäteilyä hajotessaan. Tällaista hajoamista kutsutaan beetahajoamiseksi. Ytimestä vapautuu elektroni tai positroni. Samalla ytimessä neutroni muuttuu protoniksi, tai päinvastoin. Positroni ja elektroni ovat muuten samanlaisia, mutta positronilla on positiivinen varaus. Beetahajoaminen voidaan jakaa kahteen lajiin: beeta+ -hajoamiseen, jossa ytimestä vapautuu positroni, ja beeta- -hajoamiseen, jossa vapautuu elektroni. Huomaa, että beeta- -hajoamisessa vapautuva elektroni syntyy ytimessä neutronin muuttuessa protoniksi. Se ei ole peräisin atomin elektroniverhosta.
Beetasäteilyssä syntyvien elektronien ja positronien nopeuden havaittiin olevan niin pieni, että liikemäärän ja energian säilymisen perusteella prosessissa oletettiin syntyvän väistämättä myös jotakin muuta. Enrico Fermi (1901-1954) nimesi tämän oletetun erittäin kevyen ja varauksettoman hiukkasen neutriinoksi v. 1932. Neutriino havaittiin ensimmäisen kerran v. 1956.
Beetahajoaminen johtuu energeettisesti epäedullisesta neutronien ja protonien lukumäärien suhteesta ytimessä. Hajoamisen saa aikaan nukleonien sisältämien kvarkkien välinen heikko vuorovaikutus. Vuorovaikutuksessa säilyy kokonaisvaraus ja hiukkasten lukumäärä. Esimerkiksi protonin muuttuessa neutroniksi syntyy positroni, jotta positiivinen varaus säilyisi. Koska positroni on antihiukkanen, täytyy hiukkasten lukumäärän säilymiseksi vapautua myös jokin hiukkanen. Tämä hiukkanen on aiemmin mainittu neutriino. Heikkoon vuorovaikutukseen ja säilymislakeihin palataan tarkemmin luvussa 6.
Beeta- -hajoaminen tapahtuu ytimissä, joissa on paljon neutroneja suhteessa protoneihin. Esimerkki tällaisesta on vedyn isotooppi H-3. Se hajoaa heliumin isotoopiksi He-3, kun ytimessä neutroni muuttuu protoniksi. Hajoamisen reaktioyhtälö on
[[$ \quad ^{3}_{1}\text{H} \rightarrow {^{3}_{2}\text{He}}+{^{\ \ \ 0}_{-1}\text{e}}+\bar{\nu} $]]
Yhtälössä voidaan merkitä elektroni vaihtoehtoisesti vain e.
Ytimessä oleva neutroni hajoaa protoniksi, elektroniksi ja antineutriinoksi.
Kirjoitettaessa reaktioyhtälöitä vasempaan alanurkkaan merkitään hiukkasen varaus. Atomiytimillä tämä on sama kuin järjestysluku Z. Vasempaan ylänurkkaan merkitään hiukkasen nukleonien määrä. Atomiytimillä tämä on sama kuin massaluku A. Näin toimien oikein kirjoitetusta reaktioyhtälöstä näkyy varauksen sekä nukleonien lukumäärän säilyminen: nurkissa olevien lukujen summat ovat samat alku- ja lopputilanteessa.
Beeta+ -hajoaminen tapahtuu, jos ytimessä on vähän neutroneja suhteessa protoneihin. Esimerkiksi typen isotooppi N-13 on beeta+ -aktiivinen aine, joka hajoaa hiilen isotoopiksi C-13. Hajoamisen reaktioyhtälö on
[[$ \quad ^{13}_{\ \ 7}\text{N} \rightarrow {^{13}_{\ \ 6}\text{C}}+{^{\ \ \ 0}_{+1}\text{e}}+\nu $]]
Ytimessä protoni hajoaa neutroniksi, positroniksi ja neutriinoksi.
Beetahajoaminen
Beeta- säteilyn reaktioyhtälö on yleisesti
[[$ \quad ^A_Z\text{X} \rightarrow {^{\ \ \ \ \ A}_{Z+1}\text{Y}}+{^{\ \ \ 0}_{-1}\text{e}}+\bar{\nu} $]]
Beeta+ -säteilyn reaktioyhtälö on yleisesti
[[$ \quad ^A_Z\text{X} \rightarrow {^{\ \ \ \ \ A}_{Z-1}\text{Y}}+{^{\ \ \ 0}_{+1}\text{e}}+\nu $]]
Alfahajoaminen
Isoimmat atomiytimet ovat epästabiileja, koska vahva vuorovaikutus ei kykene täysin kumoamaan ytimen protonien välisiä sähköisiä poistovoimia. Nämä ytimet hajoavat vapauttamalla alfasäteilyä eli heliumytimiä, jotka koostuvat kahdesta protonista ja kahdesta neutronista. Tätä kutsutaan alfahajoamiseksi.
Koska alfasäteilyn hiukkaset ovat suuria, ne voivat aiheuttaa suurta vahinkoa. Kokonsa takia pelkkä ilmakerros tai ihmisen iho pysäyttää ne kuitenkin helposti. Ruoan tai hengitysilman välityksellä kehoon sisään pääsevä alfa-aktiivinen aine on sen sijaan erittäin vaarallista. Esimerkiksi alfa-aktiiviset radonytimet kulkeutuvat hengittäessä keuhkoihin, mikä nostaa keuhkosyöpäriskiä. Hengitysilman radon on suurin säteilyaltistusriski suomalaisille.
Esimerkki alfa-aktiivisesta aineesta on uraanin isotooppi U-238. Se hajoaa spontaanisti toriumin isotoopiksi Th-234. Hajoaminen näkyy videolla alla. Sen reaktioyhtälö on
[[$ \quad ^{238}_{\ \ 92}\text{U} \rightarrow {^{234}_{\ \ 90}\text{Th}}+{^4_2\text{He}} $]]
Alfahajoaminen
Alfa-aktiivisen aineen hajoamisen reaktioyhtälö on yleisesti
[[$ \quad ^A_Z\text{X} \rightarrow {^{A-4}_{Z-2}\text{Y}}+{^4_2\text{He}} $]]
X-ydintä kutsutaan emoytimeksi ja Y-ydintä tytärytimeksi.
Muut hajoamisreaktiot
Elektronisieppaus
Elektronisieppaus on läheistä sukua beeta+ -hajoamiselle. Kummassakin heikko vuorovaikutus muuttaa protonin neutroniksi. Elektronisieppauksessa ei kuitenkaan emittoidu positronia, vaan vuorovaikutukseen osallistuu sisimmältä elektronikuorelta yksi elektroni, joka häviää. Yleensä elektronisieppaus esiintyy, kun ytimen neutroni-protoni -suhde on liian pieni, mutta energiaa liian vähän positronin lähettämiseen ytimestä.
Esimerkiksi berylliumin isotooppi Be-7 hajoaa elektronisieppauksen kautta litiumin isotoopiksi Li-7:
[[$ \quad ^7_4\text{Be} +{^{\ \ \ 0}_{-1}\text{e}} \rightarrow {^7_3\text{Li}}+\nu $]]
Ytimessä protoni ja elektroni yhdistyvät neutroniksi, ja samalla vapautuu neutriino.
Elektronisieppauksen reaktioyhtälö yleisellä tasolla on
[[$ \quad ^A_Z \text{X}+{^{\ \ \ 0}_{-1}\text{e}}\rightarrow {^{\ \ \ \ \ A}_{Z-1}\text{Y}}+\nu $]]
Spontaani fissio
Jotkin raskaimmista atomiytimistä hajoavat alfahajoamisen sijaan kahdeksi kevyemmäksi ytimeksi ja mahdollisesti nopeiksi neutroneiksi. Syntyvien ydinten kokoa tai neutronien määrää on vaikea ennustaa laskennallisesti. Kunkin spontaanilla fissiolla hajoavan isotoopin hajoamisreaktio tulee selvittää tapauskohtaisesti lähdekirjallisuudesta.
Esimerkiksi uraanin U-238 isotooppi voi hajota joskus alfahajoamisen sijaan myös spontaanin fission kautta:
[[$ \quad ^{238}_{\ \ 92}\text{U}\rightarrow {^{145}_{\ \ 56}\text{Ba}}+{^{90}_{36}\text{Kr}}+3\cdot {^1_0\text{n}} $]]
Hajoamisreaktiossa syntyy barium-90 isotooppi, krypton-36 isotooppi sekä kolme vapaata neutronia.
Neutronisäteilyn ja gammasäteilyn synty hajoamisreaktioissa
Neutronisäteily
Neutronisäteily koostuu vapaista neutroneista, joita syntyy esim. aineen hajotessa spontaanin fission kautta. Sen lisäksi vapaita neutroneja voi syntyä fuusioreaktioissa, jos fuusioituvissa ytimissä on yhteensä ollut enemmän neutroneja kuin on tarpeellista syntyvän uuden ytimen kannalta. Vapaat neutronit hajoavat heikon vuorovaikutuksen seurauksena protoniksi, elektroniksi ja antineutriinoksi.
Gammasäteily
Luvussa 3 esiteltiin elektronin viritystilan purkautuminen. Atomin elektronin siirtyessä korkeammalta energiatilalta matalampaan emittoituu fotoni, jonka energia on sama kuin näiden energiatilojen erotus. Tämän fotonin energia on tyypillisesti muutamia elektronivoltteja.
Myös atomin ydin voi olla virittynyt. Usein alfa- tai beetahajoamisessa syntyneen aineen tytärydin jää viritystilaan, jolloin viritystilan purkautuessa havaitaan fotoni. Ytimen viritystilojen energiat ovat huomattavasti elektronien viritystilojen energioita suurempia. Siksi ytimen viritystilan purkautuessa vapautuvan fotonin energia on huomattavan suuri, miljoonia elektronivoltteja. Tällaisen fotonin aallonpituus vastaa gammasäteilyn aallonpituutta. Gammasäteily on kaikista suurienergisintä sähkömagneettista säteilyä.
Esimerkiksi koboltin isotooppi Co-60 on beeta- -aktiivinen aine, jonka hajoamisessa syntynyt nikkeliydin jää virittyneeseen tilaan. Viritystila purkautuu välitilan kautta. Purkautumisessa havaitaan kaksi sähkömagneettisen säteilyn fotonia gammasäteilyn aallonpituusalueella, joiden energiat ovat n. 1,17 MeV ja 1,33 MeV. 0,12 %:n todennäköisyydellä beetahajoamisessa vapautuu niin energinen elektroni, että syntynyt nikkeliydin on jo välitilassa. Tällöin viritystilan purkautuessa havaitaan vain yksi fotoni. Prosessi on esitetty alla kaaviona.
Esimerkkejä
Esimerkki 1
Eräissä palovaroittimissa on sisällä Amerikium-241 alfasäteilylähde. Säteilylähteen lähellä on pieni ilmarako, jossa oleva ilma ionisoituu säteilyn seurauksena ja muuttuu sähköä johtavaksi. Tulipalon sattuessa savu kulkeutuu katonrajaan ja palovaroittimen ilmarakoon. Savun sisältämät pienhiukkaset sitovat osan ilman ioneista, jolloin säteilylähteen ilmaraossa kulkeva heikko sähkövirta häiriintyy. Kirjoita Amerikium-241 isotoopin hajoamisyhtälö.




