8. Palaminen ja paloturvallisuus
1. Virittäytyminen – edellyttääkö palaminen aina liekkiä?
2. Happi aiheuttaa ruostumista
Kokemuksen perusteella tiedetään ruostumisilmiön hidastuvan, kun polkupyörän metalliosat pidetään puhtaina ja kuivina sekä ratas- ja laakeriosat öljyttyinä. Vaikuttaa siltä, että vesi edistää ruostumista, kun taas öljy ehkäisee sitä. Olennaista on estää ilmassa ja vedessä olevan hapen reaktio metallin kanssa. Rattaissa metallin päällä oleva öljykerros toimii juuri näin.

Ruostuminen on yksi palamisilmiön monista ilmenemismuodoista. Vastakuoritun omenan tai banaanin hedelmäliha tummuu, jos se jätetään suojaamattomana pöydälle. Ilmiö johtuu hapen reaktiosta hedelmälihan kanssa. Hedelmälihan tummumista voidaan estää antioksidanteilla eli yhdisteillä, jotka estävät palamisreaktioita. Esimerkiksi sitrushedelmissä oleva C-vitamiini toimii antioksidanttina.

Ihminen on oppinut myös hyödyntämään palamista. Puun, öljyn ja maakaasun palaminen ovat kemiallisia reaktioita, jotka tuottavat runsaasti energiaa valona ja lämpönä. Valo ja lämpö tuovat turvaa, parantavat elinolosuhteita, tuovat viihtyvyyttä ja edistävät terveyttä. Tulen avulla voidaan kuumentaa vettä, jolloin taudinaiheuttajat kuolevat ja ihminen säästyy monilta infektioilta.

3. Palamisen edellytykset
Palamisen edellytykset ovat palava aine, happi ja riittävän korkea lämpötila. Palamisreaktio voidaan estää ja tulipalo tukahduttaa, jos yksi tai useampi näistä tekijöistä voidaan estää.
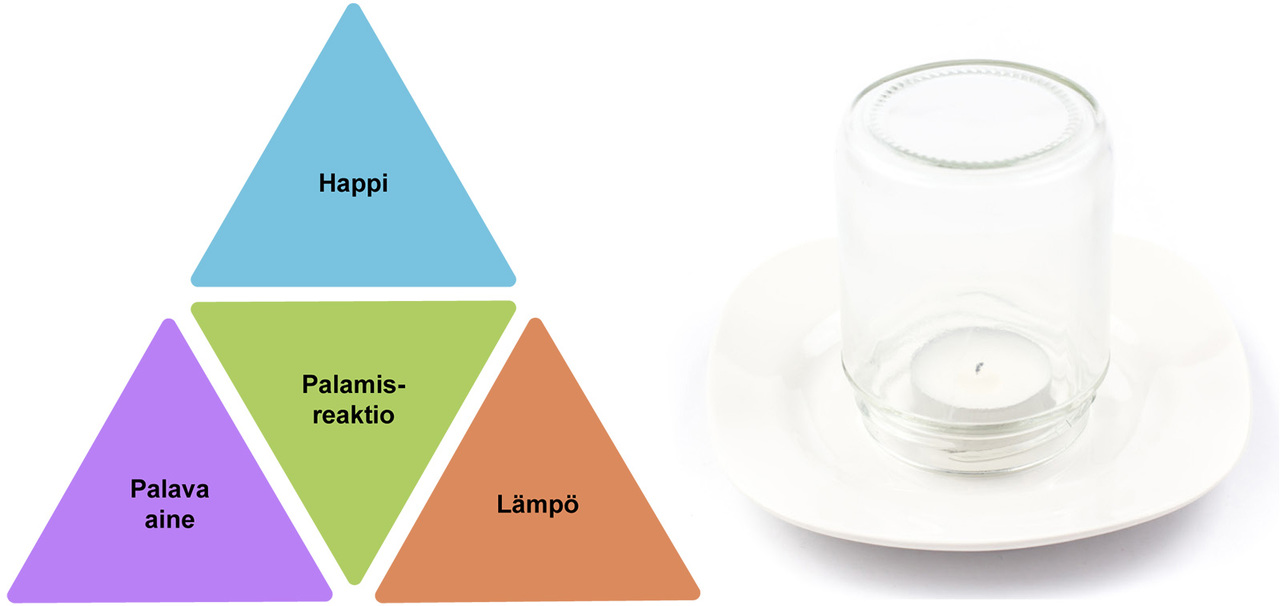
Aine voi palaa myös vedessä
![]() Magnesiumin ja veden reaktiossa palaminen perustuu aineen ja hapen reaktioon. Magnesiumin (Mg) ja vesimolekyylin hapen välinen vuorovaikutus on suurempi kuin vedyn ja hapen välinen vuorovaikutus vesimolekyylissä. Tämän vuoksi vesimolekyyli hajoaa ja magnesium reagoi hapen kanssa.
Magnesiumin ja veden reaktiossa palaminen perustuu aineen ja hapen reaktioon. Magnesiumin (Mg) ja vesimolekyylin hapen välinen vuorovaikutus on suurempi kuin vedyn ja hapen välinen vuorovaikutus vesimolekyylissä. Tämän vuoksi vesimolekyyli hajoaa ja magnesium reagoi hapen kanssa.
![]() Magnesiumia vedessä
Magnesiumia vedessä
4. Palamisesta muodostuu oksideja
Vedyn palaessa eli vedyn ja hapen reagoidessa keskenään reaktiotuotteena muodostuu vettä. Happeen perustuvien palamisreaktioiden reaktiotuotetta nimitetään yleisesti oksidiksi. Vesikin on vedyn oksidi. Sitä voisi siis kutsua divetyoksidiksi, koska siinä on kaksi vetyatomia ja yksi happiatomi.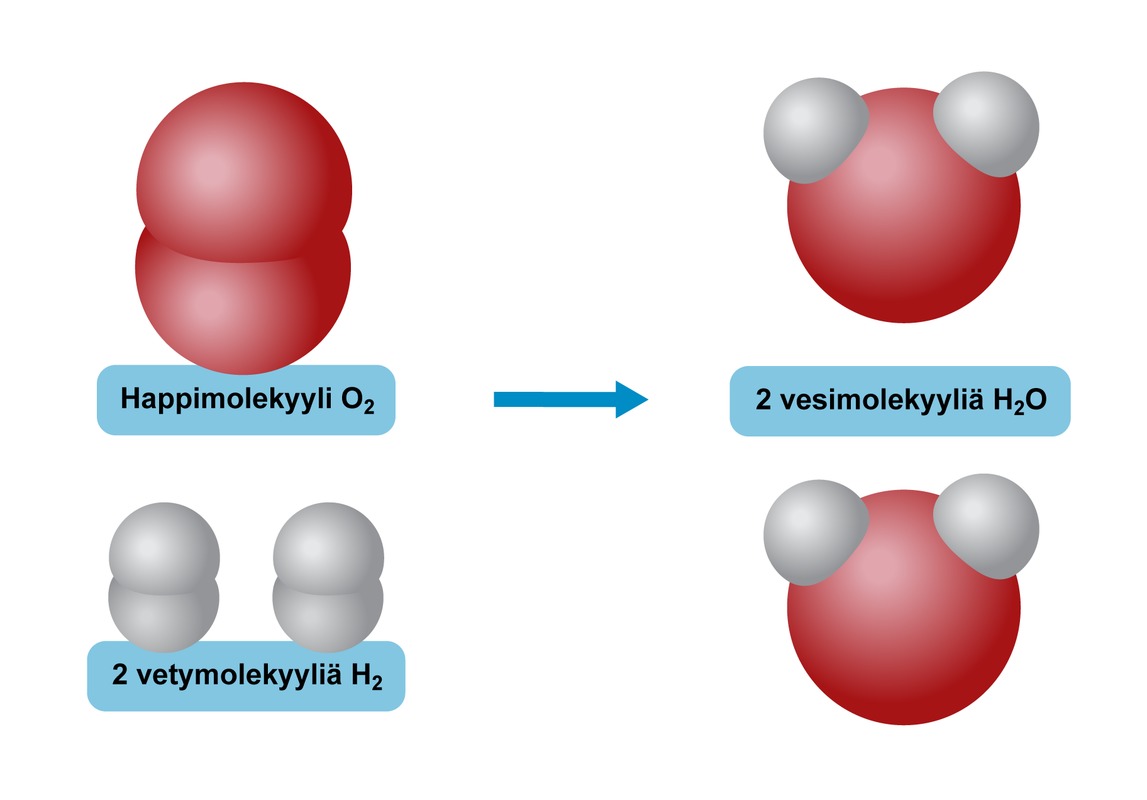

Ruostuminen taas on raudan palamista. Reaktiossa muodostuu raudan oksideja. Ruskeanvärisen ruosteen yleinen kaava on Fe3O4.
 Lähikuva ruosteesta.
Lähikuva ruosteesta.5. Polttoaineiden palamisessa vapautuu runsaasti energiaa
Palamisreaktioissa vapautuu energiaa, jota ihminen hyödyntää energialähteenä lämmön ja sähkön tuotannossa. Tähän tarkoitukseen käytettyjä aineita kutsutaan polttoaineiksi. Polttoaineet sisältävät yleensä hiiltä ja vetyä. Pelkkää hiiltä poltettaessa reaktiossa muodostuu vain hiilidioksidia. Jos polttoaine sisältää sekä hiiltä että vetyä, palamistuotteina syntyy hiilidioksidia ja vettä. Molemmat ovat kasvihuonekaasuja.
Vanhimpia polttoaineita ovat puu ja hiili. Niitä on käytetty jo esihistoriallisilta ajoilta lähtien. Puun palamista on hyödynnetty lämmöntuotantoon ja ruoanvalmistukseen. Hiiltä on käytetty metallien valmistamisessa. Myöhemmin kivihiili on korvannut puun ja hiilen energiantuotannossa. Kaikkien näiden poltossa muodostuu suuria määriä kasvihuonekaasuja, erityisesti hiilidioksidia ja vesihöyryä.

Palaminen elimistössä
Ihmisen elimistö saa tarvitsemansa energian pääasiassa ruoka-aineissa olevan sokerin (C6H12O6) palamisesta: C6H12O6 + 6 O2 → 6 CO2 + 6 H2O. Myös rasvojen ja alkoholin palamisesta saadaan energiaa. Sokerien palamisesta energiaa saadaan nopeimmin.

Polttoaineet
Fossiilisilla polttoaineilla tarkoitetaan aineita, jotka ovat muodostuneet esihistoriallisena aikana eliöstön fossilisoituessa. Näin on muodostuneet muun muassa kivihiili, maakaasu, turve ja öljy. 1900-luvun energiantuotanto on perustunut monelta osin öljyyn ja kaasuun. Öljystä voidaan valmistaa dieseliä ja bensaa liikenteen tarpeisiin. Maakaasua käytetään kaukolämpöjärjestelmän polttoaineena. Fossiiliset polttoaineet eivät uusiudu. Vaihtoehtona näille ovat uusiutuvat polttoaineet, kuten aurinkoenergia, bioenergia, tuuli ja vesivoima.
 Uusiutuvaa energiaa saadaan esim. aurinko, tuuli- ja vesivoimasta.
Uusiutuvaa energiaa saadaan esim. aurinko, tuuli- ja vesivoimasta.
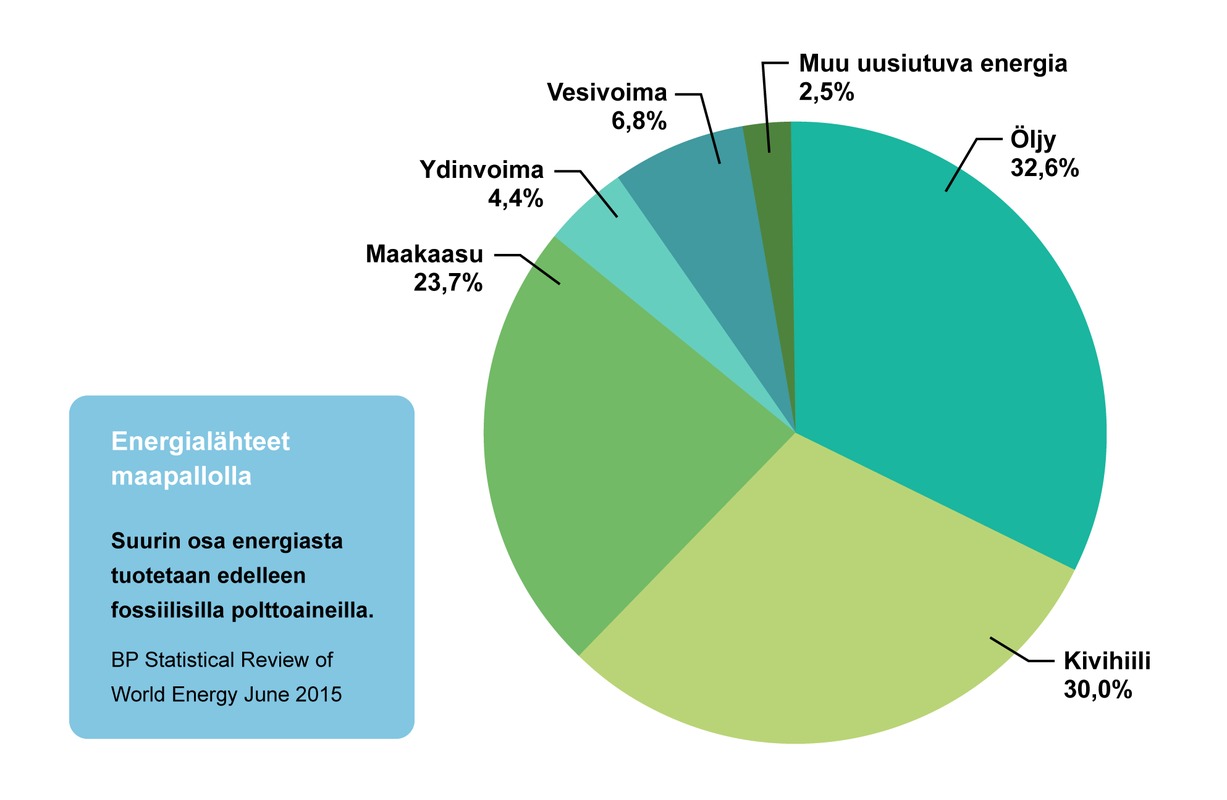
Uusiutuvat energianlähteet ovat tulevaisuuden energianlähde, mutta toistaiseksi vielä pieni. Tästä linkistä voit analysoida, miten paljon maailmassa valmistetaan fossiilisia polttoaineita.
6. Pohdintaa polttoaineista
Määrällisesti suurimman osan luonnosta saatavia hiilivetyjä ihminen käyttää polttoaineena. Näitä kutsutaan niiden muodostumistavan perusteella fossiilisiksi polttoaineiksi. Koska näiden hiilivetyjen muodostuminen luonnossa vaatii ihmisiän mittakaavassa pitkiä aikoja, maakaasua ja maaöljyä kutsutaan myös uusiutumattomiksi polttoaineiksi.
Raakaöljyn pumppaamiseen maaperästä tai merenpohjasta liittyy suuria riskejä - samoin sen siirtämiseen öljynjalostamoille, joissa siitä erotetaan eri hiilivedyt käyttötarkoituksen mukaan. Öljyonnettomuuksiin on sekä merillä että sisävesillä varauduttu melko hyvin erilaisella öljyntorjuntakalustolla, mutta vahinkoja ei voida kokonaan estää. Pienetkin öljyvuodot aiheuttavat vakavia vaurioita niin vesilinnustolle, kaloille kuin muullekin vesi- ja rantaeliöstölle. Vahingoista toipumiseen saattaa kulua kymmeniä vuosia.

Kun hiilivetyjä käytetään polttoaineina, palamistuotteita ovat vesi ja hiilidioksidi. Palaessa vapautuu samalla suuret määrät energiaa. Koska fossiilisten polttoaineiden polttaminen on helppo tapa tuottaa paljon energiaa, ne ovatkin suurin energianlähde nyky-yhteiskunnassa. Poltetut määrät ovat valtavia, minkä seurauksena ilmakehään vapautuvat hiilidioksidimäärät alkavat vaikuttaa sen toimintaan.
Alkaa olla toden teolla kiire kehittää vaihtoehtoisten energiamuotojen laajamittaista käyttöönottoa. Tuulet eivät maapallolta lopu, vesi ei lakkaa virtaamasta eikä aurinko sammu. Ne ovat uusiutuvia energiavaroja. Kasvimassan käyttö energiantuotantoon on myös yksi vaihtoehto, kunhan se tehdään järkevästi ilman että metsät hakataan autioiksi tai että ruoan tuotanto siitä kärsii.
Vety on ehtymätön luonnonvara. Sitä on kaikkialla, missä on hiilen ja vedyn yhdisteitä tai vettä. Vesi taas on vedyn palamistuote. Vesimolekyylissä vetyatomit ovat tiukasti molekyylisidoksin kiinni happiatomissa, mutta vesimolekyyli saadaan silti hajotettua sähköenergian avulla takaisin vedyksi ja hapeksi:
Saatu vety voidaan käyttää puhtaana polttoaineena, mutta veden hajoamisreaktiossa energiaa kuluu enemmän kuin sitä saadaan vedyn poltosta takaisin vedeksi.
Kaikkein tehokkain tapa turvata kohtuullinen energian saanti myös meidän jälkeemme tuleville sukupolville on energian säästäminen kaikessa toiminnassa. Tähän voi jokainen omalta osaltaan vaikuttaa.
7. Palamisen eri muodot
Palaminen voi olla nopeaa tai hidasta. Palamisessa vapautuu aina lämpöä. Monissa palamisilmiöissä esiintyy jonkinlaisia valo- ja liekki-ilmiöitä, mutta ei aina. On myös liekitöntä palamista. Palamisessa vapautuu usein kaasuja, etenkin eloperäisen aineen palaessa. Metallien palaessa kaasun muodostuminen on yleensä vähäistä tai se puuttuu kokonaan, ja reaktiossa muodostuu vain kiinteitä reaktiotuotteita.
Nopeassa palamisessa aineen ja hapen reaktio tapahtuu nopeasti, ja siinä vapautuu suuri määrä energiaa. Energian vapautuminen havaitaan yleensä valona, lämpönä tai tilavuuden muutoksena. Nopeaan palamiseen liittyy usein myös liekki-ilmiö. Räjähdykset ovat tyypillinen esimerkki nopeasta palamisesta. Siinä muodostuu lyhyessä ajassa suuri määrä kuumia kaasuja, jotka laajenevat ympäristöön ja aiheuttavat paineaallon. Esimerkiksi bensiini on herkästi syttyvää ja palaa kiivaasti liekehtien.

Hitaassa palamisessa vapautuu sama määrä energiaa kuin nopeassa palamisessa, mutta pidemmällä aikavälillä. Hitaasta palamisesta puuttuu yleensä valo- ja liekki-ilmiö. Metallin ruostuminen, omenan tummuminen ja soluissa tapahtuva palaminen ovat esimerkkejä hitaasta palamisesta. Näissä ilmiöissä havaitaan lämpöä, muttei ei valoa eikä liekkiä. Palamisreaktio on elintärkeä myös ihmiskehossa. Kehon 37 asteen lämpötila on nimittäin seuraus muun muassa soluissa tapahtuvista palamisreaktioista.

Vasemmalla nopeaa palamista. Oikealla esimerkki hitaasta palamisesta tehty kuluttajatuote – kädenlämmitin.
Kuparin pinnan tummuminen ajan saatossa on esimerkki hitaasta, liekittömästä palamisesta. Ilmiön selittävät pinnalla olevien kupariatomien reagoiminen ilman happimolekyylien kanssa, jolloin palamistuotteena muodostuu mustaa kuparioksidia. Tumma kuparioksidi patinoituu ajan saatossa vielä kauniin vihertäväksi kuparikarbonaatiksi.

8. Syttymisherkkyys
Aineen syttymisherkkyyteen vaikuttavat hienojakoisuus, materiaali ja aineen olomuoto. Syttymisherkkyyttä voidaan selvittää polttokokeilla. Aineen syttymisherkkyyden selvittäminen on tärkeä osa paloturvallisuutta. Lämpötilaa, jossa aine syttyy palamaan, nimitetään syttymispisteeksi. Nestemäisille aineille käytetään vastaavasti nimitystä leimahduspiste.
Kokonaista puupölkkyä on vaikea saada syttymään, mutta jos sen pilkkoo pieniksi lastuiksi, se syttyy helposti. Pilkkomalla lisätään reagoivien aineiden pinta-alaa ja siten lisätään todennäköisyyttä palamisreaktion alkuunsaaville hiukkasten törmäyksille. Hyvin hienojakoinen puupöly syttyy vaarallisen herkästi palamaan ja voi aiheuttaa pölyräjähdyksen.

Palavan materiaalin kemiallinen koostumus ja reaktiivisuus vaikuttavat syttymisherkkyyteen. Kaasumaiset aineet syttyvät helpommin kuin nestemäiset ja kiinteät aineet. Nestemäisten ja kiinteidenkin aineiden palamisessa aine yleensä saatetaan lämmittämällä kaasumaiseen tilaan, minkä jälkeen se reagoi helpommin ilman hapen kanssa.
Esimerkiksi bensiini on herkästi syttyvä aine. Sen kemiallinen koostumus on sopiva ja rakentuu ilman hapen kanssa helposti reagoivista hiilestä ja vedystä. Lisäksi se höyrystyy voimakkaasti jo huoneen lämpötilassa, joten muodostuu paljon helposti syttyviä kaasuja. Vastaavia ominaisuuksia on monilla muillakin aineilla, kuten alkoholilla, eetterillä ja asetonilla.
9. Paloturvallisuus
Paloturvallisuudessa tärkeintä on ennaltaehkäisy, oikeiden sammutustekniikoiden tunteminen ja ensiavun osaaminen. Suurin osa tulipaloista on seurausta virheellisestä toiminnasta ja rikkinäisistä laitteista. Ennaltaehkäisyssä on tärkeintä huolehtia siitä, että palovaroittimet kunnossa ja että niitä on riittävän paljon.

Sammutustekniikoissa on tärkeä tuntea, mitä aineita voi sammuttaa milläkin tavoin. Palavan nuotion voi sammuttaa tukahduttamalla kaatamalla sen päälle hiekkaa. Öljypalo pitää sammuttaa tukahduttamalla, mutta ei vedellä. Veden kaataminen palavan öljyn joukkoon aiheuttaa suurta vahinkoa, koska vesi höyrystyy nopeasti palavan öljyn lämmössä, minkä seurauksena muodostuu suuri määrä kaasua ja palava öljy roiskuu ympäriinsä.
Katso videolta rasvapalon turvallinen demonstraatio ja sammutus. Demonstraatio toteutetaan vetokaapissa.
Tärkeintä on pitää kodissa ja mökillä alkusammutusvälineet helposti saatavilla ja varmistua siitä, että jokainen tietää niiden sijainnin ja osaa niiden käytön.

 Palokaasuilla on keskeinen merkitys kodin ja koulun paloturvallisuuden näkökulmasta. Esimerkiksi savuavasta kynttilästä vapautuvat kaasut ovat kuumia ja syttymisherkkiä ja muodostavat ilmeisen tulipalovaaran ilman huolellista sammuttamista. Varsinkin isoja palopesäkkeistä vapautuvia kaasuja joudutaan usein viilentämään monia tunteja näkyvien liekkien sammuttua.
Palokaasuilla on keskeinen merkitys kodin ja koulun paloturvallisuuden näkökulmasta. Esimerkiksi savuavasta kynttilästä vapautuvat kaasut ovat kuumia ja syttymisherkkiä ja muodostavat ilmeisen tulipalovaaran ilman huolellista sammuttamista. Varsinkin isoja palopesäkkeistä vapautuvia kaasuja joudutaan usein viilentämään monia tunteja näkyvien liekkien sammuttua.
Seuraava video havainnollistaa, miten nopeasti tulipalo leviää pienestä palosta hengenvaaralliseksi. Olennaista siis on sammuttaa tulipalo välittömästi, kun se on havaittu. Jo muutaman minuutin kuluttua palon sammuttaminen kotikonstein voi muodostua mahdottomaksi.
Tiivistelmä
- Palamisen edellytykset ovat palava aine, happi ja riittävän korkea lämpötila.
- Tulipalo sammuu, jos yksi tai useampi näistä tekijöistä voidaan estää.
- Vedyn palamisreaktiossa muodostuu vettä.
- Hiilen palamisreaktiossa muodostuu hiilimonoksidia (CO) tai hiilidioksidia (CO2).
- Palamisreaktioissa vapautuu energiaa, jota ihminen hyödyntää lämmön ja sähkön tuotannossa. Tähän tarkoitukseen käytettyjä aineita kutsutaan polttoaineiksi.
- Palaminen voi olla nopeaa tai hidasta.
- Lämpötilaa, jossa aine syttyy palamaan, nimitetään syttymispisteeksi.
- Paloturvallisuudessa tärkeintä on ennaltaehkäisy, oikeiden sammutustekniikoiden tunteminen ja ensiavun osaaminen.
