1.oppitunti - Molekyylit ja poolisuus
Kotitehtävä: Poolisuus ja kotikokeellisuutta
Vastaa seuraaviin kysymyksiin:
Testaa seuraavaksi kotonasi liuottaa kanelia tai chiliä veteen. Tarttuuko maku hyvin veteen?
Kokeile myös liuottaa kanelia tai chiliä ruokaöljyyn, joka on heksaanin tavoin pooliton yhdiste. Tarttuiko maku öljyyn?
Mitä havaitsit?
- Muovikassi koostuu polyeteenimolekyyleistä.
- Onko polyeteenissä poolisia sidoksia? Perustele.
- Onko polyeteenimolekyyli poolinen? Perustele.
- Tunnilla tehdyssä demonstraatiossa havaittiin, että jodi liukenee heksaaniin mutta ei veteen. Laadi ilmiölle selitys, jossa käytät sanoja poolinen ja pooliton.
 |
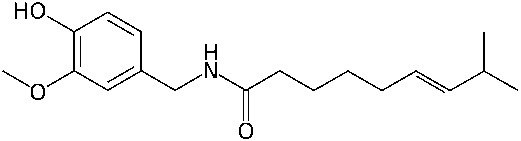 |
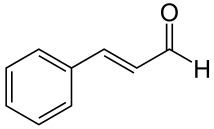
| Kanelialdehydi on yhdiste, joka antaa kanelille sen ominaisen maun. | Kapsaiini on puolestaan yhdiste, joka aiheuttaa chilikasvien poltteen. |
Testaa seuraavaksi kotonasi liuottaa kanelia tai chiliä veteen. Tarttuuko maku hyvin veteen?
Kokeile myös liuottaa kanelia tai chiliä ruokaöljyyn, joka on heksaanin tavoin pooliton yhdiste. Tarttuiko maku öljyyn?
Mitä havaitsit?
Keskeisten käsitteiden kokoamista (kertaus yläkoulusta)
PIRE-kokonaisuus käsittää (ensin) vahvat sidokset ja erityisesti johdattelee kovalenttisen sidoksen, sen mahdollisen poolisen luonteen kautta heikkoihin sidoksiin, mikä on KE1-kurssin uusi asiakokonaisuus. Vanhoja käsitteitä ovat mm.: kovalenttinen sidos, ionisidos, metallisidos, ioni, molekyyli.
Vahvojen sidoksien kertaus esim. JigSaw-menetelmällä. Ryhmissä yöstetään aiemmat käsitykset mallien muotoon.
DIA
Lähde: JigSaw-menetelmä, Kai Hakkarainen: http://mlab.taik.fi/polut/Yhteisollinen/tyokalu_jigsaw.html
Vahvojen sidoksien kertaus esim. JigSaw-menetelmällä. Ryhmissä yöstetään aiemmat käsitykset mallien muotoon.
DIA
Lähde: JigSaw-menetelmä, Kai Hakkarainen: http://mlab.taik.fi/polut/Yhteisollinen/tyokalu_jigsaw.html
Teemana kovalenttinen sidos
Ohjaava kysymys: Miksi muovipussi on kevyt ja joustava, mutta silti sillä pystyy kantamaan raskaan taakan?
Tarkoituksena on siis oppia kemiallisista sidoksista ja niiden tietojen avulla sitten vastata tähän kysymykseen. Tähän vastataan esim. portfoliossa, jota täydennätte seuraavien viiden tunnin aikana.
Pohjustusta:
- millaisia erilaisia pakkausmateriaaleja tulee mieleen?
- mitä materiaaleja kauppakassia varten on? mikä on yleisin?
- miksi muovipusseja käytetään niin paljon?
Ohjaava kysymys: millainen on muovipussin kemiallinen rakenne?

TEHTÄVÄ: Miettikää parin kanssa kysymyksiä ja valmistautukaa perustelemaan.
(kuvat Materiaalit ympärillämme –vihkosta)
Käydään sen jälkeen rakenne läpi opettajan johdolla dokukameralla.
• piirretään polyeteeniketjuja pari kappaletta
Kysellään mitä sidoksia polyeteenissä on? (peruskoulupohjalta)
Tiedekäytännöt:
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
Tarkoituksena on siis oppia kemiallisista sidoksista ja niiden tietojen avulla sitten vastata tähän kysymykseen. Tähän vastataan esim. portfoliossa, jota täydennätte seuraavien viiden tunnin aikana.
Pohjustusta:
- millaisia erilaisia pakkausmateriaaleja tulee mieleen?
- mitä materiaaleja kauppakassia varten on? mikä on yleisin?
- miksi muovipusseja käytetään niin paljon?
Ohjaava kysymys: millainen on muovipussin kemiallinen rakenne?

TEHTÄVÄ: Miettikää parin kanssa kysymyksiä ja valmistautukaa perustelemaan.
(kuvat Materiaalit ympärillämme –vihkosta)
Käydään sen jälkeen rakenne läpi opettajan johdolla dokukameralla.
• piirretään polyeteeniketjuja pari kappaletta
Kysellään mitä sidoksia polyeteenissä on? (peruskoulupohjalta)
Tiedekäytännöt:
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
Kokeellinen työ - Polymeerin valmistus (demo tai oppilastyö)
Polyamidin valmistus:
Polyamidia valmistetaan rajapintapolymeroinnilla liuottamalla lähtöaineet kahteen toisiinsa sekoittumattomaan faasin.
1. Vesifaasi valmistetaan kiinteästä diamiinista ja natriumhydroksidin (NaOH) vesiliuoksesta. Vesifaasiin lisätään indikaattoria rajapinnan näkemiseksi ja faasin tunnistamiseksi (ei siis välttämätön).
2. Orgaaninen faasi valmistettiin nestemäisestä happokloridista ja orgaanisesta liuottimesta.
Faasit yhdistetään kaatamalla tiheydeltään pienempi faasi tiheydeltään suuremman faasin päälle varovasti lasisauvaa pitkin, jotta faasit eivät pääse sekoittumaan.
Taulukko: Valmistetut polyamidit, lähtöaineet ja käytetyt liuottimet
Polyamidien 610 ja 810 valmistuksessa vesifaasi on raskaampi faasi, mutta polyamidin 66 valmistuksessa orgaanisen faasin liuotin dikloorimetaani on vettä tiheämpää. Nesteiden rajapintaan muodostuu polymeerifilmi, joka keritään nauhaksi vetolaitteen avulla.
Polyamidia valmistetaan rajapintapolymeroinnilla liuottamalla lähtöaineet kahteen toisiinsa sekoittumattomaan faasin.
1. Vesifaasi valmistetaan kiinteästä diamiinista ja natriumhydroksidin (NaOH) vesiliuoksesta. Vesifaasiin lisätään indikaattoria rajapinnan näkemiseksi ja faasin tunnistamiseksi (ei siis välttämätön).
2. Orgaaninen faasi valmistettiin nestemäisestä happokloridista ja orgaanisesta liuottimesta.
Faasit yhdistetään kaatamalla tiheydeltään pienempi faasi tiheydeltään suuremman faasin päälle varovasti lasisauvaa pitkin, jotta faasit eivät pääse sekoittumaan.
Taulukko: Valmistetut polyamidit, lähtöaineet ja käytetyt liuottimet
| Polyamidi | Diamiini | Vesifaasin liuotin | Happokloridi | Orgaaninen liuotin |
| PA 66 | 1,6-heksaanidiamiini | NaOH-liuos | Adipiinihappokliri | Dikloorimetaani |
| PA 610 | 1,6-heksaanidiamiini | NaOH-liuos | Sebasiinihappokloridi | Heksaani |
| PA 810 | 1,8-oktaanidiamiini | NaOH-liuos | Sebasiinihappokloridi | Heksaani |
Polyamidien 610 ja 810 valmistuksessa vesifaasi on raskaampi faasi, mutta polyamidin 66 valmistuksessa orgaanisen faasin liuotin dikloorimetaani on vettä tiheämpää. Nesteiden rajapintaan muodostuu polymeerifilmi, joka keritään nauhaksi vetolaitteen avulla.
Jaksollinen järjestelmä - atomien rakenteen kertausta
Millaisia aineita voimme löytää yksittäisinä atomeina?
o jalokaasut, kulta ja elohopea.
• Katsokaa ptablen avulla, mitä yhteistä on kaikkien jalokaasujen elektronirakenteessa?
Katsotaan ptablen avulla elektronien asettumista energiatasoille.
• verrataan vetyä ja heliumia
• verrataan neonia fluoriin, happeen, typpeen ja hiileen
Ptable.com
• Kovalenttinen sidos syntyy, kun kaksi atomia jakaa elektroneja saavuttaakseen jalokaasurakenteen (katsotaan orbitaalin kuva vetymolekyylistä)
• Atomi voi muodostaa useita kovalenttisia sidoksia saavuttaakseen jalokaasurakenteen.
o näitä sidoksia voi muodostaa yhden tai useamman atomin kanssa
(katsotaan ptablesta happiatomia – montako kovalenttista sidosta tarvitsee jalokaasurakenteen saavuttamiseksi?)
(piirretään happimolekyyli ja vesimolekyyli)
o jalokaasut, kulta ja elohopea.
• Katsokaa ptablen avulla, mitä yhteistä on kaikkien jalokaasujen elektronirakenteessa?
Katsotaan ptablen avulla elektronien asettumista energiatasoille.
• verrataan vetyä ja heliumia
• verrataan neonia fluoriin, happeen, typpeen ja hiileen
Ptable.com
Kovalenttinen sidos
• Kovalenttinen sidos syntyy, kun kaksi atomia jakaa elektroneja saavuttaakseen jalokaasurakenteen (katsotaan orbitaalin kuva vetymolekyylistä)
• Atomi voi muodostaa useita kovalenttisia sidoksia saavuttaakseen jalokaasurakenteen.
o näitä sidoksia voi muodostaa yhden tai useamman atomin kanssa
(katsotaan ptablesta happiatomia – montako kovalenttista sidosta tarvitsee jalokaasurakenteen saavuttamiseksi?)
(piirretään happimolekyyli ja vesimolekyyli)
Elektronegatiivisuus ja poolisuus
Otetaan esimerkiksi vetymolekyyli ja vetykloridimolekyyli. Pohditaan, onko kovalenttinen sidos molemmissa samanlainen.
- molemmissa jaetaan kaksi elektronia
- jakavien atomien rakenne kuitenkin erilainen
- Eri alkuaineilla on erilainen kyky vetää sidoselektroneja puoleensa. Tätä ominaisuutta kuvaa alkuaineen elektronega-tiivisuusarvo
- Mitä suurempi elektronegatiivisuusarvo, sitä voimakkaammin atomi vetää sidoselektroneja puoleensa.
- Alkuaineen elektronegatiivisuuteen vaikuttavat:
- atomin ytimen koko
- atomin valenssielektronien (uloimman kuoren elektronien) lukumäärä
- Jos kovalenttisen sidoksen muodostaa kaksi samanlaista atomia, elektronit jakautuvat tasaisesti.
- sidosta kutsutaan poolittomaksi
- Jos kovalenttisen sidoksen muodostaa kaksi erilaista atomia, elektronegatiivisempi atomi vetää sidoselektroneja voimak-kaammin puoleensa
- tällöin elektronegatiivisempi atomi saa negatiivisen osittaisvarauksen ja toinen atomi positiivisen osittaisvarauk-sen.
- syntyy poolinen sidos
- Molekyyli on poolinen, jos:
- siinä on poolisia sidoksia
- pooliset sidokset eivät jakaannu symmetrisesti
Kokeellinen työ: Jodin liukeneminen
Katsotaan jodin liuottaminen veteen ja heksaaniin demona.
(KUVA)
Oppilaille tehtäväksi laatia selitys ilmiölle.
Apuna:
Tiedekäytännöt:
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
5. Matemaattinen ja laskennallinen ajattelu
(KUVA)
Oppilaille tehtäväksi laatia selitys ilmiölle.
Apuna:
- MAOL elektronegatiivisuustaulukot
- MolView-ohjelman elektronitiheyspintatyökalu (esitellään tunnille jo aiemmin?)
Tiedekäytännöt:
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
5. Matemaattinen ja laskennallinen ajattelu