Soveltavat tehtävät (351–360)
Tehtävä 351
 Johann Balmer (1825–1898, kuvassa) keksi vuonna 1885 matemaattisen kaavan, jolla voitiin laskea tunnetut vetyatomin emittoimat näkyvän valon aallonpituudet. Bohrin vetyatomimalli antoi myöhemmin teoreettisen selityksen Balmerin sarjalle. Nykyään tiedetäänkin Balmerin sarjan syntyvän kun elektroni siirtyy vedyn ensimmäiselle viritystilalle.
Johann Balmer (1825–1898, kuvassa) keksi vuonna 1885 matemaattisen kaavan, jolla voitiin laskea tunnetut vetyatomin emittoimat näkyvän valon aallonpituudet. Bohrin vetyatomimalli antoi myöhemmin teoreettisen selityksen Balmerin sarjalle. Nykyään tiedetäänkin Balmerin sarjan syntyvän kun elektroni siirtyy vedyn ensimmäiselle viritystilalle.
a) Laske Balmerin sarjan lyhin aallonpituus.
b) Osoita, että ensimmäiselle viritystilalle päätyvissä siirtymissä emittoituva säteily on aina näkyvää valoa.
351
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 352
Alla on esitetty vedyn absorptiospektri, eli merkitty ne aallonpituudet, jotka voivat absorboitua vetyyn ja virittää elektronin perustilastaan.

a) Miksi absorboituvat aallonpituudet esiintyvät yhä tiheämmässä aallonpituuden pienentyessä?
b) Mitä tapahtuu aallonpituudella 91,2 nm, jota lyhyempiaaltoinen säteily näyttää absorboituvan aallonpituudesta riippumatta?
352
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 353
Ideaalikaasun molekyylien keskimääräinen liike-energia [[$ E_\text{kk} $]] riippuu kaasun lämpötilasta [[$ T $]] kaavan
[[$ \quad E_{kk}=\dfrac{3}{2}kT $]]
mukaisesti, jossa [[$ k=1,38\cdot 10^{-23} J/K $]] on ns. Boltzmannin vakio.
Laske, missä lämpötilassa vetykaasun molekyylien keskimääräinen liike-energia riittää ionisoimaan vetyatomin.
353
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 354
354
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 355
355
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 356
Tehtävä 357
 Kvartsikiteen rakennepoikkeamien energiatiloja voidaan mallintaa kuvassa esitetyllä tavalla lähekkäisten tilojen ryhminä. Ryhmiä kutsutaan tässä energiavyöhykkeiksi. Vyöhykettä A kutsutaan perustilojen vyöhykkeeksi. Kun kvartsikide ottaa vastaan energiaa, se voi virittyä kaikille kuvassa näkyville energiavyöhykkeille, mutta kun se luovuttaa energiaa, se palautuu aina vyöhykkeelle A.
Kvartsikiteen rakennepoikkeamien energiatiloja voidaan mallintaa kuvassa esitetyllä tavalla lähekkäisten tilojen ryhminä. Ryhmiä kutsutaan tässä energiavyöhykkeiksi. Vyöhykettä A kutsutaan perustilojen vyöhykkeeksi. Kun kvartsikide ottaa vastaan energiaa, se voi virittyä kaikille kuvassa näkyville energiavyöhykkeille, mutta kun se luovuttaa energiaa, se palautuu aina vyöhykkeelle A.
a) Millä aallonpituuksilla kvartsikide absorboi ja emittoi säteilyä?
b) Miten energiatilojen ryhmittyminen energiavyöhykkeiksi näkyy kvartsikiteen emittoiman säteilyn spektrissä?
(YO kevät 2015)
357
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 358
a) Laserin toimintaperiaate ja laserin valon tärkeimmät ominaisuudet.
b) Oheisessa kuvassa on esitetty argonlaserin yksinkertaisettu energiatasokaavio. Kuvaan on merkitty lasersiirtymät a ja b. Laske siirtymiä vastaavat aallonpituudet. Minkä väristä on näissä siirtymissä syntyvä valo?

(YO kevät 2008 a ja b)
358
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 359
a) Tutustu oheiseen kaaviokuvaan sekä aihetta käsittelevään Wikipedia-artikkeliin. Selitä, miten materiaaliin kohdistettu röntgensäteily synnyttää havainnoitavaa säteilyä. Miten säteilyn mittaaminen mahdollistaa alkuaineiden tunnistamisen?

![]() Röntgenfluoresenssi (Wikipedia eng.)
Röntgenfluoresenssi (Wikipedia eng.)
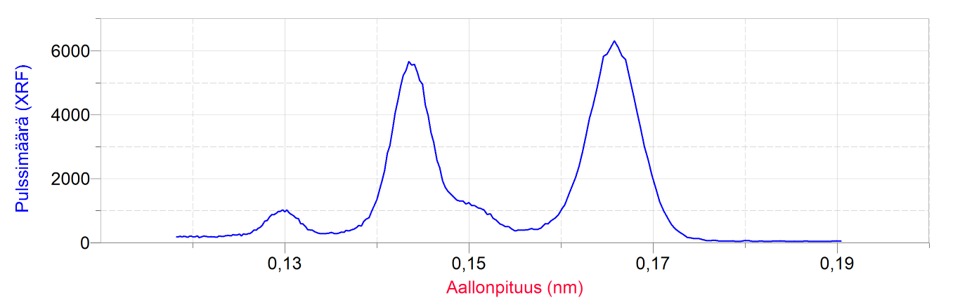
b) Erään metalliseoksen koostumusta tutkittiin XRF-menetelmällä. Materiaaliin kohdistettiin röntgensäteilyä. Materiaalin emittoimalle säteilylle mitattiin alla olevan kuvaajan mukainen spektri. Taulukossa on lueteltu metallien karakteristisen säteilyn ominaisuuksia. Selvitä spektrin perusteella, mitä alkuaineita näyte sisälsi. Halutessasi voit käsitellä spektridataa taulukkomuodossa.
| Alkuaine | [[$ K_\alpha $]](keV) | [[$ K_\beta $]](keV) |
|---|---|---|
| Cr | 5415 | 5947 |
| Fe | 6405 | 7059 |
| Ni | 7480 | 8267 |
| Cu | 8046 | 8904 |
| Zn | 8637 | 9570 |
| Ga | 9251 | 1027 |
| Ge | 9886 | 1098 |
| As | 10540 | 11726 |
| Se | 11224 | 12497 |
359
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
Tehtävä 360
 James Franck ja Gustav Hertz palkittiin Nobelin fysiikan palkinnolla v. 1925 kokeestaan, jossa he tutkivat matalapaineista elohopeahöyryä. Elohopeahöyry (Hg) oli putkessa, jossa oli viereisen kytkentäkaavion mukaisesti kolme elektrodia.
James Franck ja Gustav Hertz palkittiin Nobelin fysiikan palkinnolla v. 1925 kokeestaan, jossa he tutkivat matalapaineista elohopeahöyryä. Elohopeahöyry (Hg) oli putkessa, jossa oli viereisen kytkentäkaavion mukaisesti kolme elektrodia.
Kaavion kohdassa C on katodi. Katodina toimii hehkulanka, josta irtoaa jännitteen UH vaikutuksesta elektroneja. Katodin ja keskimmäisen elektrodin A välillä oli säädettävä jännite U1, jonka vuoksi elektronit joutuvat kiihtyvään liikkeeseen. Kiihdytetyt elektronit kulkevat verkkomaisen elektrodin A läpi. Elektrodin A ja anodin S välillä on pieni jännite U2 (U2U1), minkä vuoksi kiihdytetyillä elektroneilla tulee olla tietyn suuruinen liike-energia, jotta ne pääsevät anodille. Anodille saapuvat elektronit havaitaan sähkövirtana.
 Jännitettä U1 kasvattaessaan Franck ja Hertz havaitsivat sähkövirran kasvavan kunnes se putosi lähes nollaan jännitteen arvolla 4,9 V. Kun saavutetaan ensimmäinen sähkövirran huippuarvo, elohopeahöyryn havaittiin lähettävän ultraviolettisäteilyä, jolla oli tietty aallonpituus. Kiihdytysjännitettä kasvatettaessa ultraviolettisäteilyn aallonpituus pysyy samana. Sähkövirta kasvaa jännitteen kasvaessa kunnes putoaa lähes nollaan jännitteen arvolla 4,9 V. Sama toistuu jännitteillä, jotka ovat 4,9 V:n monikertoja.
Jännitettä U1 kasvattaessaan Franck ja Hertz havaitsivat sähkövirran kasvavan kunnes se putosi lähes nollaan jännitteen arvolla 4,9 V. Kun saavutetaan ensimmäinen sähkövirran huippuarvo, elohopeahöyryn havaittiin lähettävän ultraviolettisäteilyä, jolla oli tietty aallonpituus. Kiihdytysjännitettä kasvatettaessa ultraviolettisäteilyn aallonpituus pysyy samana. Sähkövirta kasvaa jännitteen kasvaessa kunnes putoaa lähes nollaan jännitteen arvolla 4,9 V. Sama toistuu jännitteillä, jotka ovat 4,9 V:n monikertoja.
Selitä, miten havaittu jännite–sähkövirta-riippuvuus liittyy elohopea-atomien ominaisuuksiin.
Franckin ja Hertzin koejärjestely on toteutettavissa myös muilla kaasuilla. Valokuvassa näkyy neonkaasun lähettämää oranssinpunaista valoa alhaalla olevan katodin C ja keskellä olevan verkkomaisen elektrodin A välissä.

360
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.
360
Sinulla ei ole tarvittavia oikeuksia lähettää mitään.