17. Hapot ja emäkset
Aine voi olla hapan, emäksinen tai neutraali
Muistellaanpa ensin karboksyylihappoja, joiden yhteydessä jo puhuttiin hieman hapoista. Mainittiin esimerkiksi, että muurahaiset erittävät muurahaishappoa puolustautumiseen, ja että etikkahapon avulla voidaan elintarvikkeiden happamuutta lisätä jolloin ne säilyvät paremmin. Sitruunahappo taas tekee sitruunasta happaman makuisen.
Ennestään tiedät että ioniyhdisteiden vesiliuokset johtavat sähköä. Vedessä vapaasti liikkumaan pääsevät positiiviset ja negatiiviset ionit toimivat sähkön kuljettajina.
[[$ \text{H}^+ + \text{H}_2\text{O} \rightarrow \text{H}_3\text{O}^+ $]]
Emäksisyys on happamuuden vastakohta. Eli emäs taas on aine, joka pystyy vastaanottamaan vetyionin (H+). Vesiliuoksen emäksyys johtuu hydroksidi-ioneista (OH-).
[[$ \text{NaOH} + \text{H}_2\text{O} \rightarrow \text{Na}^+ + \text{OH}^- $]]
Liuos voi myös neutraali. Neutraalissa liuoksessa on yhtä monta oksonium- ja hydroksidi-ionia.
Tutki ilmiötä tällä Java-simulaatiolla.
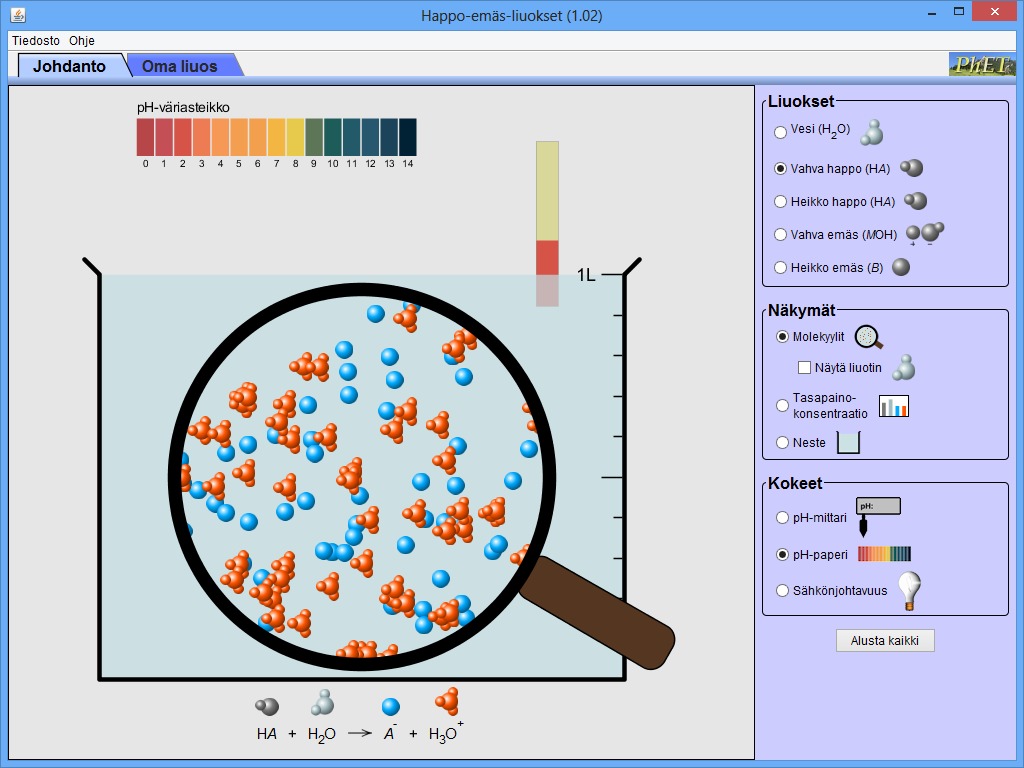
Ennestään tiedät että ioniyhdisteiden vesiliuokset johtavat sähköä. Vedessä vapaasti liikkumaan pääsevät positiiviset ja negatiiviset ionit toimivat sähkön kuljettajina.
Videosta huomaat, että happojen ja emästen vesiliuokset johtavat myös sähköä. Niidenkin täytyy tuottaa vesiliuoksiinsa ioneja.
Sitruunahapon makuaistimus ei johdu happomolekyylista vaan sen kyvystä luovuttaa vetyioni eli protoni (H+). Tämä happomolekyylistä irtoava vetyioni reagoi välittömästi vesimolekyylin kanssa ja syntyy oksoniumioni, joka aiheuttaa vesiliuoksen happamuuden.[[$ \text{H}^+ + \text{H}_2\text{O} \rightarrow \text{H}_3\text{O}^+ $]]
Emäksisyys on happamuuden vastakohta. Eli emäs taas on aine, joka pystyy vastaanottamaan vetyionin (H+). Vesiliuoksen emäksyys johtuu hydroksidi-ioneista (OH-).
[[$ \text{NaOH} + \text{H}_2\text{O} \rightarrow \text{Na}^+ + \text{OH}^- $]]
Liuos voi myös neutraali. Neutraalissa liuoksessa on yhtä monta oksonium- ja hydroksidi-ionia.
Tutki ilmiötä tällä Java-simulaatiolla.

Happamuus todetaan indikaattorilla
Indikaattorit ovat väriaineita, joita käytetään liuoksen happamuuden toteamiseen. Indikaattorit ovat erivärisiä happamassa, neutraalissa ja emäksisessä liuoksessa. Indikaattoreiden värit tunnetaan, joten niiden avulla voidaan päätellä liuoksen happamuus.

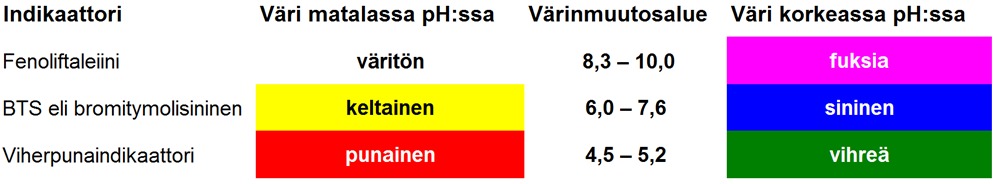
Esimerkiksi BTS:n väri muuttuu keltaisesta vihreän kautta siniseen. Fenoliftaleiini muuttuu värittömästä fuksiaan, joka on kirkkaan vaaleanpunainen.

Myös esim. puolukasta ja punakaalista voidaan valmistaa indikaattoriliuos.

Video luonnonindikaattorien värinmuutoksista.


Esimerkiksi BTS:n väri muuttuu keltaisesta vihreän kautta siniseen. Fenoliftaleiini muuttuu värittömästä fuksiaan, joka on kirkkaan vaaleanpunainen.

Myös esim. puolukasta ja punakaalista voidaan valmistaa indikaattoriliuos.

Video luonnonindikaattorien värinmuutoksista.
Happamuus ilmaistaan pH-arvona
Kaikki happamat ruoka-aineet eivät ole yhtä happamia, eivätkä emäksiset yhtä emäksisiä On olemassa siis eri vahvuisia happoja ja emäksiä. Aineiden vesiliuoksen happamuus ilmaistaan pH-asteikolla, joka kertoo onko liuos neutraali, hapan tai emäksinen.
pH:ta voidaan mitata esimerkiksi pH-paperilla tai pH-mittarilla.

Huomaa, että saippua voi olla myös emäksistä (vertaa alta taulukosta).
Hyvin happamat tai emäksiset liuokset ovat vaarallisen syövyttäviä. Alta taulukosta näet joidenkin tuttujen aineiden pH-arvoja.
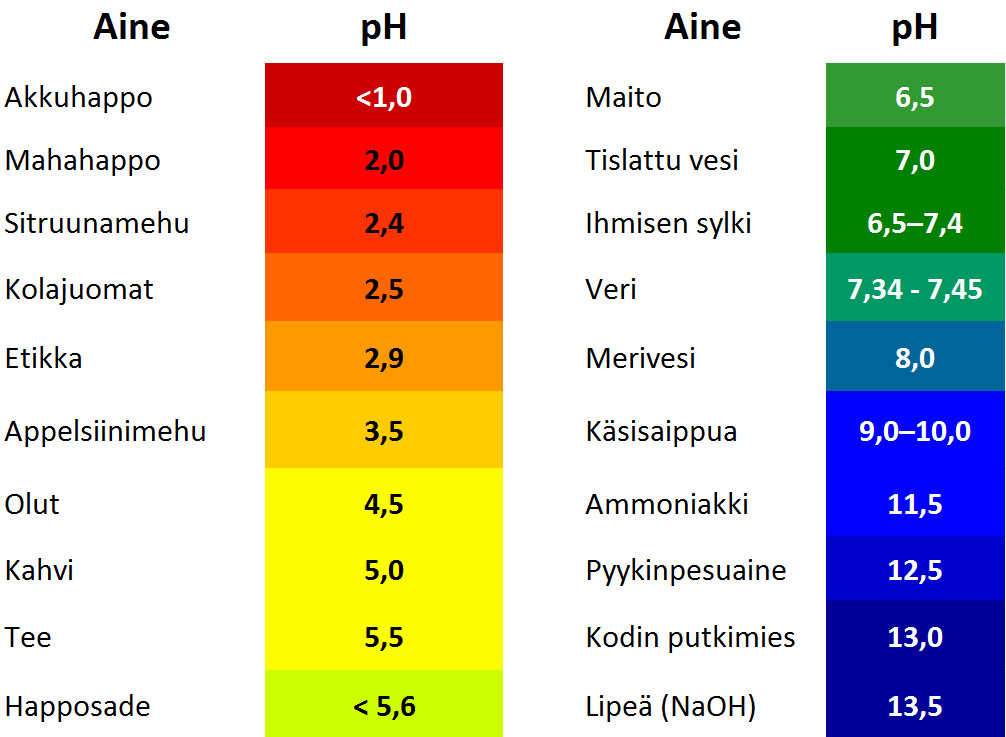
- pH < 7 hapan
- pH = 7 neutraali
- pH > 7 emäksinen
pH:ta voidaan mitata esimerkiksi pH-paperilla tai pH-mittarilla.

Huomaa, että saippua voi olla myös emäksistä (vertaa alta taulukosta).
Hyvin happamat tai emäksiset liuokset ovat vaarallisen syövyttäviä. Alta taulukosta näet joidenkin tuttujen aineiden pH-arvoja.

Happosade
Happosade on sadetta, jonka pH on alle 5,6. Sadevesi on normaalistikin hiukan hapanta (pH hieman alle 6), koska ilmakehän hiilidioksidi liukenee sadeveteen ja muodostaa hiilihappoa. Hiilihappo on heikko happo. Itse happosade johtuu sadeveteen liuenneista ilmansaasteista, kuten esim. teollisuuden rikki- ja typpipäästöistä.

Soittolistassa on kaksi videota. Ensimmäisessä muutetaan veden pH:ta puhaltamalla. Muutoksen saa aikaan ihmisen hengityksessä oleva hiilidioksidi. Toisessa videossa rakennetaan hiilidioksidimolekyyli muovimalleilla.

Soittolistassa on kaksi videota. Ensimmäisessä muutetaan veden pH:ta puhaltamalla. Muutoksen saa aikaan ihmisen hengityksessä oleva hiilidioksidi. Toisessa videossa rakennetaan hiilidioksidimolekyyli muovimalleilla.