Sähkön tuottoa ja käyttöä
Sähkökemian historiaa
- Luigi Galvani luuli keksineensä "eläinsähkön"
https://backyardbrains.com/experiments/Galvani_Volta
- Alessandro Volta osoitti, että kahden metallin välillä kulkee sähkövirta, jos ne on upotettu sähköä johtavaan liuokseen eli elektrolyyttiin
- Elektrolyytti = ioneja sisältävä liuos (joka johtaa siksi sähköä)
- Lisätietoa:
- Eläinten (ja ihmisten) kudosnesteet ovat elektrolyyttejä
- Kaikki ihmisen solujen, hermojen ja lihasten toiminta perustuu sähkökemiaan
- Eläimiä ei siis tarvittu muuhun kuin elektrolyytiksi!
Sähkökemiallinen pari
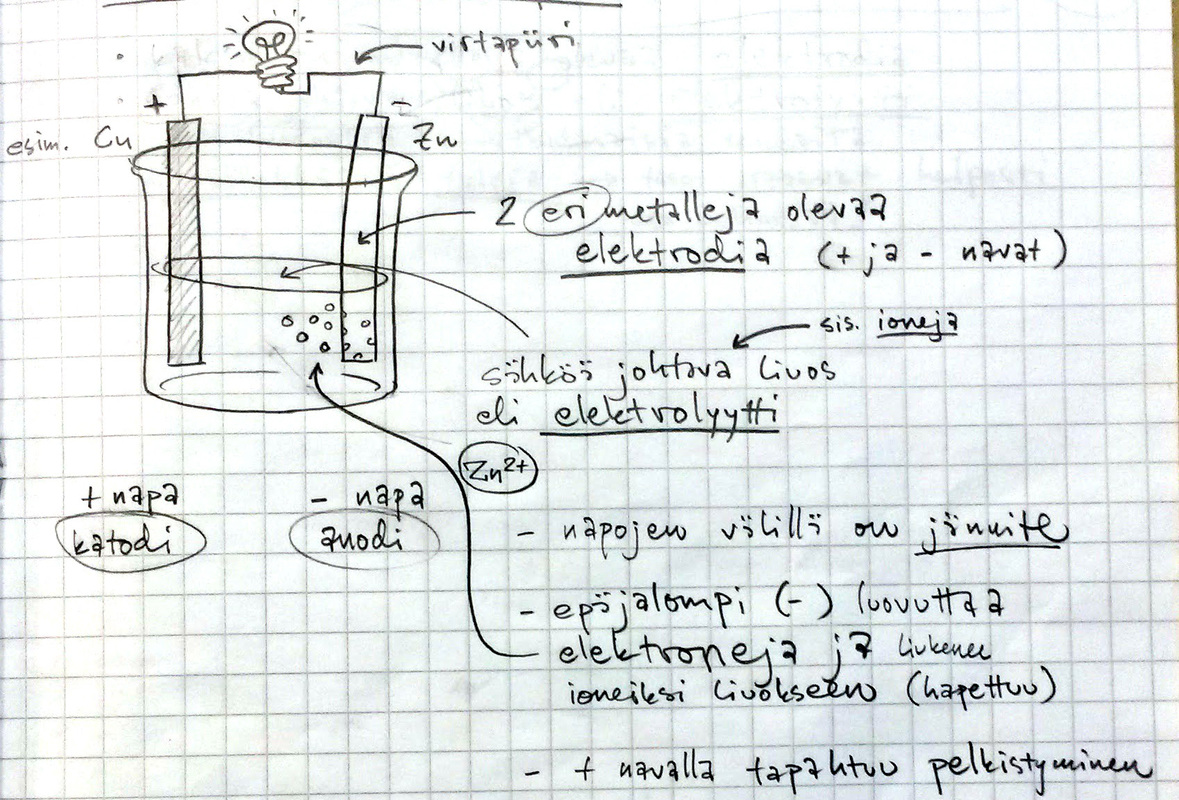
- Kahden eri metallin välille muodostuu potentiaaliero eli jännite
- Sitä suurempi mitä kauempana toisistaan jännitesarjalla
- Paristot ovat sähköparin sovelluksia
- sinkki-hiili -paristo: Zn + MnO2, elektrolyyttinä NH4Cl-hyytelö (hiilisauva päällystetty mangaanioksidilla)
- alkaliparistoissa elektrolyyttinä emäs (eli alkali) NaOH tai KOH (elektrodeina edelleen Zn + MnO2)
- Akuissa kemialliset reaktiot ovat käännettäviä
- käytettäessä (eli purettaessa) sähköpari antaa sähkövirtaa
- ladattaessa reaktio etenee päinvastaiseen suuntaan (ulkoinen jännitelähde!)
- Litiumioniakku on nykyisin yleisin ladattavissa sähkölaitteissa käytettävä energianlähde
| HUOM! Paristoja ei voi ladata! Kemiallinen reaktio ei toimi elektrolyysissä ja tuloksena on voimakas lämpötilan nousu ja mahdollinen räjähdys. |
Elektrolyysi
- Elektrolyysissä sähköparissa tapahtuva reaktio pakotetaan päinvastaiseen suuntaan ulkoisella jännitelähteellä (sähköllä!)
- positiiviset ionit pelkistyvät alkuaineeksi katodin pinnalle (+ ja - navat toisin päin kuin sähköparissa!)
- käyttöä: epäjalojen metallien puhdistus, kaasujen valmistus, sähköä johtavien esineiden pinnoitus