Muovikalvon, suolan ja alumiinifolion ominaisuuksia
Oppilaat saavat elmukelmua, suolaa ja alumiinifoliota. Esitetään mallit näiden kolmen rakenteesta.
Mallit:
Ionisidos
Metallisidos
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
6. Selitysten rakentelu ja ratkaisujen muotoilu
7. Argumenttien sitominen tutkimustuloksiin
- Millaisia sidoksia näissä kolmessa materiaalissa esiintyy?
- Tutki materiaalien sähkönjohtavuutta.
- Selitä sähkönjohtavuusmittausten havaintosi materiaalien mallien avulla. Kehitä mallia edelleen, jos tarve.
Mallit:
 |
 |
 |
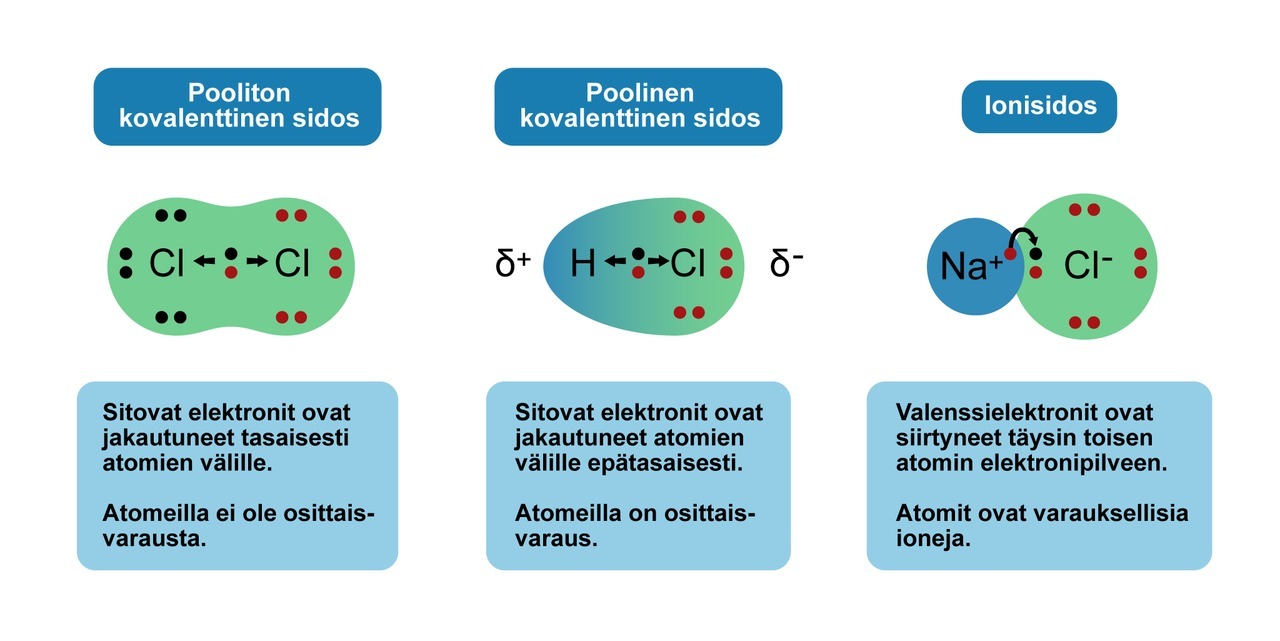
Ionisidos
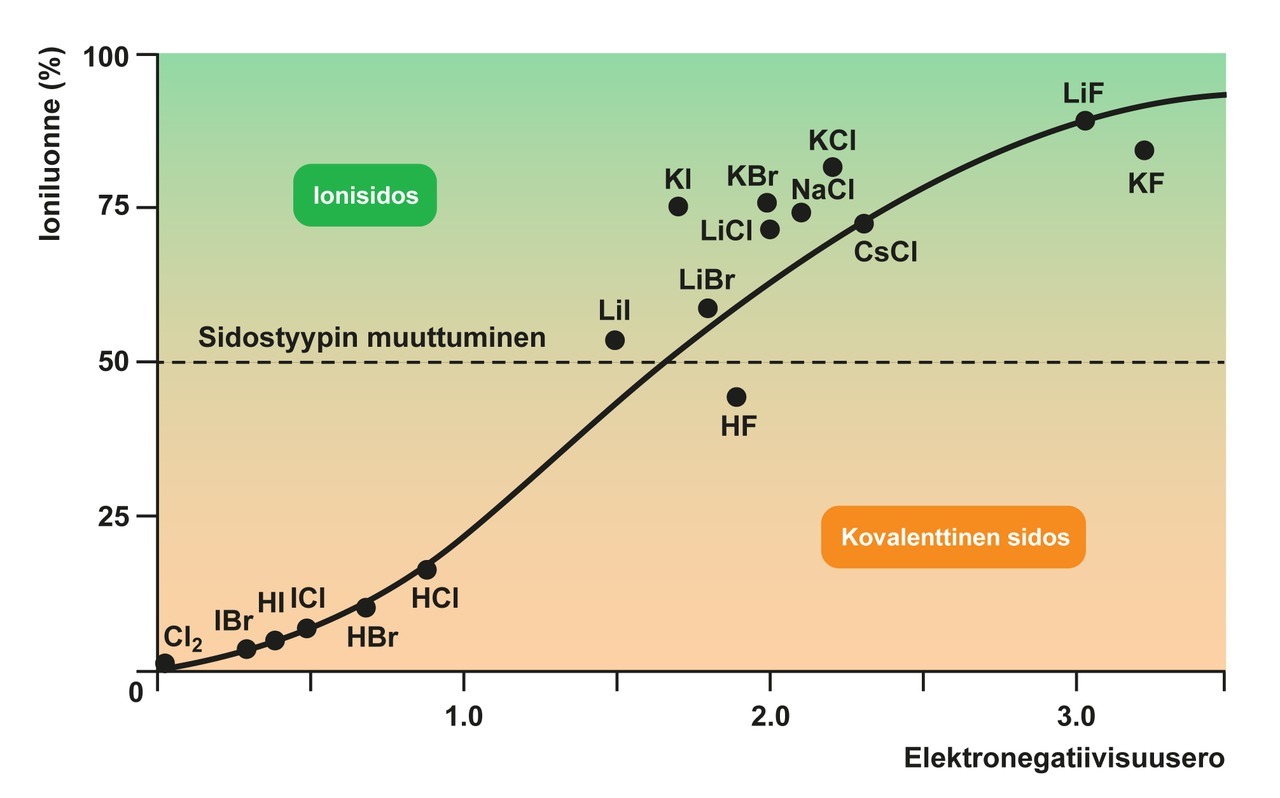
- Kun kahden atomin välinen elektronegatiivisuusero kasvaa suureksi, elektronegatiivisempi atomeista voi viedä sidoselektronin kokonaan itselleen.
- Syntyy positiivinen ja negatiivinen ioni, joiden välillä on ionisidos.
- usein ionisidoksen rajana pidetään elektronegatiivisuuseroa, joka on vähintään 1,7
- Yleensä ajatellaan, että epämetallin ja metallin välinen sidos on ionisidos.
- Voidaan myös ajatella, että sidoksella on sekä ioniluonnetta että kovalenttista luonnetta – eikä tarkkaa rajaa välttä-mättä voida vetää.
 |
 |
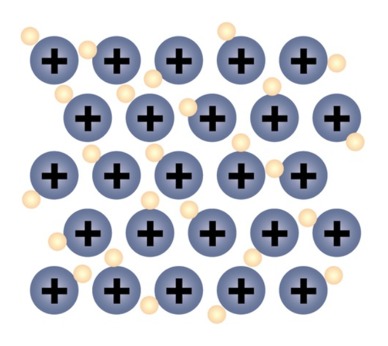
Metallisidos
- Metalliatomien uloimmat elektronit on yleensä helppo irrottaa ytimestä.
- Metalliatomit jakavatkin näitä elektroneja keskenään helposti. Jaetut elektronit muodostavat metallisidoksen.
- nämä jaetut elektronit pääsevät helposti liikkumaan metallihilassa, minkä vuoksi metallit johtavat hyvin sähköä
- Metalliatomit muodostavat tiiviin metallihilan. Hilassa voi esiintyä myös kovalenttisia sidoksia metalliatomien välillä, jolloin metal-lista tulee kovaa.
2. Mallien kehittely ja käyttö
4. Aineiston analysointi ja tulkitseminen
6. Selitysten rakentelu ja ratkaisujen muotoilu
7. Argumenttien sitominen tutkimustuloksiin