3. Kemiallisen reaktion tunnuspiirteet. TÄRKEITÄ SANOJA: KEMIALLINEN REAKTIO, LÄHTÖAINEET, REAKTIOTUOTTEET.
KEMIALLINEN REAKTIO ON TAPAHTUMA, JOSSA AINEET REAGOIVAT KESKENÄÄN JA MUUTTUVAT UUSIKSI AINEIKSI
Kemiallisia reaktioita: palaminen, ruostuminen, patinoituminen
Fysikaalisia tapahtumia: sulaminen, höyrystyminen, jähmettyminen
Fysikaalisissa tapahtumissa aine pysyy samana. Siksi ne eivät ole kemiallisia reaktioita.
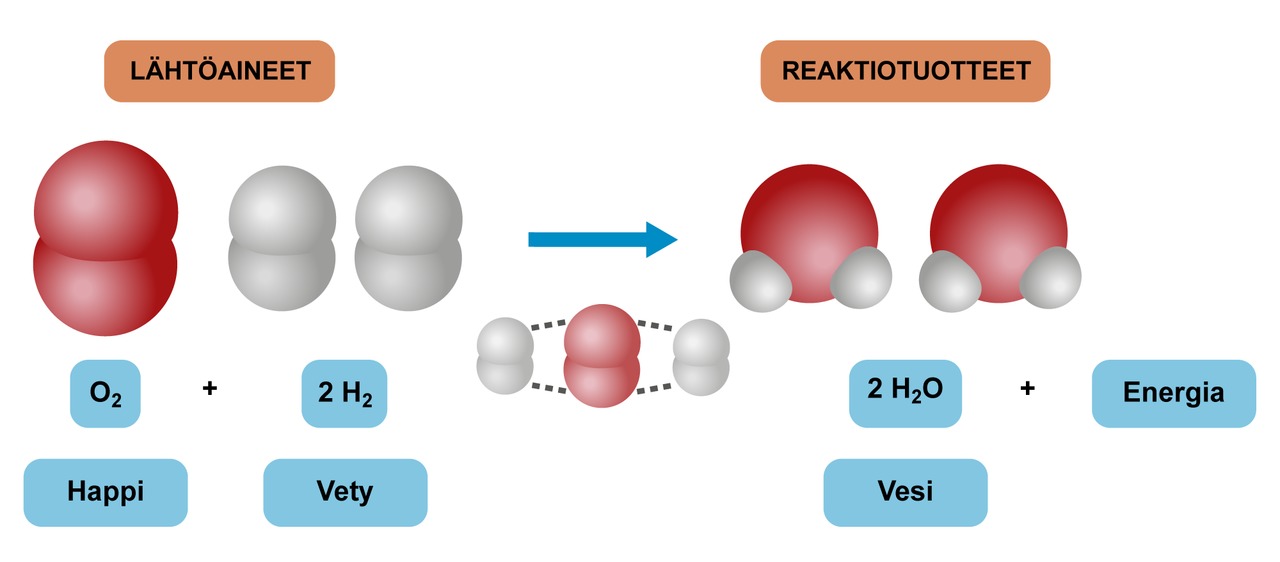
Opettaja valmistaa suolahapon ja metallin reaktiolla vetykaasua ja kerää sen koeputkeen. Toisella reaktiolla hän valmistaa vetyperoksidista mangaanioksidin avulla happea ja kerää sen samaan koeputkeen. Kaasuseosta lämmitetään tuomalla palava tulitikku koeputken suuaukolle. Kuumentuneet kaasut reagoivat herkästi. Reaktiotuotteena muodostuu vettä ja samalla vapautuu suuri määrä energiaa valona ja lämpönä.
Valo ja lämpö ovat peräisin happi- ja vetyatomien sitoutumisessa vapautuvasta energiasta. Vapautunut lämpöenergia kuumentaa tuotteena muodostuneen veden höyryksi. Höyry vaatii suuremman tilan kuin sama määrä vettä nesteenä, sillä höyry laajenee nopeasti ympäröivän ilman joukkoon ja muodostaa paineaallon. Korva aistii ilmanpaineen vaihtelut äänenä, mikä tässä tapauksessa havaitaan poksahduksena tai vingahduksena.
Esimerkki: vetykaasun muodostuminen
Esimerkkikokeessa kuumentaminen saa aikaan sen, että molekyylit törmäilevät toisiinsa yhä useammin ja yhä voimakkaammin. Monet törmäyksistä ovat sellaisia, että happi- ja vetymolekyylien atomit pääsevät riittävän lähelle toisiaan, mikä mahdollistaa reaktion niiden välillä. Lähtöainemolekyylien sisäiset sidokset heikkenevät ja uusia muodostuu happi- ja vetyatomien kesken. Lopulta alkuperäiset sidokset katkeavat ja lähtöaineatomit ryhmittyvät uudelleen siten, että jokaiseen happiatomiin liittyy kaksi vetyatomia. Reaktiotuotteena muodostuu uusi yhdiste vesimolekyylejä.