9. Energian vapautuminen ja sitoutuminen
 Osa kemiallisista reaktioista tuottaa ympäristöönsä energiaa, toiset taas tarvitsevat energiaa tapahtuakseen. Palava nuotio on hyvä esimerkki energiaa tuottavista reaktiosta. Kun puut ensin saadaan sytytettyä, palaminen jatkuu reaktiossa vapautuvan lämpöenergian ansiosta. Nuotion äärellä on hyvä lämmitellä, sillä puukuitujen kemiallisiin sidoksiin varastoitunut kemiallinen energia vapautuu lämpönä ympäristöön.
Osa kemiallisista reaktioista tuottaa ympäristöönsä energiaa, toiset taas tarvitsevat energiaa tapahtuakseen. Palava nuotio on hyvä esimerkki energiaa tuottavista reaktiosta. Kun puut ensin saadaan sytytettyä, palaminen jatkuu reaktiossa vapautuvan lämpöenergian ansiosta. Nuotion äärellä on hyvä lämmitellä, sillä puukuitujen kemiallisiin sidoksiin varastoitunut kemiallinen energia vapautuu lämpönä ympäristöön.
Tulitikun syttymiseen tarvittava energia otetaan raapaisusta. Kun tulitikku on kerran saatu sytytettyä, palaminen edistyy reaktiossa vapautuvan lämpöenergian ansiosta niin kauan kuin palavaa puuta on jäljellä ja happea saatavilla.

Kemiallisissa reaktioissa muodostuvasta lämmöstä voi olla vaaraa. Vanha kemian sananlasku opettaa "ensin vesi, sitten happo, muuten tulee käteen rakko". Loru on tärkeä, sillä monien happojen liuetessa veteen vapautuu lämpöenergiaa. Sitä voi vapautua niin paljon, että vesi höyrystyy ja polttavan kuumaa happoliuosta lentää ympäristöön.

Osa kemiallisista reaktioista sitoo energiaa ympäristöstään. Tämä havaitaan esimerkiksi liuoksen jäähtymisenä. Esimerkiksi yhteyttäminen on reaktio, joka tarvitsee energiaa tapahtuakseen. Samoin monet ruoanvalmistukseen liittyvät reaktiot ovat sellaisia, jotka vaativat energiaa tapahtuakseen, kuten kasvisten tai lihan kypsyminen.
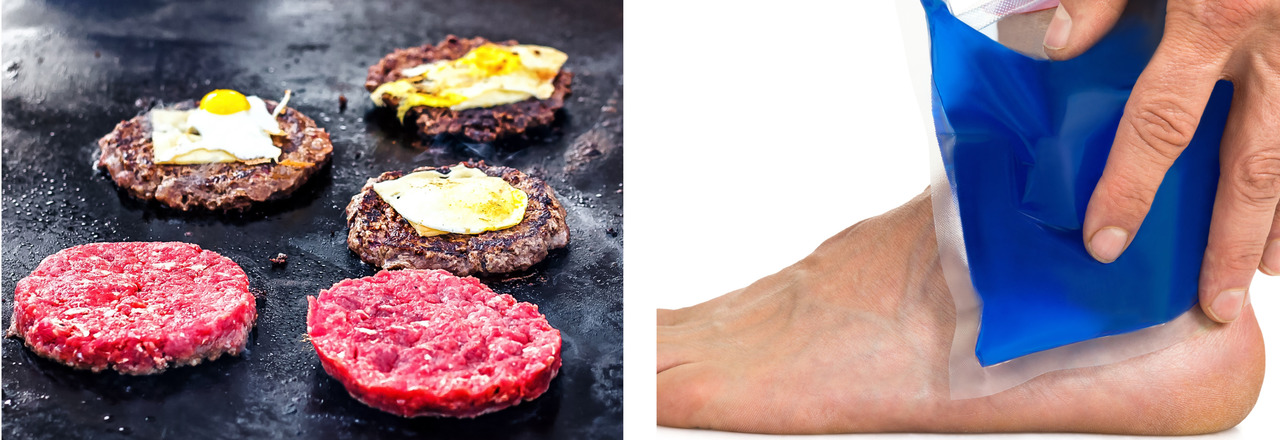
Ruoanvalmistuminen tarvitsee energiaa. Urheiluvammaan annetaan ensiapuna kylmää, joka sitoo energiaa vamma-alueelta ja hidastaa vammaan liittyviä kemiallisia reaktioita.
Tässä videossa nähdään ruokasoodan ja etikan välinen reaktio, jossa sitoutuu energiaa. Energiaa sitovat reaktiot ovat endotermisiä reaktioita ja energiaa vapauttavat reaktiot ovat eksotermisiä reaktioita.