8.1 Fotonit, atomin energiatasot ja aaltohiukkasdualismi
Fotonit
Sähkömagneettisen säteilyn energia esiintyy paketteina (kvantteina), joita kutsutaan fotoneiksi. Säteily absorboituu tai emittoituu kokonaisina fotoneina.

Fotonin energia on suoraan verrannollinen säteilyn taajuuteen: [[$ E=hf $]].
Fotonilla on liikemäärä: [[$ p=h/\lambda $]]

Fotonin energia on suoraan verrannollinen säteilyn taajuuteen: [[$ E=hf $]].
Fotonilla on liikemäärä: [[$ p=h/\lambda $]]
Fotonin energia voidaan laskea elektronivoltteina tai jouleina. Useimmissa yhteyksissä käytetään elektronivolttia. Planckin vakion yksikkö valitaan halutun energian yksikön mukaisesti. Voidaan siis laskea esimerkiksi taajuudeltaan 1,4 PHz:n säteilyn fotonin energia seuraavasti:
[[$ \quad E=hf=6,62606957 \cdot 10^{-34} \text{ Js}\cdot 1,4 \cdot 10^{15}\text{ Hz} \approx 9,3 \cdot 10^{-19}\text{ J} $]]
tai
[[$ \quad E=hf=4,13566751 \cdot 10^{-15} \text{ eVs}\cdot 1,4 \cdot 10^{15}\text{ Hz} \approx 5,8\text{ eV} $]]
Valosähköilmiö
Sähkömagneettinen säteily voi irrottaa elektroneja metallista, mikäli sen taajuus ylittää metalllille ominaisen kynnystaajuuden.
Valosähköilmiössä fotonin energia muuttuu irrotustyöksi (W0) ja irtoavan elektronin liike-energiaksi: [[$ hf=W_0+E_k $]]
Säteilyn yksittäisen fotonin energian tulee olla irrotustyötä suurempi, jotta valosähköilmiö tapahtuu.

1: Matalataajuuksinen (pitkäaaltoinen) säteily ei synnytä valosähköilmiötä, koska yksittäisen fotonin energia ei riitä irrottamaan elektronia.
2: Kynnystaajuudella fotonin energia on irrotustyön suuruinen, jolloin elektroneja irtoaa.
3: Suurella taajuudella irtoaa elektroneja, joilla on sitä enemmän liike-energiaa, mitä suurempi on säteilyn taajuus.
Valosähköilmiössä fotonin energia muuttuu irrotustyöksi (W0) ja irtoavan elektronin liike-energiaksi: [[$ hf=W_0+E_k $]]
Säteilyn yksittäisen fotonin energian tulee olla irrotustyötä suurempi, jotta valosähköilmiö tapahtuu.

1: Matalataajuuksinen (pitkäaaltoinen) säteily ei synnytä valosähköilmiötä, koska yksittäisen fotonin energia ei riitä irrottamaan elektronia.
2: Kynnystaajuudella fotonin energia on irrotustyön suuruinen, jolloin elektroneja irtoaa.
3: Suurella taajuudella irtoaa elektroneja, joilla on sitä enemmän liike-energiaa, mitä suurempi on säteilyn taajuus.
Atomin energiatasot
Atomien elektronien energiat on kvantittuneet eli ne saavat vain tiettyjä kiinteitä arvoja. Atomi virittyy vastaanottaessaan juuri sopivan määrän energiaa fotonin muodossa. Tällöin atomin elektroni siirtyy korkeammalle energiatasolle.
Elektronit palaavat luonnostaan kohti alinta energiatasoa, jolloin atomin viritystila purkautuu ja se luovuttaa energiaa fotonina. Viritystila voi purkautua vaiheittain useiden viritystilojen kautta.
Atomi vastaanottaa tai luovuttaa vain fotoneita, joiden energia on täsmälleen kahden tilan energioiden välisen erotuksen [[$ \Delta E $]] suuruinen. Fotonin aallonpituus lasketaan tällöin kaavasta:
[[$ \quad \Delta E=\dfrac{hc}{\lambda} $]]
Vetyatomin elektronin mahdolliset energiat noudattavat kaavaa
[[$ \quad E_n=-\dfrac{13,6 \text{ eV}}{n^2} $]]
Vedyn perustilaa kuvaa arvo n=1. Vedyn ensimmäistä viritystilaa vastaa arvo n=2, toista viritystilaa n=3 jne.
Vetyatomiin sidotun elektronin energia on negatiivinen. Korkeimpien viritystilojen energiat ovat hyvin lähellä nollaa. Fotoni, jonka energia on 13,6 eV tai suurempi, aiheuttaa vedyn ionisoitumisen.
Aineen atomit absorboivat fotoneita, joiden energia on juuri sopiva virittämään atomin perustilasta jollekin viritystilalle. Absorptiospektristä puuttuvat tällaisten fotonien aallonpituudet. Aineen virittyneet atomit emittoivat fotoneita, joiden energia vastaa siirtymiä viritystilalta kohti perustilaa.Emissiospektri koostuu aallonpituuksista, joita vastaava fotoni on vapautunut virityksen purkautuessa.
Elektronit palaavat luonnostaan kohti alinta energiatasoa, jolloin atomin viritystila purkautuu ja se luovuttaa energiaa fotonina. Viritystila voi purkautua vaiheittain useiden viritystilojen kautta.
Atomi vastaanottaa tai luovuttaa vain fotoneita, joiden energia on täsmälleen kahden tilan energioiden välisen erotuksen [[$ \Delta E $]] suuruinen. Fotonin aallonpituus lasketaan tällöin kaavasta:
[[$ \quad \Delta E=\dfrac{hc}{\lambda} $]]

Vetyatomin energiatasot
Vetyatomin elektronin mahdolliset energiat noudattavat kaavaa
[[$ \quad E_n=-\dfrac{13,6 \text{ eV}}{n^2} $]]
Vedyn perustilaa kuvaa arvo n=1. Vedyn ensimmäistä viritystilaa vastaa arvo n=2, toista viritystilaa n=3 jne.
Vetyatomiin sidotun elektronin energia on negatiivinen. Korkeimpien viritystilojen energiat ovat hyvin lähellä nollaa. Fotoni, jonka energia on 13,6 eV tai suurempi, aiheuttaa vedyn ionisoitumisen.
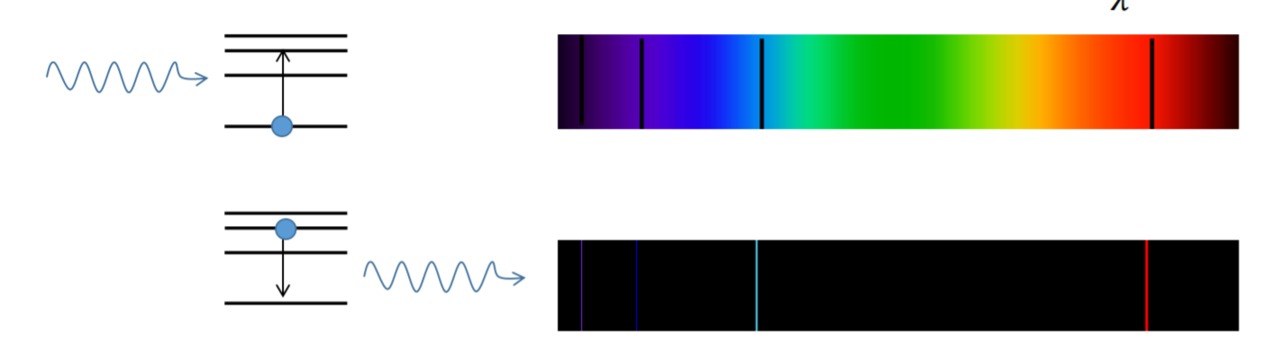
Absorptio- ja emissiospektri
Aineen atomit absorboivat fotoneita, joiden energia on juuri sopiva virittämään atomin perustilasta jollekin viritystilalle. Absorptiospektristä puuttuvat tällaisten fotonien aallonpituudet. Aineen virittyneet atomit emittoivat fotoneita, joiden energia vastaa siirtymiä viritystilalta kohti perustilaa.Emissiospektri koostuu aallonpituuksista, joita vastaava fotoni on vapautunut virityksen purkautuessa.