Energia ja laskut
Energia ja olomuodon muutokset
- Aineen lämmittäminen kuluttaa energiaa (liike lisääntyy, energiaa sitoutuu)
- Myös olomuodon muuttaminen kuluttaa energiaa
- Olomuodon muuttuessa aineen lämpötila ei muutu! (kaavio VP s.110)
- (kaikki energia kuluu sidosten rikkomiseen)
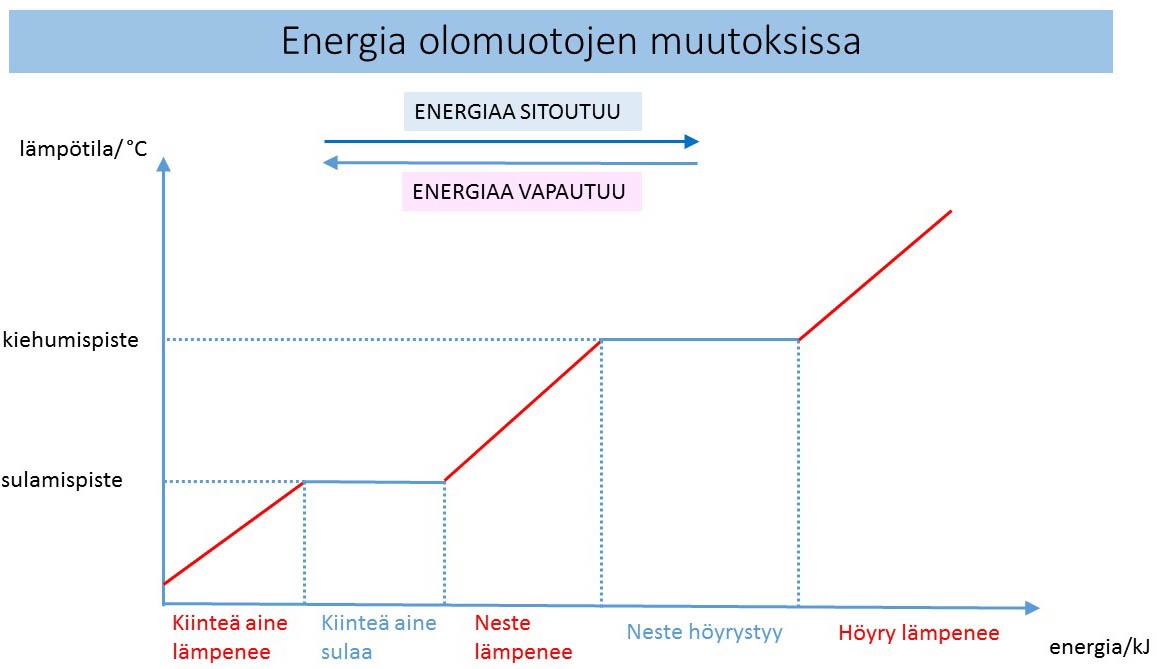
lähde: https://otavanopisto.muikkuverkko.fi/workspace/ke1-kemiaa-kaikkialla/materials#page-115161
-
- Aineen lämpeneminen, sulaminen ja höyrystyminen sitovat (kuluttavat) energiaa
- Aineen viileneminen, jähmettyminen ja tiivistyminen vapauttavat energiaa
- Haihtuminen vs. kiehuminen
- haihtumista tapahtuu kaikissa lämpötiloissa, nesteen pinnalta
- kiehuminen tapahtuu aineen kiehumispisteessä, kaikkialta nesteessä
- kuvia googlella (evaporation = haihtuminen, boiling = kiehuminen)
Olomuodon muutoksiin liittyvät laskut
Ominaissulamislämpösulamiseen tarvittava energia on [[$$ Q=s \cdot m $$]] jossa Q on lämpömäärä (energia, kJ), s on ominaissulamislämpö (kJ/kg) ja m on massa (kg) |
- Aineen ominaisuus (eri aineilla eri arvot!)
- ominaissulamislämpöjä löytyy taulukoista (kirjan s. 111)
- Wikipedia (heat of fusion, HUOM! [[$ \frac{J}{g} = \frac{kJ}{kg} $]])
- Wikipedia (heat of fusion, HUOM! [[$ \frac{J}{g} = \frac{kJ}{kg} $]])
- HUOM! ominaissulamis- ja höyrystymislämmöt eivät mitenkään liity lämpötilaan vaan energiaan!
Ominaishöyrystymislämpö
- Aineen höyrystymiseen vaadittava energia
- Taulukoita kirjan s. 111, Wikipedia
- Aineen ominaisuus kuten sulamislämpökin
Ominaissulamis- ja höyrystymislämpö, esimerkit
Esim 1. Kuinka paljon energiaa tarvitaan kun halutaan sulattaa 250 g sulamispisteessään olevaa rautaa?
- raudan ominaissulamislämpö s on 276 kJ/kg
- tehtävässä raudan massa m on 250 g = 0,25 kg
- [[$ Q=s \cdot m = 276 kJ/kg \cdot 0,25 kg = 69 kJ $]]
- rauta pitää ensin lämmittää sulamispisteeseen (VP s.102-3!)
- raudan sulamispiste 1535 °C (lämpötilan muutos siis 1535-25 =1510°C)
- raudan ominaislämpökapasiteetti 0,45 kJ/kg°C
- [[$ Q_lämmitys = c m \Delta t = 0,45 \cdot 0,25 \cdot 1510 = 169,875 kJ \approx 170 kJ $]]
- sitten itse sulamiseen saman verran kuin esimerkissä 1 eli 69 kJ
- yhteensä [[$ Q=170kJ+69kJ=239kJ $]]