Kotitehtävien malliratkaisut
Sisällys
Luku 1: Lämpö laajentaa
7.
a) 100 ℃ = 373 K
b) 0 ℃ = 273 K
c) 0 ℃ = 273 K
d) 0 ℃ = 273 K
e) Kehon lämpötila voi vaihdella 35,8–37,8 °C. Yleensä normaali lämpötila kainalosta tai peräaukosta mitattuna on joitakin kymmenyksiä alle 37 ℃ = 310 K. Kuume tarkoittaa, että lämpöä on yli 37,5 ℃.
d) Celsius-asteikon peruspisteet ovat veden sulamispiste 0 ℃ ja veden kiehumispiste 100 ℃.
8. Tämän tehtävän vastaukset riippuvat siitä, miten paljon pidät ulkoilusta ja saunomisesta. Saunan voi lämmittää 130–140 °C, mutta saunominen ei ole silloin enää miellyttävää. Suomen pakkasennätys –51,5 °C on mitattu Kittilässä 1999.
Kotipakastimessa on tavallisesti –18 °C. Leivinuunissa tai hiiligrillissä hiilloksen lämpötila on parhaimmillaan 800 – 1200 °C.
9.
a) Nestemäinen vesi on tiheimmillään +4 °C lämpötilassa. Jäähtyessään lähelle jäätymispistettä 0 °C vesi laajenee. Yli +4 °C lämpötilassa vesi laajenee sitä mukaa, kun lämpötila kasvaa.
Kiinteä jää laajenee lämmetessään samaan tapaan kuin muutkin kiinteät aineet.
Olomuodon muutoksen aikana tapahtuu tapahtuu suuri muutos: jään tiheys on huomattavasti pienempi kuin nestemäisen veden.
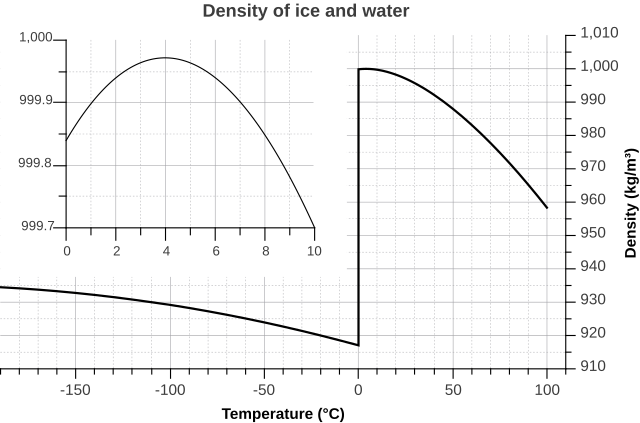
https://commons.wikimedia.org/wiki/File:Density_of_ice_and_water_(en).svg
b) Koska 0 °C vesi on kevyempää kuin +4 °C vesi, pakkasella vesistöt jäätyvät pinnalta. Lisäksi jään tiheys on pinenempi kuin nestemäisen veden, joten jää kelluu eikä vajoa pohjaan. Jää ja sen päälle satava lumi toimivat myös lämpöeristeenä. Järven tai meren syvänteessä on +4 °C vettä.
c) Jää vesiputkien tai astioiden sisällä laajenee sään lauhtuessa. Laajeneminen voi halkaista putken tai saavin.
10.
a) o K = –273,15 °C
b) 1535 °C = (1535+273) K = 1808 K
c) 77 K = (77 – 273 ) °C = –196 °C
11.
a) Väärin. Alumiinin α=0,000 023 1/K ja kuparin α=0,000 017 1/K.
b) Oikein.
c) Oikein. Järven pohjassa on tihein 4 °C vesi, jään alla lämpötila on lähellä jäätymispistettä.
d) Väärin. Nestelämpömittarin toiminta perustuu nesteen lämpölaajenemiseen. Aikaisemmin kuumemittareissa oli elohopeaa, nykyään yleensä galliumia sisältävä metalliseos (Ga, In, Sn, Zn).
12.
a) [[$$ \begin{split}\Delta T &= 1\,{}^\circ\rm{C}\\ \Delta l &= \alpha \cdot l \cdot \Delta T\\&=0{,}0000168 \frac{1}{\,{}^\circ\rm{C}}\cdot1\,\rm{m}\cdot1\,{}^\circ\rm{C}\\&=0{,}0000168\,\rm{m} \\ &\approx 0{,}02\,\rm{mm}=20 \,µ m \end{split} $$]]
b)
[[$$ \begin{split}\Delta T &= 100\,{}^\circ\rm{C}\\ \Delta l &= \alpha \cdot l \cdot \Delta T\\&=0{,}0000168 \frac{1}{\,{}^\circ\rm{C}}\cdot1\,\rm{m}\cdot100\,{}^\circ\rm{C}\\&=0{,}00168\,\rm{m} \\ &\approx 2\,\rm{mm} \end{split} $$]]
Luku 2. Lämpöenergia on energiamuoto
Energiamuotoja voi ryhmitellä ja nimetä monella tavalla.
- liike-energia eli kineettinen energia
- pyörimisenergia on eräs kineettisen energian muoto
- asemaenergia eli potentiaalienergia painovoimakentässä (putoavan pallon asemaenergia muuttuu liike-energiaksi)
- kineettinen ja potentiaalienergia yhdessä ovat mekaanista energiaa
- sähköinen potentiaalienergia: varauksen potentiaali sähkökentässä=jännite
[[$ U=E : Q $]] - lämpöenergia
- säteilyenergia
- kemiallinen enrgia on aineen kemiallisiin sidoksiin varastoitunutta energiaa
15.
a) kemiallinen energia → lämpöenergia
b) säteilyenergia → lämpöenergia
16.
Seoksen osia on saman verran, joten seoksen lämpötila on alkuperäisten lämpötilojen keskiarvo.
a) [[$$ \frac{30+70}{2}\,{}^\circ\rm{C} = \frac{100}{2}\,{}^\circ\rm{C} = 50\,{}^\circ\rm{C} $$]]
b) [[$$ \frac{40+80}{2}\,{}^\circ\rm{C} = \frac{120}{2}\,{}^\circ\rm{C} = 60\,{}^\circ\rm{C} $$]]
17.
Nuotiossa ja tähtisadetikussa kemiallinen energia muuttuu nopeasti lämpö- ja säteilyenergiaksi. Nuotion yläpuolella kuumeneva ilma laajenee ja saa liike-energiaa. Makkaraan siirtyy lämpöenergiaa sekä johtumalla ilmasta että säteilynä.
Makkaranpopsijan elimistössä makkaran kemiallinen energia varastoituu ja vapautuu myöhemmin haravoidessa (työssä) liike-energiana ja lämpönä. Kompostissa lehdet maatuvat, kun lahottajat käyttävät niitä ravintonaan. Samalla vapautuu hitaasti lämpöenergiaa.
18. Työssä verrataan hopean ja veden kykyä varastoida lämpöenergiaa.
Ominaislämpökapasiteetti [[$ c $]] mittaa aineen kykyä varastoida lämpöenergiaa.
[[$$ c=\frac{\Delta E}{m\cdot\Delta T} $$]]
Kun massan [[$ m $]] lämpötila muuttuu [[$\Delta T$]] verran, energiaa siirtyy [[$ \Delta E $]] verran.
Kun ominaislämpökapasiteetti tunnetaan, voidaan ratkaista siirtyneen energian määrä.
[[$$ \Delta E = c \cdot m \cdot \Delta T $$]]
Esimerkiksi veden ominaislämpökapasiteetti on 4,2 kJ/(kg·℃). Jos 2 kg vettä lämpenee 10 ℃, tarvitaan energiaa
[[$$ \begin{split}\Delta E &= 4,2\,\rm{kJ/kg} \cdot 2\,\rm{kg} \cdot 10\,{}^\circ\rm{C}\\&=84\,\rm{kJ}\\&=84\,000\,\rm{J} \end{split} $$]]
Veden jäähtyessä saman verran energiaa vapautuu.
19.
Kokeessa verrataan veden ja tuntemattoman nesteen kykyä varastoida lämpöä. Molempia nesteitä on yhtä paljon; jos tuntematon neste olisi vettä, seoksen lämpötila olisi alkuperäisten lämpötilojen keskiarvo.
Tuntematon neste jäähtyy [[$ (80-32)\,{}^\circ\rm{C} =48\,{}^\circ\rm{C} $]] ja vesi lämpenee [[$ (32-20)\,{}^\circ\rm{C} =12\,{}^\circ\rm{C} $]] . Veden luovuttama energiamäärä on sama kuin nesteen vastaanottama energiamäärä. Koska tuntemattoman nesteen lämpötila muuttuu enemmän, se tarkoittaa, että sen kyky varastoida lämpöä on huonompi kuin vedellä.
20.
a) Lämpöenergiaa siirtyy kuumasta vedestä kylmiin perunoihin, joten vesi jäähtyy.
b) Veden kyky varastoida lämpöenergiaa (ominaislämpökapasiteetti) on suurempi kuin ilman. Se tarkoittaa, että veden lämmittämiseen tarvitaan enemmän energiaa kuin ilman lämmittämiseen. Siksi vesi lämpenee hitaammin.
Luku 3. Olomuodonmuutokset
21.
a. sulaminen
b. tiivistyminen
c. sublimoituminen
23.
a. Vesi höyrystyy märästä pyyhkeestä. Höyrystyminen vaatii energiaa, joka siirtyy lämpönä sekä ilmasta että pullosta.
b. Kuumassa ihminen hikoilee ja iholta haihtuu vesihöyryä. Höyrystyminen sitoo lämpöä. Pintaverenkierron kiihtyminen tehostaa kehon lämmön siirtymistä ilmaan.
(Myöhemmin opimme, että ilma johtaa myös huonosti lämpöä. Siksi lämpöenergia siirtyy hitaasti ilmasta kehoon ja 100 ℃ saunassa voi oleskella, vaikka 100 ℃ vesi aiheuttaisi heti pahan palovamman.)
c, Ilma jäähtyy kylmän pinnan vieressä ja ilmassa oleva vesihöyry tiivistyy nestemäiseksi vedeksi.
24.
a. kiinteä
b. neste
c. aine on sulanut kokonaan nesteeksi
d. kiinteä kappale alkaa sulaa
e. neste alkaa kiehua
f. 630 kJ – 52 kJ = 578 kJ
Vaiheet:
| A | Aine on kiinteää. Lämmittäminen alkaa. |
| B =A-C | Aine lämpenee mutta pysyy edelleen kiinteänä. |
| C | Aine alkaa sulaa. Aineen sulamispiste on 79 ℃. |
| D = C-E | Aine on osin kiinteää, osin nestettä. |
| E | Aine on sulanut kokonaan nesteeksi. |
| F | Neste lämpenee. Höyrystymistä |
| G | Neste alkaa kiehua. Aineen kiehumispiste on 436 ℃. |
| H | Kiehuminen jatkuu, kunnes kaikki neste on höyrystynyt. |
25.
a. Jään ominaissulamislämpö on [[$ s=333 \,\rm{kJ/kg} $]].
Se tarkoittaa, että 1 kg:n sulattamiseen tarvitaan 333 kJ energiaa.
Puolen kilon sulattamiseen tarvitaan
[[$ E=sm=333 \,\rm{kJ/kg}\cdot 0{,}5\,\rm{kg} = 166{,}5 \rm{kJ} \approx 170 \rm{kJ} $]]
b. Veden jäätyessä energiaa vapautuu saman verran kuin jään sulaessa sitoutuu, eli 170 kJ.