5. Ioniyhdisteiden ominaisuuksia

Ioniyhdiste rakentuu positiivisista ja negatiivisista ioneista, jotka muodostavat kiinteässä olomuodossa ollessaan säännöllisen, kolmiulotteisen kiderakenteen.
Tuttuja ioniyhdisteitä ovat esimerkiksi ruokasuola NaCl ja monet kivilajit, kuten kuvan graniitti.

Ruokasuolaa ja graniittia.
Korkeat sulamis- ja kiehumispisteet
Ionien väliset sähköiset vetovoimat ovat vahvoja. Ioneista rakentuvat aineet ovat kovia, ja niillä on korkeat sulamis- ja kiehumispisteet. Ioniyhdiste kuitenkin rikkoontuu iskusta, kun samanmerkkiset ionit joutuvat vastakkain.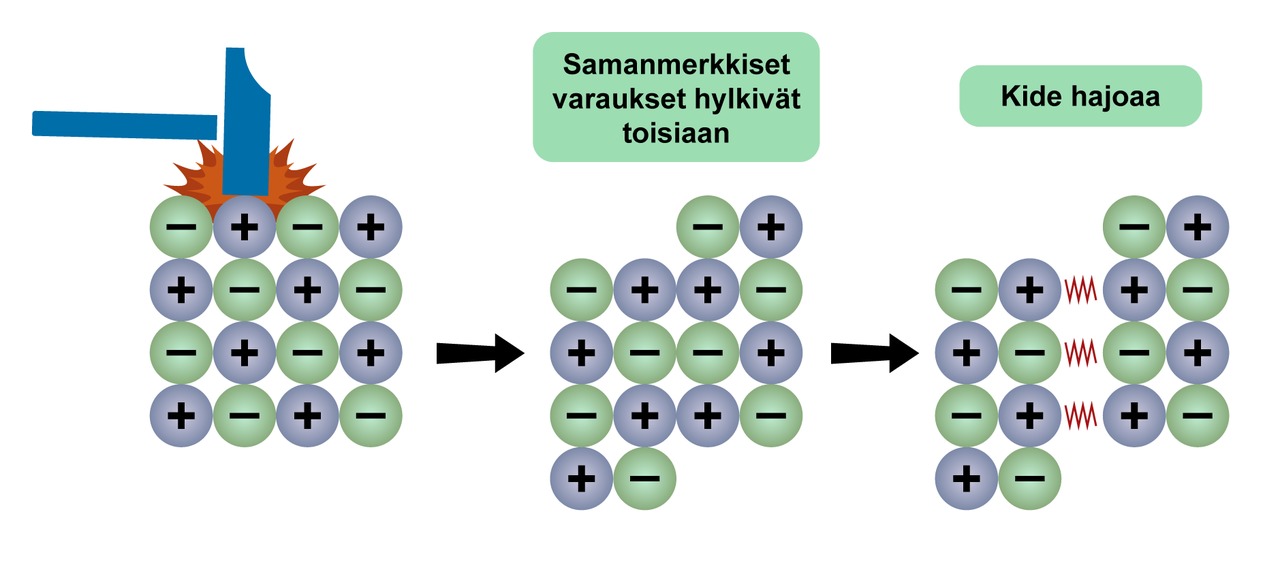
Liukoisuus
Ioniyhdisteet liukenevat veteen, mutta liukoisuuksista on suuria eroja. Esimerkiksi ruokasuola liukenee helposti veteen, kun taas monet kivilajit huonosti. Sulana ja vesiliuoksina ioniyhdisteet johtavat hyvin sähköä, kun taas kiinteänä ja kuivana ne ovat hyviä sähkön-, ja lämmöneristeitä. Ioniyhdisteiden sähkönjohtavuus perustuu siihen, että vesimolekyylit liikkuvat ionien väliin, mikä heikentää ionien välistä sähköistä vetovoimaa. Ionit joutuvat yhtä etäämmälle toisistaan, kunnes lopulta eroavat kokonaan. Ionit siirtyvät veden joukkoon ja voivat toimia sähkön kuljettajina. Ioniyhdisteen kuumentaminen saa ionit värähtelemään yhä voimakkaammin. Jossain vaiheessa värähtely on niin voimakasta, että ionit irtoavat toisistaan ja aine sulaa. Sulassa ionit pääsevät liikkumaan vapaasti ja toimimaan sähkönkuljettajina.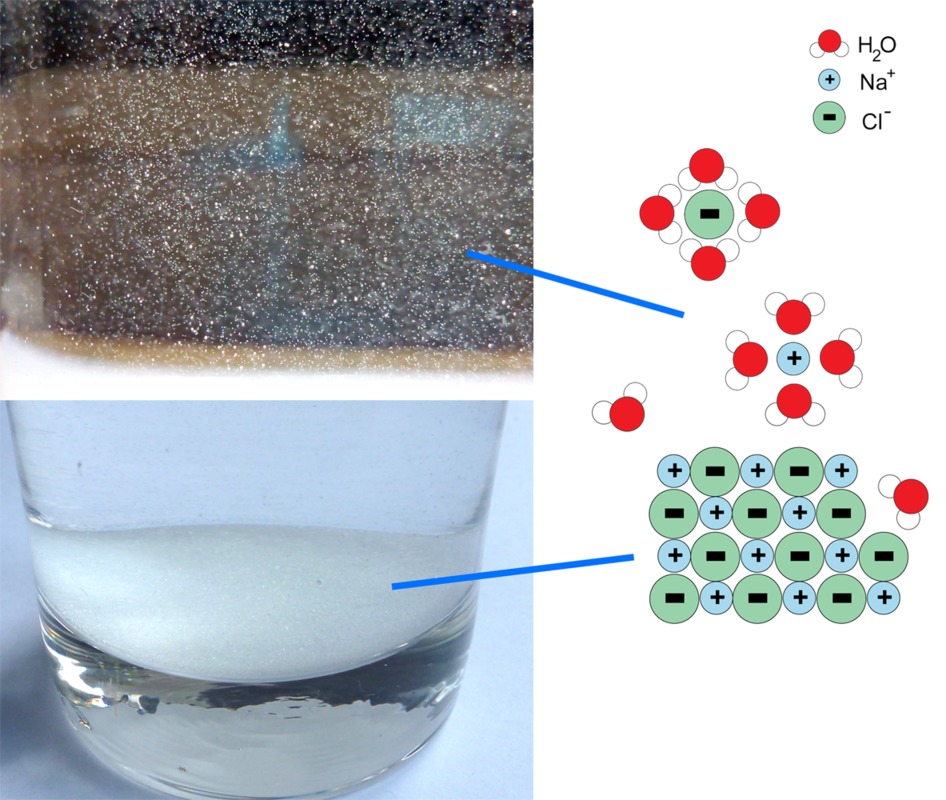
Video erilaisten yhdisteiden sähkönjohtavuudesta. Tarkkaile johtokykymittarin punaista valoa.