7. Karboksyylihapot ja esterit
1. Virittäytyminen – mikä tekee ruoasta happaman?
2. Karboksyylihappot aiheuttavat happamaa makua
Karboksyylihapon tunnistaa hiiliketjuun liittyneestä karboksyyliryhmästä (-COOH). Karboksyylihappomolekyylin hiilivetyketju voi olla suora, haaroittunut ja rengas. Hiilivetyketjuun voi liittyä useampi kuin yksi karboksyylihapporyhmä. Karboksyylihappoja löytyy monista hedelmistä ja marjoista, kuten puolukasta, sitruunasta tai viinimarjoista. Karboksyylihapot saavat nimensä mukaisesti aikaan marjojen ja hedelmien happaman maun.
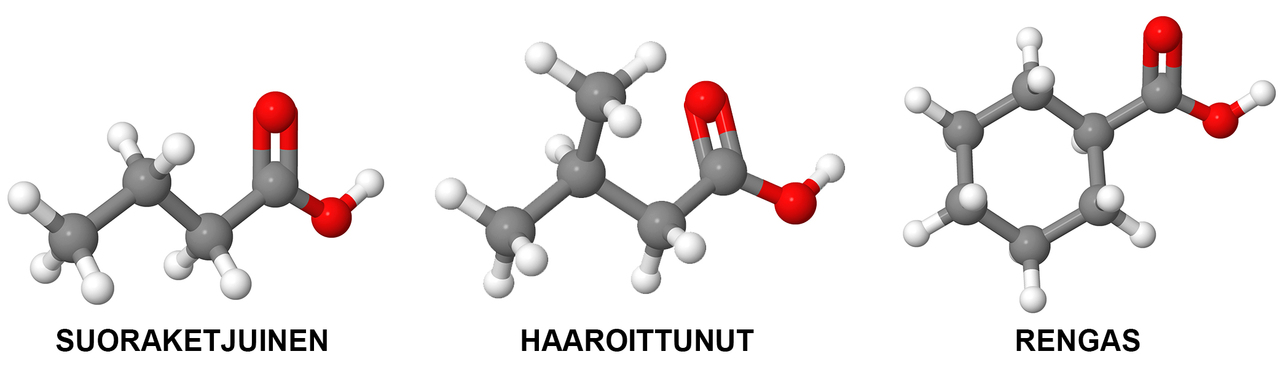
 Karboksyylihapot nimetään hiilirungon peruseella. Nimen runko muodostetaan hiiliatomien lukumäärän mukaan, joka on vastaavalla alkaanilla, ja nimen loppuosa on -happo.
Karboksyylihapot nimetään hiilirungon peruseella. Nimen runko muodostetaan hiiliatomien lukumäärän mukaan, joka on vastaavalla alkaanilla, ja nimen loppuosa on -happo.
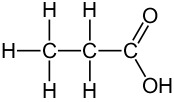
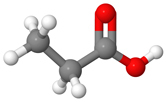
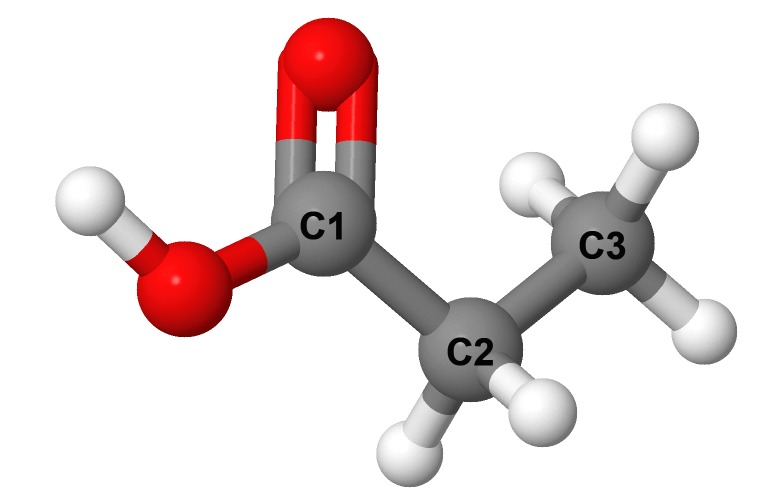
Esimerkiksi propaanihapossa etuliite propaani- tarkoittaa, että karboksyylihapon hiilirunko on kolmen hiilen pituinen alkaani, ja nimen pääte -happo sitä, että hiiliketjun päässä on COOH-ryhmä. Kaikki hiili-hiili- ja hiili-vety- ja vety-happisidokset ovat yksinkertaisia sidoksia. COOH-ryhmän toinen happiatomi kiinnittyy hiiliatomiin kaksinkertaisella sidoksella.
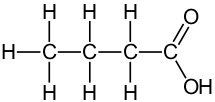
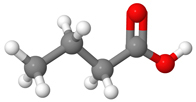
3. Neljä keveintä karboksyylihappoa
4. Karboksyylihappojen kemiallisia ominaisuuksia
Karboksyylihappojen happamuus voidaan todeta pH-paperilla. Karboksyylihapot ovat myös syövyttäviä. Katso oheisesta videosta, miten ne reagoivat magnesiumin kanssa. Muurahaishappo on videon hapoista vahvin.
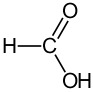
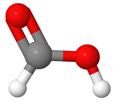
5. Metaanihappo eli muurahaishappo
Metaanihappo (HCOOH) on pienimolekyylisin karboksyylihappo. Metaanihappoa nimitetään myös muurahaishapoksi, koska muurahaiset ja monet muut hyönteiset erittävät sitä. Muurahaishappo on huoneenlämmössä pistävän hajuinen ja syövyttävä väritön neste. Muurahaishappoa käytetään eläinten rehun säilöntäaineena, desinfiointiaineena tai tekstiilien ja paperin värjäysaineena.

Muurahaiset erittävät muurahaishappoa puolustamista ja saalistusta varten.
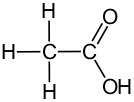
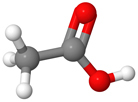
6. Etaanihappo eli etikkahappo
Etaanihappo eli etikkahappo CH3COOH on väritöntä, pistävän hajuista, syövyttävää nestettä, josta tehdään vedellä laimentamalla ruokaetikkaa. Sitä käytetään mausteena ja säilöntäaineena. Etikkahappo on myös tärkeä teollisuuden raaka-aine. Sitä käytetään muovien, vaatteiden, hajusteiden, painovärien ja lääkkeiden valmistuksessa.

Etanoli hapettuu etikkahappobakteerien vaikutuksesta etaanihapoksi eli etikkahapoksi, jota käytetään paljon ruoanlaitossa.
7. Marjojen ja hedelmien hapot
 Marjoissa ja hedelmissä olevia happoja nimitetään yleisesti hedelmähapoiksi. Puolukassa, lakassa ja karpaloissa on bentsoehappoa. Siinä bentseenirenkaaseen on liittynyt yksi karboksyylihapporyhmä.
Marjoissa ja hedelmissä olevia happoja nimitetään yleisesti hedelmähapoiksi. Puolukassa, lakassa ja karpaloissa on bentsoehappoa. Siinä bentseenirenkaaseen on liittynyt yksi karboksyylihapporyhmä.
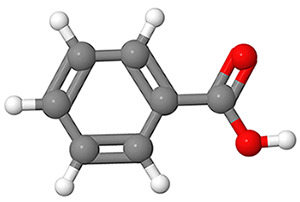
![]() Bentsoehappo
Bentsoehappo
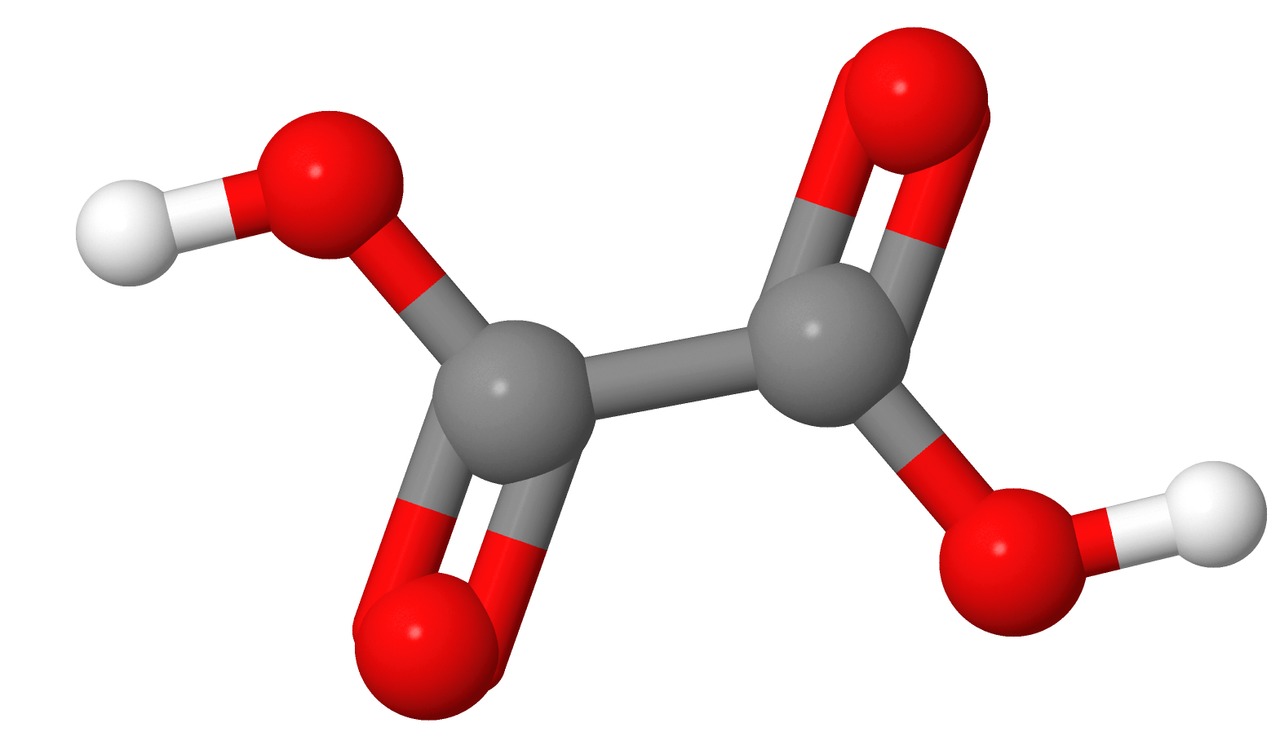
Raparperissa, suolaheinässä ja ketunleivässä on oksaalihappoa (COOH)2. Siinä hiiliketjuun on liittynyt kaksi karboksyylihapporyhmää. Oksaalihapon ja kalsiumionien reaktiossa muodostuu niukkaliukoista kalsiumoksalaattia, minkä vuoksi raparperiruokien kanssa olisi hyvä nauttia jotain kalsiumpitoista maitotuotetta. Näin oksaalihappo saostuisi jo maitotuotteessa olevan kalsiumin kanssa eikä kuluttaisi elimistön kalsiumioneja. Elimistössä kalsiumoksalaatti voi kerääntyä munuaisiin ja muodostaa munuaiskiviä.
![]() Oksaalihappo
Oksaalihappo

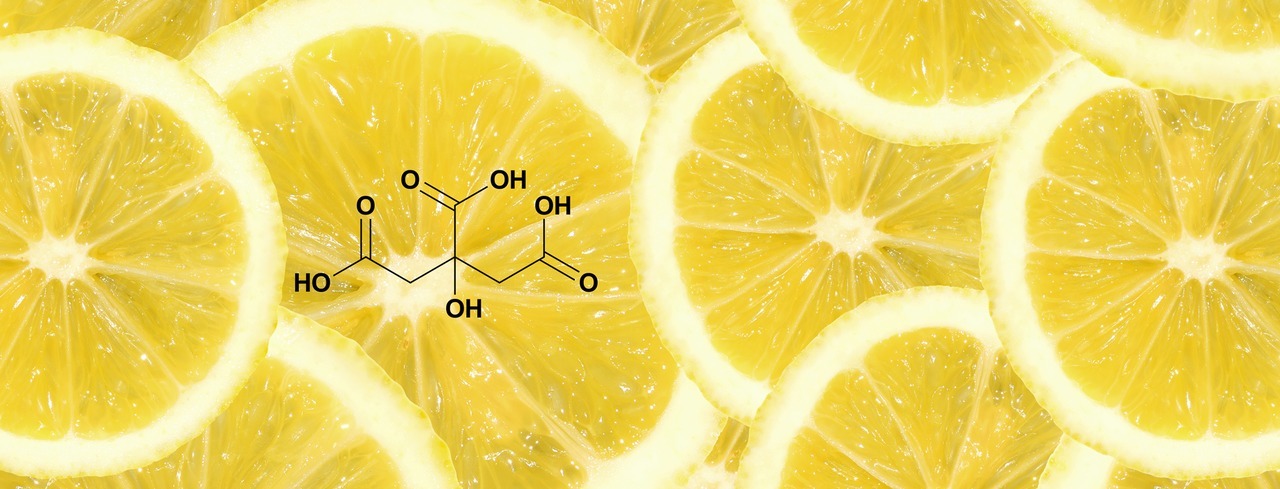
Appelsiinissa, greippissä ja sitruunassa on sitruunahappoa. Siinä hiiliketjuun on liittynyt kolme karboksyylihapporyhmää.
![]() Sitruunahappo
Sitruunahappo
8. Kuvagalleria: karboksyylihappoja luonnossa
9. Maitohappo
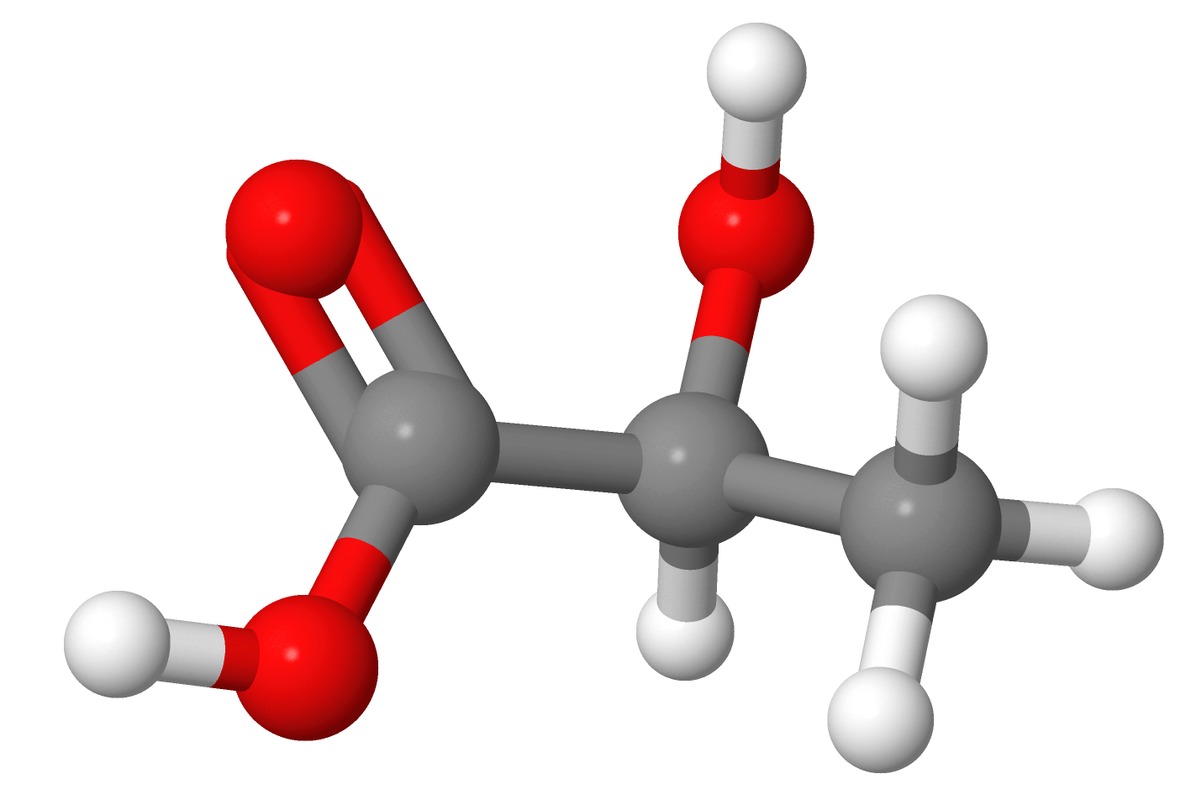
Elimistö saa tarvitsemansa energiansa pääasiassa sokereista ja rasvoista. Voimakkaassa rasituksessa on mahdollista, ettei soluun ehdi kulkeutua riittävää määrää happea ja lihaksiin muodostuu maitohappoa CH3CHOHCOOH, joka kipeyttää lihakset. Maitohappomolekyylissä on karboksyylihapon happoryhmä ja alkoholin hydroksyyliryhmä.
Maitohappoa hyödynnetään ruoanlaitossa. Esimerkiksi piimäjuuston valmistuksessa maitohappo ja lämpö rikkovat maidon valkuaisaineiden kolmiulotteisen rakenteen. Yhdisteellä on myös teollista merkitystä, sillä jotkin biohajoavista muoveista on valmistettu käyttämällä lähtöaineena maitohappoa ja maissitärkkelystä.
10. Hapon ja alkoholin reaktiossa muodostuu esteriä
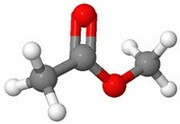
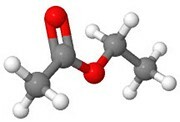
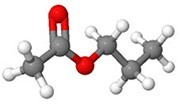
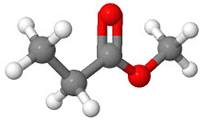
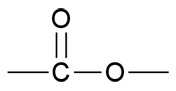 Esterit ovat hyväntuoksuisia yhdisteitä, jotka muodostuvat karboksyylihapon ja alkoholin reagoidessa keskenään. Reaktiotuotteena muodostuu esteriä ja vettä. Esterien toiminnallinen ryhmä on -COO-. Monilla estereillä on voimakas ominaishaju, ja ne ovat monien luonnosta löytyvien hedelmien ja marjojen tuoksujen aiheuttajia. Niistä käytetään yleisnimitystä hedelmäesterit.
Esterit ovat hyväntuoksuisia yhdisteitä, jotka muodostuvat karboksyylihapon ja alkoholin reagoidessa keskenään. Reaktiotuotteena muodostuu esteriä ja vettä. Esterien toiminnallinen ryhmä on -COO-. Monilla estereillä on voimakas ominaishaju, ja ne ovat monien luonnosta löytyvien hedelmien ja marjojen tuoksujen aiheuttajia. Niistä käytetään yleisnimitystä hedelmäesterit.
 Estereitä voidaan valmistaa myös laboratoriossa. Laboratoriossa valmistettuja estereitä käytetään esim. hajuvesissä ja elintarvikkeiden lisäaineina.
Estereitä voidaan valmistaa myös laboratoriossa. Laboratoriossa valmistettuja estereitä käytetään esim. hajuvesissä ja elintarvikkeiden lisäaineina.
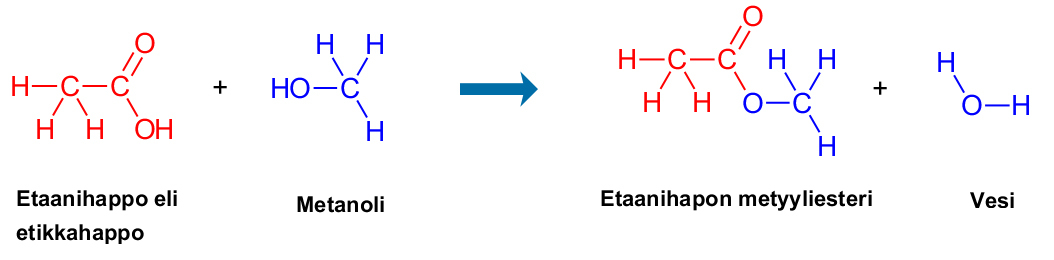
Esterit muodostuvat esteröitymisreaktiosta:
happo + alkoholi [[$ \rightarrow $]] esteri + vesi.
Esimerkiksi etaanihapon ja metanolin reaktiossa muodostuu etaanihapon metyyliesteriä ja vettä. Esteri tuoksuu liimalta. Vastaavasti kun butaanihappo ja metanoli reagoivat, reaktiossa syntyy butaanihapon metyyliesteriä ja vettä. Tämä yhdiste taas tuoksuu ananakselta.
Tiivistelmä
- Karboksyylihapon tunnistaa hiiliketjuun liittyneestä karboksyyliryhmästä (-COOH).
- Karboksyylihapot saavat nimensä mukaisesti aikaan marjojen ja hedelmien happaman maun.
- Metaanihappo (HCOOH) on pienimolekyylisin karboksyylihappo. Metaanihappoa nimitetään myös muurahaishapoksi, koska muurahaiset ja monet muut hyönteiset erittävät sitä.
- Etaanihappo eli etikkahappo (CH3COOH) on tärkeä teollisuuden raaka-aine.
- Marjoissa ja hedelmissä olevia happoja nimitetään yleisesti hedelmähapoiksi.
- Esterit ovat hyväntuoksuisia yhdisteitä, jotka muodostuvat karboksyylihapon ja alkoholin reagoidessa keskenään.