Tehtävät 4,2 S.114
T.9
Selvitä, millainen ioni muodostuu, kun seuraava atomi saa jalokaasun elektronirakenteen.
a) Litium: Li+
b) Typpi: N3-
c) Strontium: Sr2+
d) Alumiini: Al3+
e) Happi: O2-
f) Fluori: F-
Muodosta ioneista kuusi eri yhdistettä.
LiF, AlN, SrO, Al2O3, Li3N
T.10
X ja Y ovat alkuaineita, jotka järjestysluvut ovat 9 ja 19
a) Tunnista alkuaineet taulukkokirjan avulla.
K (Järjestysluku 19)
F (Järjestysluku 9)
b) Hae taulukkokirjasta näistä alkuaineista muodostuvien ionien kaavat ja kirjoita ionien muodostaman yhdisteen kaava.
K+ + F- -->KF
c) Mitkä seuraavista ominaisuuksista kuvaavat tätä yhdistettä
- Vesiliukoinen
- Hyvä sähköjohtokyky kiinteänä
- Korkea sulamispiste
- Helposti muokattava
- Hyvä lämmöjohtokyky
T.13
Selvitä seuraavien ilmiöiden syy.
a) Kipsistä (CaSO4) valmistetusta koristeesineestä lohkeaa helposti palasia, kun se putoaa lattialle.
- Kipsi on kaksiumsulfaattia, joka on kovaa mutta haurasta ioniyhdistettä. Lattialle putoaminen saa aikaan sen, että sähköisesti samoin varautuneita ioneja joutuu vierekkäin ja näiden hylkimisvoima rikkoo hilarakenteen.
b) Alkaliparistot sisältävät kaliumhydroksidin vesiliuostaa (KOH(aq)).
- Kaliumhydroksidi on ioniyhdise, jonka vesiliuos on elektrolyytti eli se johtaa sähköä.
c) Marmonia (CaSO3) voidaan muotoilla patsaaksi taltalla ja vasaralla.
- Marmori on kalsiumkarbonaattia, joka on kovaa mutta haurasta ioniyhdistettä eli sitä voi muotoilla taltalla ja vasaralla.
T.17
Nimeä seuraavat ioniyhdisteet.
a) NaBr= Natriumbromidi
b) MgCl2= Magnesiumkloridi
c) Al(NO3)3= Alumiininitraatti
d) (NH4)2SO4= Ammoniumsulfaatti
e) NH4CH3COO= Ammoniumasetaatti
f) CaC2O4= Kalsiumoksalaatti
g) Fe2O3= Rauta(III)oksidi
h) FeO= Rauta(II)oksidi
i) AuCl3= Kulta(III)kloridi
T.18
Kirjoita kaava seuraaville ioniyhdisteille.
a) Natriumnitraatti: NaNO3
b) Kalsiumkarbonaatti: CaCO3
c) Kalsiumsulfatti: CaSO4
d) Tina(IV)kloridi: SnCl4
e) Vanadiini(V)oksidi: V2O5
f) Kaliumpermanganaatti: KMnO4
g) Ammoniumfosfaatti: (NH4)3PO4
T.20
Järjestä alkuaineet elektronegatiivisuuden perusteella siten, että elektronegatiivisin on viimeisenä.
Typpi 3,0
Seleeni 2,4
Indium 1,7
Strontium 1,0
Hopea 1,9
Bromi 2,8
Jodi 2,5
Typpi, Bromi, Jodi, Seleeni, Hopea, Indium, Strontium
T.21
Tutki, missä kohdassa jaksollista järjestelmää seuraavat alkuaineet sijaitsevat. Päättele sen perusteella, kumpi alkuaineista on elektronegatiivisempi. Tarkista ennustuksesi taulukkokirjan elektronegatiivisuusarvojen avulla.
a) Bromi ja platina
- Bromi
b) Kalium ja kalsium
- Kalsium
c) Fosfori ja fluori
- Fluori
d) Tina ja titaani
- Tina
T.22
Päättelee, mitkä seuraavista sidoksista ovat poolisia.
C=O
C-H
O-H
H-H
N-H
Poolisia sidoksia ovat kaikki muut paitsi H-H-sidos, koska muissa sidoksissa alkuaineiden välillä on elektronegatiivisuusero.
T.23
Lisää oheisiin molekyyleihin elektronegatiivisuusarvojen perusteella merkinnät ja
ja 
a) Br-Br
b)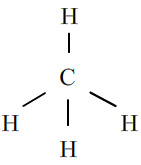
C: 4
H:
c) O=C=O
C: 2
O:
d) H-Cl
Cl:
T.25
Tutki seuraavien molekyylien muotoja joko molekyylimallinnusohjelmalla tai taulukkokirjan avulla. Päättele onko molekyyli poolinen vai pooliton. Perustele vastauksesi.
a) Vertyfluori HF
H: 2,1
F: 4,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
b) Tetrakloorimetaani CCl4 (vertaa metraanimolekyyliin)
C: 2,5
Cl: 3,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
c) Trikloorimetaani CHCl3
C: 2,5
H: 2,1
Cl: 3,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
d) Hiilidioksidi CO2
C: 2,5
O: 3,5
v: Poolinen, koska niiden negatiivisuus arvo on eri.
T.27
Nimeä seuraavat molekyyliyhdisteet
a) NO typpioksidi
b) NO2 typpidioksidi
c) SO3 rikkitrioksidi
d) CCl4 tetrakloorimetaani
e) HBr Vetybromidi
f) PCl5 fosforipentakloridi
Selvitä, millainen ioni muodostuu, kun seuraava atomi saa jalokaasun elektronirakenteen.
a) Litium: Li+
b) Typpi: N3-
c) Strontium: Sr2+
d) Alumiini: Al3+
e) Happi: O2-
f) Fluori: F-
Muodosta ioneista kuusi eri yhdistettä.
LiF, AlN, SrO, Al2O3, Li3N
T.10
X ja Y ovat alkuaineita, jotka järjestysluvut ovat 9 ja 19
a) Tunnista alkuaineet taulukkokirjan avulla.
K (Järjestysluku 19)
F (Järjestysluku 9)
b) Hae taulukkokirjasta näistä alkuaineista muodostuvien ionien kaavat ja kirjoita ionien muodostaman yhdisteen kaava.
K+ + F- -->KF
c) Mitkä seuraavista ominaisuuksista kuvaavat tätä yhdistettä
- Vesiliukoinen
- Hyvä sähköjohtokyky kiinteänä
- Korkea sulamispiste
- Helposti muokattava
- Hyvä lämmöjohtokyky
T.13
Selvitä seuraavien ilmiöiden syy.
a) Kipsistä (CaSO4) valmistetusta koristeesineestä lohkeaa helposti palasia, kun se putoaa lattialle.
- Kipsi on kaksiumsulfaattia, joka on kovaa mutta haurasta ioniyhdistettä. Lattialle putoaminen saa aikaan sen, että sähköisesti samoin varautuneita ioneja joutuu vierekkäin ja näiden hylkimisvoima rikkoo hilarakenteen.
b) Alkaliparistot sisältävät kaliumhydroksidin vesiliuostaa (KOH(aq)).
- Kaliumhydroksidi on ioniyhdise, jonka vesiliuos on elektrolyytti eli se johtaa sähköä.
c) Marmonia (CaSO3) voidaan muotoilla patsaaksi taltalla ja vasaralla.
- Marmori on kalsiumkarbonaattia, joka on kovaa mutta haurasta ioniyhdistettä eli sitä voi muotoilla taltalla ja vasaralla.
T.17
Nimeä seuraavat ioniyhdisteet.
a) NaBr= Natriumbromidi
b) MgCl2= Magnesiumkloridi
c) Al(NO3)3= Alumiininitraatti
d) (NH4)2SO4= Ammoniumsulfaatti
e) NH4CH3COO= Ammoniumasetaatti
f) CaC2O4= Kalsiumoksalaatti
g) Fe2O3= Rauta(III)oksidi
h) FeO= Rauta(II)oksidi
i) AuCl3= Kulta(III)kloridi
T.18
Kirjoita kaava seuraaville ioniyhdisteille.
a) Natriumnitraatti: NaNO3
b) Kalsiumkarbonaatti: CaCO3
c) Kalsiumsulfatti: CaSO4
d) Tina(IV)kloridi: SnCl4
e) Vanadiini(V)oksidi: V2O5
f) Kaliumpermanganaatti: KMnO4
g) Ammoniumfosfaatti: (NH4)3PO4
T.20
Järjestä alkuaineet elektronegatiivisuuden perusteella siten, että elektronegatiivisin on viimeisenä.
Typpi 3,0
Seleeni 2,4
Indium 1,7
Strontium 1,0
Hopea 1,9
Bromi 2,8
Jodi 2,5
Typpi, Bromi, Jodi, Seleeni, Hopea, Indium, Strontium
T.21
Tutki, missä kohdassa jaksollista järjestelmää seuraavat alkuaineet sijaitsevat. Päättele sen perusteella, kumpi alkuaineista on elektronegatiivisempi. Tarkista ennustuksesi taulukkokirjan elektronegatiivisuusarvojen avulla.
a) Bromi ja platina
- Bromi
b) Kalium ja kalsium
- Kalsium
c) Fosfori ja fluori
- Fluori
d) Tina ja titaani
- Tina
T.22
Päättelee, mitkä seuraavista sidoksista ovat poolisia.
C=O
C-H
O-H
H-H
N-H
Poolisia sidoksia ovat kaikki muut paitsi H-H-sidos, koska muissa sidoksissa alkuaineiden välillä on elektronegatiivisuusero.
T.23
Lisää oheisiin molekyyleihin elektronegatiivisuusarvojen perusteella merkinnät
a) Br-Br
b)

C: 4
H:
c) O=C=O
C: 2
O:
d) H-Cl
Cl:
T.25
Tutki seuraavien molekyylien muotoja joko molekyylimallinnusohjelmalla tai taulukkokirjan avulla. Päättele onko molekyyli poolinen vai pooliton. Perustele vastauksesi.
a) Vertyfluori HF
H: 2,1
F: 4,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
b) Tetrakloorimetaani CCl4 (vertaa metraanimolekyyliin)
C: 2,5
Cl: 3,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
c) Trikloorimetaani CHCl3
C: 2,5
H: 2,1
Cl: 3,0
v: Poolinen, koska niiden negatiivisuus arvo on eri.
d) Hiilidioksidi CO2
C: 2,5
O: 3,5
v: Poolinen, koska niiden negatiivisuus arvo on eri.
T.27
Nimeä seuraavat molekyyliyhdisteet
a) NO typpioksidi
b) NO2 typpidioksidi
c) SO3 rikkitrioksidi
d) CCl4 tetrakloorimetaani
e) HBr Vetybromidi
f) PCl5 fosforipentakloridi