6. Ioniyhdisteitä muodostuu monissa reaktioissa
Arkipuheessa suolalla tarkoitetaan yleensä ruokasuolaa (NaCl), mutta kemiassa suola tarkoittaa suurta joukkoa ioniyhdisteitä. Ruokasuolan lisäksi suoloja ovat esimerkiksi kalsiumfluoridi ja rautaoksidi eli ruoste. Suoloja muodostuu muun muassa
- neutraloitumisreaktioissa
- metallin ja epämetallin reaktiossa
- saostumisreaktioissa
- hapon ja metallin reaktiossa.
Neutraloitumisreaktio
Happojen ja emästen neutraloitumisreaktiossa muodostuu suolaa ja vettä. Reaktion päätyttyä suola on veteen liuenneena, mutta kun vesi haihdutetaan pois, suola saadaan talteen kiinteänä ioniyhdisteenä. Neutraloitumisreaktiossa syntyvä suola syntyy hapon negatiivisesta ja emäksen positiivisesta ionista.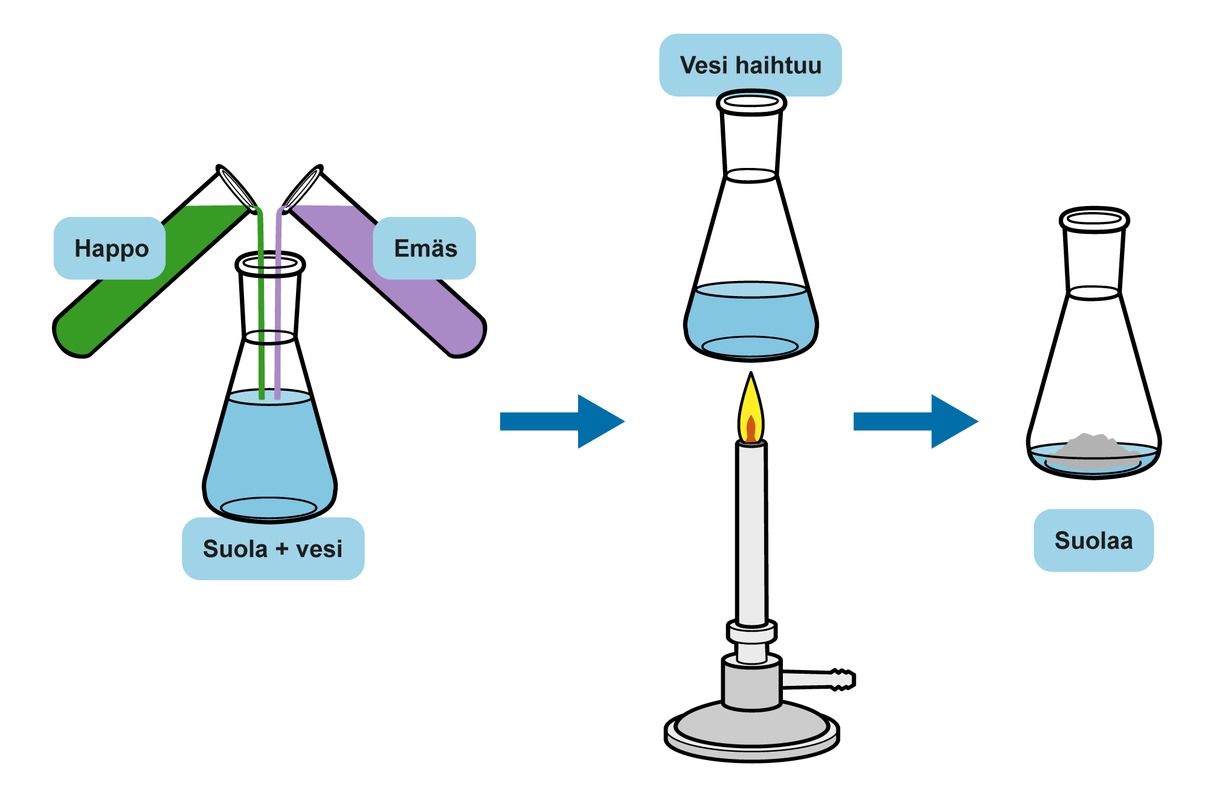
Hapon ja emäksen reaktiossa muodostu suolaa ja vettä. Kun vesi haihdutetaan, astiaan jää suolaa.
Metallin ja epämetallin reaktio
Metallin ja epämetallin reaktiossa voi muodostua suolaa. Esimerkiksi raudan palaessa muodostuu rautaoksidia. Raudan palamista tapahtuu esimerkiksi ruostumisessa, tähtisädetikun palaessa ja poltettaessa rautavillaa kemian tunnilla.
Alumiini ja jodi reagoivat kiivaasti muodostaen alumiinijodidia.
Saostumisreaktio
Saostumisreaktiossa muodostuu suolaa. Saostumisreaktiossa sekoitetaan toisiinsa kahta tai useampaa suolaliuosta. Lähtötilanteessa liuoksissa olevat ionit ovat veteen liuenneina, mutta kun liuokset sekoitetaan, eri liuosten ionit voivat reagoida keskenään, jolloin voi muodostua uusia veteen liukenemattomia suoloja.
Kobolttisulfaatin positiiviset koboltti-ionit ja ammoniumhydroksidin negatiiviset hydroksidi-ionit muodostavat veteen niukkaliukoisen kobolttihydroksidin.